
【题目】除去括号内杂质的有关试剂正确的是
A.苯(硝基苯):蒸馏水B.苯(Br2):NaOH溶液
C.乙酸(乙酸乙酯):氢氧化钠溶液D.乙烷(乙烯):酸性高锰酸钾溶液
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池,其原理如图所示。下列说法不正确的是
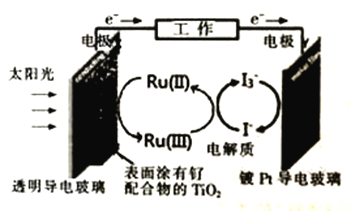
A. 电池工作时,能量的转化形式至少有三种
B. 放电时,I-和I3-的浓度均减小
C. Y电极为电池的正极,发生的反应为:I3-+2e-=3I-
D. 电池工作时,X电极上发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种优良的消毒剂,其溶解度约是Cl2的5倍,但温度过高、浓度过大时均易发生分解,因此常将其制成固体,以便运输和贮存。制备KClO2固体的实验裝置如图所示,其中A装置制备ClO2,B装置制备KClO2。请回答下列问题:
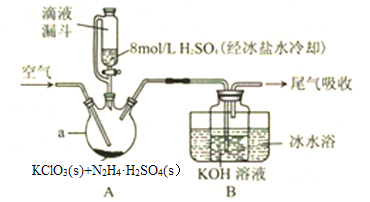
(1)仪器a的名称是________。
(2)滴液漏斗与普通分液漏斗相比,其优点是_________。
(3)加入的硫酸需要用冰盐水冷却的原因是_________。
(4)实验过程中通入空气的目的是________,空气流速过快或过慢,均降低KClO2产率,试解释其原因________ 。
(5)用图示装置制备的KClO2中含有较多杂质,其原因是________。
(6)A中制备ClO2的化学方程式为_________ 。
(7)有人认为用图示装置吸收ClO2易引起倒吸,但经过多次实验均未发现有倒吸现象,其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:

下列有关叙述不正确的是
A. 贝诺酯分子中有2种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. lmol乙酰水杨酸最多消耗3molNaOH
D. 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氮基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)△H<0,在其他条件不变的情况下,下列说法正确的是
CO2(g)+H2(g)△H<0,在其他条件不变的情况下,下列说法正确的是
A. 若在原电池中进行,反应放出的热量不变
B. 升高温度,反应速率加快,反应放出的热量不变
C. 改变压强,平衡不发生移动,反应放出的热量不变
D. 加入催化剂,改变了反应的途径,反应的△H也随之改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,将其一定量溶于水,有沉淀产生,在所得悬浊液中逐滴加入5mol/L的盐酸,右图表示盐酸加入量与沉淀量的变化关系,图中M点表示已加入的盐酸体积,则M点的体积是
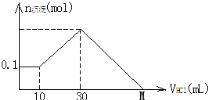
A. 70mL B. 130mL C. 120mL D. 100mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业上使用的印刷电路板,是在敷有铜膜的塑料板上以涂层保护所要的线路,然后用三氯化铁浓溶液作用掉(腐蚀)未受保护的铜膜后形成的。某工程师为了从使用过的腐蚀废液(含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费)中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,准备采用下列步骤:
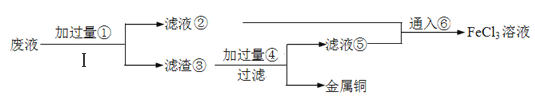
(1)步骤Ⅰ的操作名称:________;所需玻璃仪器:_________、_________、__________。
(2)写出FeCl3溶液与铜箔发生反应的离子方程式:______________________。
(3)检验废腐蚀液中是否含有Fe3+所需试剂名称:___________、实验现象:__________。
(4)向②中加入NaOH溶液并长时间暴露在空气中,此过程的现象:________________,此转化的化学方程式为:______________________________。
(5)写出③中所含物质:_________⑥发生反应的离子方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法表示下列反应的电子转移情况并将其改写成离子方程式: 3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,______________,离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POCl3是重要的基础化工原料,广泛用于制药、染料、表面活性剂等行业。一种制备POCl3的原理为:PCl3+Cl2+SO2=POCl3+SOCl2。某化学学习小组拟利用如下装置在实验室模拟制备POCl3。有关物质的部分性质如下:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其它 |
PCl3 | -93.6 | 76.1 | 1.574 | 遇水强烈水解,易与氧气反应 |
POCl3 | 1.25 | 105.8 | 1.645 | 遇水强烈水解,能溶于PCl3 |
SOCl2 | -105 | 78.8 | 1.638 | 遇水强烈水解,加热易分解 |

(1)仪器甲的名称为______________,与自来水进水管连接的接口编号是________________。(填“a”或“b”)。
(2)装置C的作用是___________________,乙中试剂的名称为____________________。
(3)该装置有一处缺陷,解决的方法是在现有装置中再添加一个装置,该装置中应装入的试剂为_________(写名称)。若无该装置,则可能会有什么后果?请用化学方程式进行说明__________________________。
(4)D中反应温度控制在60-65℃,其原因是_______________。
(5)测定POCl3含量。①准确称取30.70gPOCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;④以Fe3+为指示剂,用0.2000mol/LKSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
①滴定终点的现象为____________________,用硝基苯覆盖沉淀的目的是__________________。
②反应中POCl3的百分含量为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com