
【题目】氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为___________个。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为_______________。
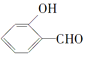 的沸点比
的沸点比![]() 高,原因是______________________。
高,原因是______________________。
(3)H+可与H2O形成H3O+,H3O+中O原子采用________杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为________________。
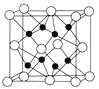
(4)CaF2离子晶体的晶胞结构如图所示。该离子化合物晶胞的边长为a cm,则晶体的密度是_____________g/cm3(只要求列出算式)。
【答案】 2 O—H键、氢键、范德华力 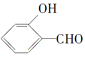 形成分子内氢键,而
形成分子内氢键,而![]() 形成分子间氢键,分子间氢键使分子间作用力增大 sp3 H2O中O原子有2对孤对电子,H3O+中O原子只有1对孤对电子,排斥力较小
形成分子间氢键,分子间氢键使分子间作用力增大 sp3 H2O中O原子有2对孤对电子,H3O+中O原子只有1对孤对电子,排斥力较小 ![]()
【解析】(1)氧元素是8号元素,基态原子的电子排布式为1s22s22p4,核外未成对电子数为2个,故答案为:2;
(2)共价键的键能大于氢键的作用力,氢键的作用力还大于范德华力,故H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、分子间的范德华力;含分子间氢键的物质的沸点大于分子内氢键物质的沸点,因此原因是前者易形成分子间氢键,后者易形成分子内氢键,故答案为:O-H键、氢键、范德华力;低;邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛形成分子间氢键,分子间氢键使分子间作用力增大
(3)H3O+价层电子对模型为四面体,氧原子采取sp3杂化.
H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,因为孤电子对间的排斥力>孤电子对与成键电子对间的排斥力>成键电子对间的排斥力,导致H3O+中H-O-H键角比H2O中H-O-H键角大.
故答案为:sp3;H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,排斥力较小;
(4)该晶胞中钙原子个数=8×![]() +6×
+6×![]() =4,氧原子个数=8,1mol晶胞的质量为4×78g,1mol晶胞的体积为NA×a3cm3,则该晶体的密度为÷4×78g NA×a3cm3=
=4,氧原子个数=8,1mol晶胞的质量为4×78g,1mol晶胞的体积为NA×a3cm3,则该晶体的密度为÷4×78g NA×a3cm3=![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A. 用水可以区分苯和四氯化碳
B. 用金属钠可以区分乙醇和乙醚
C. 用溴水可以区分乙烯和乙炔
D. 用酸性高锰酸钾溶液可以区分己烷和己烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境、保护地球已成为人类共同的呼声。
(1)下列措施不利于环境保护的是___________(选填字母,下同)。
A.推广使用无铅汽油 B.提倡家庭使用太阳能热水器
C.推广废旧电池单独回收 D.提倡家庭购买大排量汽车
(2)酸雨的PH<5.6,下列气体排放可能形成酸雨的是______________。
A.N2 B.CO C.SO2 D.氟氯代烷
(3)下列情况可能引起大气污染的是____________。
①煤的燃烧 ②工业废气任意排放 ③燃放鞭炮 ④飞机、汽车尾气的排放
A.只有①② B.只有②④
C.只有①②③ D.①②③④
(4)废弃的热塑性塑料通过清洗、熔融、重新制成塑料。塑料属于____________。
A.无机非金属材料 B.有机合成材料
C.复合材料 D.合金
(5)维生素C又称为抗坏血酸,在人体内有重要功能,其结构简式如下所示,则维生素C的分子式为_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:下表为25℃时某些弱酸的电离平衡常数。

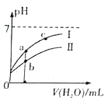
如图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。下列说法正确的是
A. 相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B. 向NaClO溶液中通入少量二氧化碳的离子方程式为:ClO-+CO2+H2O=HClO+CO32-
C. 图象中a点的酸的总浓度大于b点酸的总浓度
D. 图象中a、c两点处的溶液中c(R-)/[c(HR)c(OH-)]相等(HR代表CH3COOH或HClO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种烃,它们含碳质量分数相同,下列关于A和B的叙述正确的是( )
A. A和B一定是同分异构体B. A和B最简式一定相同
C. A和B不可能是同系物D. A和B的化学性质相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请认真审题并作答:
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_______________________。CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和CO2,由此可以推知CN22-的空间构型为__________________。
(2)三聚氰胺( )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸( )后,三聚氰酸与三聚氰胺分子相互之间通过______________结合。在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过______________结合。在肾脏内易形成结石。
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为_________。
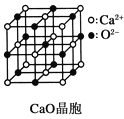
(4)CaO晶体和NaCl晶体的晶格能分别为:CaO 3401kJ·mol-1、NaCl 786kJ·mol-1。导致两者晶格能差异的主要原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 处于最低能量的原子叫做基态原子
B. 3p2表示3p能级有两个轨道
C. 同一原子中,1s、2s、3s电子的能量逐渐减小
D. 同一原子中,2p、3p、4p能级的轨道数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2,故常在实验室中用作吸湿剂和空气湿度指示剂。
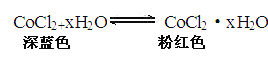
现有65g无水CoCl2,吸水后变成CoCl2·xH2O 119g。
(1)水合物中x=______;
(2)若该化合物中Co2+的配位数为6,而且经测定得知内界和外界占有Cl-的个数比为1:1,则其化学式可表示为:______
(Ⅱ)在极性分子中,正电荷中心同负电荷中心间的距离称为偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
(3)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0。
①试在方框中画出两种异构体的构型图:_________;___________________
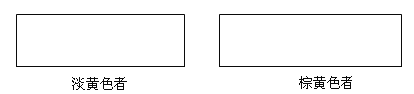
②该化合物的两种异构体在水中溶解度较大的是___________________(填“棕黄色者”或“淡黄色者”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com