
����Ŀ��ͭ���ʼ��仯�����ںܶ������ж�����Ҫ����;����ش��������⣺
(1)��ϸͭ�ۿ�����������ϡ������ȣ����Ʊ��������£�

��NH4CuSO3�н��������ӵĺ�������Ų�ʽΪ__________________��N��O��S����Ԫ�صĵ�һ�����ܴ�С˳��Ϊ____________(��Ԫ�ط���)��
����CuSO4��Һ�м��������ˮ��������[Cu(NH3)4]SO4������˵����ȷ����________��
A��������������ˮ��ԭ��֮һ��NH3���Ӻ�H2O����֮���γ������Ե��
B��NH3���Ӻ�H2O���ӣ����ӿռ乹�Ͳ�ͬ���������ӵļ���С��ˮ���ӵļ���
C��[Cu(NH3)4]SO4��Һ�м����Ҵ�������������ɫ�ľ���
D����֪3.4 g��������������ȫȼ����������Ⱦ�����壬���ų�a kJ��������NH3��ȼ���ȵ��Ȼ�ѧ����ʽΪ��NH3(g)��3/4O2(g)===1/2N2(g)��3/2H2O(g)����H����5a kJ��mol��1
(2)ͭ��������(CuMn2O4)���ڳ����´����������е�������Ϊ����(��SO2��Ϊ�ȵ�����)�����ݵȵ���ԭ����O3���ӵĿռ乹��Ϊ________��
(3)���벻ͬ��̬��ͭ���������ֻ�����������Ӿ�Ϊ�������ṹ(��ͼ��ʾ)��aλ����Clԭ��(����һ����λ��)���ӻ��������Ϊ____________________��

(4)��ͼ�ǽ���Ca��D���γɵ�ij�ֺϽ�ľ����ṹʾ��ͼ����֪�����Ͻ�������Ca��D�Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10��23 cm3��������γ�LaNinH4.5�Ͻ�(����뾧����϶���������)����LaNin��n��______________________(����ֵ)�����ںϽ��е��ܶ�Ϊ________(������λ��Ч����)��

���𰸡�1s22s22p63s23p63d10(��[Ar]3d10) N��O��S AC V�� sp3�ӻ� 5 0.083 g��cm��3
��������
��1����NH4CuSO3�н���������ΪCu+��ͭ��29��Ԫ�أ�ʧȥһ������������ͭ���ӣ�Nԭ��2p���Ϊ������ṹ����һ�����ܴ���Oԭ�ӣ�ͬһ����Ԫ�صĵ�һ����������ԭ���������������С��
A������������ˮ����֮����������
B������������Nԭ�Ӻ�ˮ����Oԭ�Ӿ�Ϊsp3�ӻ�����������Nԭ��ֻ��һ�Թ¶Ե��ӣ�ˮ������Oԭ�������Թ¶Ե��ӣ�
C�������������ܿ�֪���Ҵ����Ӽ�������ˮ�ļ��ԣ�
D��ȼ���ȵ��Ȼ�ѧ����ʽ�У�����H2OΪҺ̬��
��2��O3������SO2��Ϊ�ȵ����壬�ȵ����������ͬ�Ŀռ乹�ͣ�
��3��aλ���ϵ�Cl�γ���2������������2�Թ¶Ե��ӣ�
��4����ͼ��֪���ھ����ϡ����������Ϲ���4��Dԭ�ӣ���ǰ���������ĸ����Ϲ���4��Dԭ�ӣ��ھ��������Ļ���һ��Dԭ�ӡ�
��1����NH4CuSO3�н���������ΪCu+��ͭ��29��Ԫ�أ������������ԭ����̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p63d104s1��[Ar]3d104s1����ԭ��ʧȥһ������ʱ��������ͭ���ӣ�ʧȥ�ĵ������������ӣ�������ͭ���ӵĻ�̬�ĵ����Ų�ʽΪ��1S22S22P63S23P63d10��[Ar]3d10��Nԭ��2p���Ϊ������ṹ����һ�����ܴ���Oԭ�ӣ�ͬһ����Ԫ�صĵ�һ����������ԭ���������������С���������һ�����ܴ�СΪN��O��S���ʴ�Ϊ��1S22S22P63S23P63d10��[Ar]3d10��N��O��S��
��A������������ˮ����֮��������������Ĵ���ʹ���ʵ��ܽ�������������ȷ��
B������������Nԭ�Ӻ�ˮ����Oԭ�Ӿ�Ϊsp3�ӻ�����������Nԭ��ֻ��һ�Թ¶Ե��ӣ�ˮ������Oԭ�������Թ¶Ե��ӣ����ݼ۲���ӶԻ������ۿ�֪�������ӵļ��Ǵ���ˮ���ӵļ��ǣ��ʴ���
C�������������ܿ�֪���Ҵ����Ӽ�������ˮ�ļ��ԣ�[Cu(NH3)4]SO4���Ҵ����ܽ�Ƚ��ͣ���[Cu(NH3)4]SO4��Һ�м����Ҵ�����������ɫ�ľ��壬����ȷ��
D����ʾȼ���ȵ��Ȼ�ѧ����ʽ�У�����H2OΪҺ̬���ʴ���
��ѡAC���ʴ�Ϊ��AC��
��2��O3������SO2��Ϊ�ȵ����壬SO2������Sԭ�Ӽ۲���Ӷ���Ϊ3���¶Ե�����Ϊ1���ռ乹��ΪV�Σ��ȵ����������ͬ�Ŀռ乹�ͣ���O3���ӿռ乹��ΪV�Σ��ʴ�Ϊ��V�Σ�
��3��aλ���ϵ�Cl�γ���2������������2�Թ¶Ե��ӣ���Ϊsp3�ӻ����ʴ�Ϊ��sp3�ӻ���
��4�������Ͻ�Ca��D�Ͻ�����ͬ���͵ľ����ṹXYn����ͼ��֪���ھ����ϡ����������Ϲ���4��Dԭ�ӣ���ǰ���������ĸ����Ϲ���4��Dԭ�ӣ��ھ��������Ļ���һ��Dԭ�ӣ���Ca��D�ĸ�����Ϊ8��![]() ����8��
����8��![]() +1��=1��5����n=5���������Ϊ9.0��10-23cm3��LaNinH4.5�Ͻ���H������Ϊ
+1��=1��5����n=5���������Ϊ9.0��10-23cm3��LaNinH4.5�Ͻ���H������Ϊ![]() =
=![]() �����ںϽ��е��ܶ�Ϊ
�����ںϽ��е��ܶ�Ϊ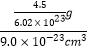 =0.083 g��cm��3���ʴ�Ϊ��0.083 g��cm��3��
=0.083 g��cm��3���ʴ�Ϊ��0.083 g��cm��3��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д� Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ����������
A. 0.1 mol��L1NaOH��Һ��Na+��K+��![]() ��
��![]()
B. 0.1 mol��L1FeCl2��Һ��K+��Mg2+��![]() ��
��![]()
C. 0.1 mol��L1K2CO3��Һ��Na+��Ba2+��Cl��OH
D. 0.1 mol��L1H2SO4��Һ��K+��![]() ��
��![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CH3CH2CH3 ��CH3CH2CH2CH3 ��CH3CH2CH2CH2CH3 ��![]()
�� ��CH3CH2CH2CH2CH2CH3
��CH3CH2CH2CH2CH2CH3
�������ʵķе㰴�ɸߵ��͵�˳�����е��ǣ� ��
A. �ޢۢܢݢڢ� B. �ޢۢڢ٢ܢ� C. �ݢܢޢۢڢ� D. �ޢݢܢۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ���������������Ҫ�ɷ�ΪFeTiO3������������MgO��SiO2�����ʣ����Ʊ��������������£�
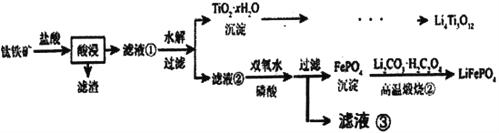
��֪���������������Ҫ��TiOCl42-��ʽ����
FeTiO3+4H++4C1-=Fe2++ TiOCl42-+2H2O
����˵������ȷ����
A. Li2Ti5O15��Ti�Ļ��ϼ�Ϊ+4��������4��������
B. ��Һ���е������ӳ���Fe2+��H+������Mg2+
C. ��Һ����Ҳ����ֱ�Ӽ���������ˮ����˫��ˮ
D. ���������բڡ������У�FeԪ�ر�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������﮵�������͵���ɫ��Դ��أ�������������������¡�
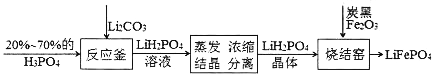
(1)��Ӧ���з�Ӧ�Ļ�ѧ����ʽΪ_______���÷�Ӧ���ֳ��ǽ����Թ�ϵ��P_____C(�>����<��)��
(2)�����£�LiH2PO4��Һ��pH��c(H2PO4-)�ı仯��ͼ1��ʾ��H3PO4��Һ��H2PO4-�ķֲ�����![]() ��pH�ı仯��ͼ2��ʾ[
��pH�ı仯��ͼ2��ʾ[![]() (��PԪ�ص�����)]��
(��PԪ�ص�����)]��
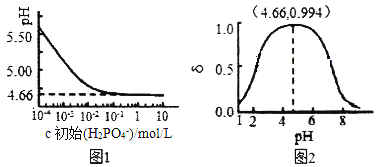
����ͼ1֪����Ũ��ʱLiH2PO4��Һ��pHС��7��������c��ʼ(H2PO4-)���������С��������Ľ���Ϊ__________________��
���ۺ���ͼ����������Ũ�ȴ���1mol/L��H3PO4��Һ�ܽ�Li2CO3��Ҫʹ��Ӧ���е�H3PO4����ȫ��ת����LiH2PO4����Ӧ������Ҫ������Һ��pH=________��
(3)������﮵���ܷ�ӦΪ��LiFePO4+6C![]() Li1-xFePO4+LixC6������еĹ������ʿɴ���Li+�����ʱ��Li+����______(���������������)���ŵ�ʱ��������ӦʽΪ__________________��
Li1-xFePO4+LixC6������еĹ������ʿɴ���Li+�����ʱ��Li+����______(���������������)���ŵ�ʱ��������ӦʽΪ__________________��
(4)������﮵�������ĺ�����ͨ�����·����ⶨ����ȡ1.60g�����������ܽ⣬����Һ�м����Թ�����SnCl2��Һ���ټ���HgCl2������Һ���ö�������������ָʾ������0.030mol/L�ظ������Һ�ζ�����Һ��dz��ɫ��Ϊ����ɫ�������ظ������Һ50.00mL��
��֪��2Fe3++Sn2++6Cl-=SnCl62-+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
��ʵ���м���HgCl2������Һ��Ŀ����____________��
�����İٷֺ���Fe(��)=_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���û�ѧ�����ʾ2Na+2H2O�T2NaOH+H2���е��������������ȷ����(����)
A. ������Ϊ8����ԭ�ӣ�88O
B. NaOH�ĵ���ʽ��![]()
C. H2O�Ľṹʽ��![]()
D. Na+�Ľṹʾ��ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����Ȼ�ѧ��Ӧ����������ȷ����
A. HCl��NaOH��Ӧ���к��ȡ�H����57.3 kJ��mol1����H2SO4��Ca(OH)2��Ӧ���к��ȡ�H=2��(��57.3)kJ��mol1
B. ����ı�ȼ���Ȧ�H����890.3 kJ��mol1����CH4(g)��2O2(g)��CO2(g)��2H2O(g) ��H����890.3 kJ��mol1
C. ��֪��500�桢30MPa�£�N2(g)��3H2(g)![]() 2NH3(g) ��H����92.4kJ��mol��1����1.5 mol H2������N2�ڴ������³�ַ�Ӧ���ų�����46.2 kJ
2NH3(g) ��H����92.4kJ��mol��1����1.5 mol H2������N2�ڴ������³�ַ�Ӧ���ų�����46.2 kJ
D. CO(g)��ȼ������283.0kJ��mol1����2CO2(g) ===2CO(g)+O2(g)��Ӧ�ġ�H��+566.0 kJ��mol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(H2C2O4)��һ�ֶ�Ԫ���ᡣ�����£���H2C2O4��Һ����μ���NaOH��Һ�������Һ��lgX[XΪc(HC2O4-)/c(H2C2O4)��c(C2O42-)/c(HC2O4-)]��pH�ı仯��ϵ��ͼ��ʾ������˵��һ����ȷ����(����)

A. ���ʾlgc(HC2O4-)/c(H2C2O4)��pH�ı仯��ϵ
B. pH��1.22����Һ�У�2c(C2O42��)+c(HC2O4��)��c(Na+)
C. 1.22��pH��4.19����Һ�У�c(HC2O4��)��c(C2O42��)��c(H2C2O4)
D. pH��4.19����Һ�У�c(Na+)��3c(HC2O4��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��Һ��c��H+����c��OH�����Ĺ�ϵ�������жϴ������

A. ����������������c��H+����c��OH������KW
B. M��������������c��H+����c��OH����
C. ͼ��T1��T2
D. XZ������������pH��7
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com