
【题目】下列化学反应的离子方程式正确的是( )
A. 氢氧化钡溶液与稀硫酸反应:Ba2++SO42﹣+H++OH﹣=BaSO4↓+H2O
B. 往碳酸镁中滴加稀盐酸:CO32﹣+2H+=CO2↑+H2O
C. 往澄清石灰水中通入过量二氧化碳:Ca2++2OH﹣+CO2=CaCO3↓+H2O
D. 用小苏打治疗胃酸过多:HCO3﹣+H+=CO2↑+H2O
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:高中化学 来源: 题型:
【题目】CO2是燃烧和代谢的最终产物,也是造成温室效应的废气,但CO2作为一种资源,开发和利用的前景十分诱人。
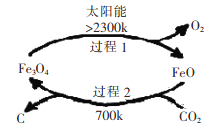
I、利用太阳能,以CO2为原料制取炭黑的流程如上图所示。过程2的化学方程式为:__________。
II、近年科学家提出“绿色自由”构想。把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应制取甲醇。其工艺流程如图所示:

(1)①由吸收池导入分解池中的主要物质的化学式是____________。
②上述流程中____________(填化学式)可循环使用,该流程体现了“绿色化学”理念。
(2)不同温度下,在1L恒容密闭容器中充入2mol CO2和5 mol H2,相同时间内测得CO2的转化率随温度变化如下图所示:

①合成塔中发生的化学反应方程式为____________。
②T1时a点v(正)____________v(逆)(填“>”,“<”,“=”)
③计算温度为T4时b的平衡常数为____________。
(3)为检验吸收池中饱和K2CO3溶液是否充足,量取l00mL吸收液用0.10 mol./L盐酸滴定,生成的V(CO2)(标准状况下)随V(盐酸)变化关系如图所示:

则该l00mL吸收液还可吸收标准状况下_______mLCO2.
III、以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能将CO2转化为低碳烯烃,工作原理如右图所示。

(1)H+的移动方向是_______________(填从左至右或从右至左);
(2)产生乙烯的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】家用天然气的主要成分是烷烃,其中甲烷(CH4)占绝大多数,已知氧气约占空气体积的20%,出现燃气泄漏时如果遇到火花会引起爆炸,当泄漏的甲烷与空气体积比为1:10时,爆炸最剧烈,此时甲烷与氧气的质量比约为
A.1:2B.2:1C.1:4D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸镧[La2(CO3)3]可用于治疗终末期肾病患者的高磷酸盐血症。制备反应原理为:LaCl3+6NH4HCO3= La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O;某化学兴趣小组利用下列装置实验室中模拟制备碳酸镧。

(1)盛放稀盐酸的仪器为__________________。
(2)制备碳酸镧实验流程中导管从左向右的连接顺序为:F→ → → → → 。_____________
(3)Y中发生反应的化学反应式为____________________________________。
(4)X中盛放的试剂是____________,其作用为___________________________。
(5)Z中应先通入NH3,后通入过量的CO2,原因为_________________________。
(6)La2(CO3)3质量分数的测定:准确称取10.0g产品试样,溶于10.0mL稀盐酸中,加入10 mL NH3-NH4Cl缓冲溶液,加入0.2 g紫脲酸铵混合指示剂,用0.5 mol·L-1 EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La 3++H2Y2-= LaY-+2H+),消耗EDTA溶液44.0 mL。则产品中La2(CO3)3的质量分数w[La2(CO3)3]=________________。
(7)该化学兴趣小组为探究La2(CO3)3和La(HCO3)3的稳定性强弱,设计了如下的实验装置,则甲试管中盛放的物质为__________;实验过程中,发现乙试管中固体质量与灼烧时间的关系曲线如图所示。在t1 min之后固体质量增加的原因可能是_______________。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
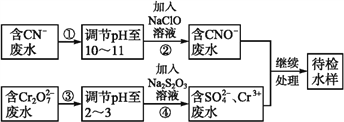
回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为_______________。
(2)步骤④的反应为S2+Cr2O72-+H+![]() SO42-+Cr3++H2O(未配平), 则每消耗0.4 molCr2O72-转移转移____mol e-。
SO42-+Cr3++H2O(未配平), 则每消耗0.4 molCr2O72-转移转移____mol e-。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是_________________。
(4)在25 ℃下,将a mol·L-1的NaCN溶液与0.01 mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示HCN的电离常数Ka=____。若25 ℃时将浓度均为0.1 mol·L-1的NaCN、HCN溶液等体积混合后,溶液呈碱性,则关于该溶液的说法不正确的是____(填字母)。
a.此溶液一定有c(Na+)+c(H+)=c(OH-)+c(CN-)
b.此溶液一定有c(Na+)=c(HCN)+c(CN-)
c.混合溶液中水的电离程度一定大于该温度下纯水的电离程度
d.此溶液加入少量氢氧化钠或盐酸,溶液的pH变化不大
(5)除去废水中的阳离子:取水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入一定量的Na2S溶液,蓝色沉淀转化成黑色沉淀。该过程中反应的离子方程式为_______、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是( )
A.油脂水解的产物中含甘油
B.淀粉与纤维素互为同分异构体
C.蛋白质可水解生成多肽和氨基酸
D.医疗上用75%的酒精消毒是因为其能使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T K时,向2.0L恒容密闭容器中充入0.10molCOCl2,发生反应![]() ,经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是
,经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表,下列说法正确的是

A. T K时该反应的化学平衡常数为![]()
B. 反应在前2s的平均速率![]() mol·L-1·s-1
mol·L-1·s-1
C. 保持其他条件不变,升高温度,若新平衡时c(C12)=0.038mol·L-1,则反应的△H<0
D. 平衡后向上述容器中再充入0.10molCOCl2,平衡正向移动,COCl2的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于可逆反应的是( )
A.Pb+PbO2+4H++2SO42﹣ ![]() 2PbSO4+2H2O
2PbSO4+2H2O
B.2SO2+O2 ![]() 2SO3
2SO3
C.Cl2+H2O?HCl+HClO
D.2NO2?N2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去). 
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出E中含有的化学键类型;已知1molA与水反应放出283.5kJ的热量,试写出A与水反应的热化学反应方程式;
(2)若A 为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则单质A与H2O反应的离子方程式 .
(3)若A 为淡黄色粉末,回答下列问题: ①1molA与足量的H2O充分反应时,转移电子总数为
②若X为非金属单质,通常为黑色粉末,写出D的结构式
(4)若A为氧化物,X是Fe,溶液D加入KSCN溶液变红. ①A与H2O反应的离子方程式
②请用离子方程式表示D盐的净水原理 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com