
����Ŀ��A(C3H6)�ǻ����л�����ԭ�ϣ���A�Ʊ��ۺ���C�� �ϳ�·����ͼ��ʾ������������ȥ����
�ϳ�·����ͼ��ʾ������������ȥ����

��֪�� ��
��![]() R-COOH
R-COOH
(1)A��������_____________��B���������������________________��
(2)C�Ľṹ��ʽ________________��D��E�ķ�Ӧ����Ϊ________________
(3)E��F�Ļ�ѧ����ʽΪ___________________________��
(4)B��ͬ���칹���У���B������ͬ���������ܷ���������Ӧ�����к˴Ź�����������ʾ3��壬�ҷ����֮��Ϊ6:1:1����__________________��д���ṹ��ʽ����
(5)�����ʵ����� �ֱ�������NaOH��NaHCO3 ��Ӧ������NaOH��NaHCO3 �����ʵ���֮��Ϊ__________������
�ֱ�������NaOH��NaHCO3 ��Ӧ������NaOH��NaHCO3 �����ʵ���֮��Ϊ__________������ ����һ�ֹ����ŵķ�����______________��д�����������ơ���Ӧ�Լ�������
����һ�ֹ����ŵķ�����______________��д�����������ơ���Ӧ�Լ�������
���𰸡���ϩ ����  ȡ����Ӧ CH2=CH-CH2OH+CH2=CH-CCl=CH2
ȡ����Ӧ CH2=CH-CH2OH+CH2=CH-CCl=CH2![]()
![]() HCOO-CH=C(CH3)2 l��l �����Ȼ���ȡ�������л������������ɫʯ����Һ���(�����̼̼˫����������ˮ����ˮ��ɫ)
HCOO-CH=C(CH3)2 l��l �����Ȼ���ȡ�������л������������ɫʯ����Һ���(�����̼̼˫����������ˮ����ˮ��ɫ)
��������
A����ʽΪC3H6��A��CO��CH3OH������Ӧ����B����A�ṹ��ʽΪCH2=CHCH3��B�ṹ��ʽΪCH3CH=CHCOOCH3��B�����Ӿ۷�Ӧ���ɾ۶�ϩ��������۶�ϩ���������ˮ�ⷴӦ��Ȼ���ữ�õ��ۺ���C��C�ṹ��ʽΪ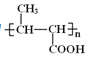 ��A��Cl2�ڸ����·�����Ӧ����D��D����ˮ�ⷴӦ����E������E�Ľṹ��ʽCH2=CHCH2OH��֪D�ṹ��ʽΪCH2=CHCH2Cl��E��2-��-1��3-����ϩ�����ӳɷ�Ӧ����F��F�ṹ��ʽΪ
��A��Cl2�ڸ����·�����Ӧ����D��D����ˮ�ⷴӦ����E������E�Ľṹ��ʽCH2=CHCH2OH��֪D�ṹ��ʽΪCH2=CHCH2Cl��E��2-��-1��3-����ϩ�����ӳɷ�Ӧ����F��F�ṹ��ʽΪ![]() ��F����ȡ����Ӧ����G��G������Ϣ�з�Ӧ�õ�����G�ṹ��ʽΪ
��F����ȡ����Ӧ����G��G������Ϣ�з�Ӧ�õ�����G�ṹ��ʽΪ![]() ��
��
���������ƶϿ�֪A��CH2=CH-CH3��CΪ ��D��CH2=CHCH2Cl��EΪCH2=CHCH2OH��F��
��D��CH2=CHCH2Cl��EΪCH2=CHCH2OH��F��![]() ��G��
��G��![]() ��
��
(1)A��CH2=CH-CH3������Ϊ��ϩ��B�ṹ��ʽΪCH3CH=CHCOOCH3��B�к���������������������
(2)C�Ľṹ��ʽΪ ��D��CH2=CHCH2Cl������Clԭ�ӣ���NaOH��ˮ��Һ���ȷ���ˮ�ⷴӦ����E��CH2=CHCH2OH����ˮ�ⷴӦҲ��ȡ����Ӧ�����D��ΪE�ķ�ӦΪȡ����Ӧ��ˮ�ⷴӦ��
��D��CH2=CHCH2Cl������Clԭ�ӣ���NaOH��ˮ��Һ���ȷ���ˮ�ⷴӦ����E��CH2=CHCH2OH����ˮ�ⷴӦҲ��ȡ����Ӧ�����D��ΪE�ķ�ӦΪȡ����Ӧ��ˮ�ⷴӦ��
(3)EΪCH2=CHCH2OH��E��2-��-1��3-����ϩ�����ӳɷ�Ӧ����F��F�ṹ��ʽΪ![]() ���÷�Ӧ����ʽΪ��CH2=CH-CH2OH+CH2=CH-CCl=CH2
���÷�Ӧ����ʽΪ��CH2=CH-CH2OH+CH2=CH-CCl=CH2![]()
![]() ��
��
(4)B�ṹ��ʽΪCH3CH=CHCOOCH3��B��ͬ���칹���У���B������ͬ���������ܷ���������Ӧ��˵������ȩ����������̼̼˫������Ϊ�����γɵ��������к˴Ź�����������ʾ3��壬�ҷ����֮��Ϊ6:1:1����HCOO-CH=C(CH3)2��
(5) �����Ȼ���������NaOH��Ӧ����
�����Ȼ���������NaOH��Ӧ���� �������Ȼ�������NaHCO3��Ӧ����
�������Ȼ�������NaHCO3��Ӧ���� ��H2O��CO2��������ʵ���
��H2O��CO2��������ʵ��� ����NaOH��NaHCO3�����ʵ���֮��Ϊ1��1����
����NaOH��NaHCO3�����ʵ���֮��Ϊ1��1���� �к����Ȼ���̼̼˫�������ǻ����ֹ����ţ������Ȼ��ķ����ǣ�ȡ�������л������������ɫʯ����Һ��Ϊ��ɫ������̼̼˫���ķ����ǣ�������ˮ����ˮ��ɫ��
�к����Ȼ���̼̼˫�������ǻ����ֹ����ţ������Ȼ��ķ����ǣ�ȡ�������л������������ɫʯ����Һ��Ϊ��ɫ������̼̼˫���ķ����ǣ�������ˮ����ˮ��ɫ��


 ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д� Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����һ�������������½���ˮ�е�����CO(NH2)2ת��Ϊ�����Ѻ����ʣ�ʵ�ֻ�ѧ��ת��Ϊ���ܵ�װ�ã������üס�����װ��ʵ�������϶�ͭ������˵���в���ȷ����

A. ��װ������Һ��ɫ����
B. ͭ�缫Ӧ��Y������
C. M�缫��Ӧʽ��CO(NH2)2+H2O-6e-=CO2��+N2��+6H��
D. ��N�缫����0.25 mol����ʱ��ͭ�缫��������16g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ����Ҫ�Ļ���ԭ�ϣ������Ʊ�һϵ�����ʣ���ͼ��ʾ��������˵���������
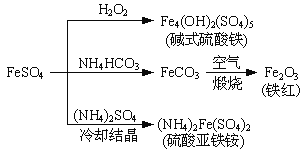
A. ��ʽ������ˮ���ܲ���Fe(OH)3���壬��������ˮ��
B. Ϊ��ֹNH4HCO3�ֽ⣬����FeCO3���ڽϵ��¶��½���
C. ����KSCN��Һ����(NH4)2Fe(SO4)2�Ƿ�����
D. �����£�(NH4)2Fe(SO4)2��ˮ�е��ܽ�ȱ�FeSO4�Ĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����98%��Ũ����(�ܶ�Ϊ1.84g/cm3)����l00mL 1mol/L��ϡ���ᣬ��窳���������(���ƹ����п����õ�):��100mL��Ͳ��10mL��Ͳ��50mL�ձ� ��������ƽ��100mL����ƿ����ͷ�ι�����������������ʹ���������Ⱥ����������ȷ����
A. �ܢۢߢݢ� B. �ڢݢߢ� C. �٢ۢݢޢ� D. �ڢޢۢߢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӣ�Ni-Cd���ɳ�������ִ��������й㷺Ӧ�ã����ij䡢�ŵ練Ӧ����ʽ���У�Cd(OH)2+2Ni(OH)2![]() Cd+2NiOOH+2H2O���й������ص�˵����ȷ���ǣ� ��
Cd+2NiOOH+2H2O���й������ص�˵����ȷ���ǣ� ��
A.ԭ���ʱ��������Ӧ�ǣ�Cd(OH)2+2e-=Cd+OH-
B.ԭ���ʱ�ĸ�����Ӧ�ǣ�Cd-2e-+2OH-=Cd(OH)2
C.�ŵ�ʱ������������Һ�ļ��Բ���
D.�ŵ�ʱ�������Һ�е�OH-�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ֽƬb���䵽a�У��ɵõ�һ�����������ӷ���ʽ(δ��ƽ)������˵����ȷ����(�� ��)

A. ��Ӧ������S��SO![]() ��OH��
��OH��
B. �÷�Ӧ���������������½���
C. �������뻹ԭ�������ʵ���֮��Ϊ2��1
D. 2 mol S�μӷ�Ӧʱ��ת�Ƶĵ�����Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�ʴ��Һ(��![]() ��
��![]() )�Ʊ�����ʴ��Һ��
)�Ʊ�����ʴ��Һ��![]() ��Һ�ݺ�
��Һ�ݺ�![]() ����Ҫ���裺��
����Ҫ���裺��![]() ������ʴ�̿�Һ���Ʊ��������Ʊ�����ʴ��Һ[
������ʴ�̿�Һ���Ʊ��������Ʊ�����ʴ��Һ[![]() �ݣ���Һ���룬�������ܽ�������Ʊ�
�ݣ���Һ���룬�������ܽ�������Ʊ�![]() ������ʵ��װ�úͲ������ܴﵽʵ��Ŀ�ĵ���
������ʵ��װ�úͲ������ܴﵽʵ��Ŀ�ĵ���
A.  �Ʊ�
�Ʊ�![]()
B.  �Ʊ�
�Ʊ�![]() ���õ�
���õ�![]()
C.  ����
����![]() ��Һ��
��Һ��![]()
D.  ��
��![]() ��Һ�����Ʊ�
��Һ�����Ʊ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��ɽ���ǽ�ɽ��ɽ�����о�NO2��NO��CO��NO2�ȴ�����Ⱦ���ˮ��Ⱦ��Ĵ����Խ��������й�������Ҫ���塣
��1����֪����NO2(g) + CO(g)![]() CO2(g) + NO(g)��H��-234 kJ/mol�÷�Ӧ��ƽ�ⳣ��ΪK1����ͬ��
CO2(g) + NO(g)��H��-234 kJ/mol�÷�Ӧ��ƽ�ⳣ��ΪK1����ͬ��
��N2(g)+O2(g) ![]() 2NO(g) ��H��+179.5 kJ/mol K2
2NO(g) ��H��+179.5 kJ/mol K2
��2NO(g) +O2(g)![]() 2NO2(g) ��H��-112.3 kJ/mol K3
2NO2(g) ��H��-112.3 kJ/mol K3
��д��NO��CO��Ӧ��������Ⱦ��������Ȼ�ѧ����ʽ____________________��
�Լ����Ȼ�ѧ����ʽ��ƽ�ⳣ��K=________����K1��K2��K3��ʾ����
��2����һ�������£���λʱ���ڲ�ͬ�¶��²ⶨ�ĵ�������ת������ͼ1��ʾ���¶ȸ���710Kʱ�����¶ȵ����ߵ�������ת���ʽ��͵�ԭ�������________��
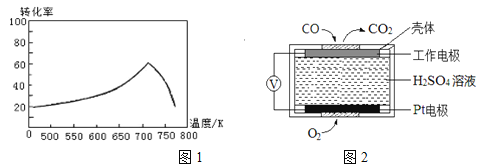
����֪���ⶨ������NO��CO�������õķ��������֣�
����1���绯ѧ������������������CO�������Ĺ���ԭ����ͼ2��ʾ�������缫�ķ�ӦʽΪ____��
����2��������ԭ�ζ�������H2O2��Һ����β��������������ת��Ϊǿ�ᣬ������к͵ζ����ⶨǿ��Ũ�ȡ�д��NO��H2O2��Һ��Ӧ�����ӷ���ʽ��________________��
��3��NO2����Ⱦ����������Na2CO3��Һ����NO2 ������CO2����֪9.2gNO2�����Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol��ǡ�÷�Ӧ��ʹ����Һ�е�CO2��ȫ�ݳ��������ܱ��������ԣ�����Һ�д��ڵ���������Ũ�ȴ�С��ϵ��____________________________��
��4�������ѵ����ɾ�����Ũ��NO������������������ͣ��ʱ���Ϊ90s������£���ò�ͬ������NO���ѵ�����ͼI������ʾ��
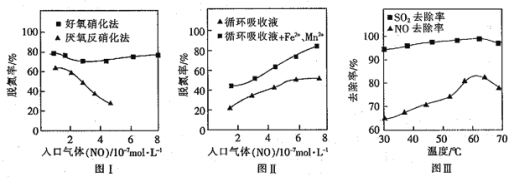
����ͼI֪���������е�NO��������ʱ����ѡ��___________������ѵ���Ч�ʡ�
��ͼ���У�ѭ������Һ����Fe2+��Mn2+��������ѵ���Ч�ʣ������ԭ��Ϊ___________��
��5���о�������NaClO/H2O2���Ը������ռ���ͬʱ��Ч����������ͼ����ʾΪ�������ռ����һ��ʱ���¶ȶ�����������Ӱ�졣�¶ȸ���60����NOȥ�����½���ԭ��Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ﻷ��������(H)��һ��Ӧ�ù㷺���л���ϳɻ�����H��·����ͼ��
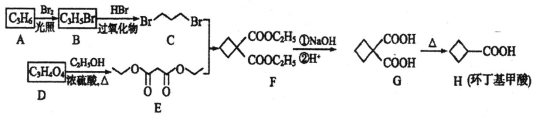
(1)A����ϩ������ṹ��ʽΪ______________����A��B�ķ�Ӧ������___________��
(2)D�й����ŵ�������_________________����D��E�ķ�Ӧ������________________��
(3)E��������_______________��
(4)д��F��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ_______________________��
(5)M��G��ͬ���칹�壬��������������������ʹ������Ȼ�̼��Һ��ɫ����1mol M����������NaHCO3��Ӧ����88g���壻�ۺ˴Ź�������Ϊ2��壻��M�Ľṹ��ʽΪ(�����������칹��ֻдһ��)________________��N�DZ�M��һ��̼ԭ�ӵ�ͬϵ���N��ͬ���칹����_________�֡�
(6)���������ϳ�·�ߣ���![]() �ͻ�����EΪԭ��(���Լ���ѡ)������Ʊ�
�ͻ�����EΪԭ��(���Լ���ѡ)������Ʊ�![]() �ĺϳ�·��________________________________��
�ĺϳ�·��________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com