
【题目】甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中的两种组成.常温下,甲是一种含氮质量分数为87.5%的液态化合物,其相对分子质量与空气中某种主要成分的相对分子质量相等;乙和丙是铜的两种常见氧化物,乙是新制氢氧化铜与乙醛反应的还原产物.试回答下列问题:
(1)甲的结构式 .
(2)甲是一种二元弱碱,则甲与过量硫酸反应的产物为(写化学式).16g甲在空气中充分燃烧,生成一种常见液态物质和氮气,放出311kJ热量,则其热化学方程式为 .
(3)甲和丙反应的产物中含有乙和一种气态单质,写出其化学方程式 .
(4)向乙的固体中加入过量硫酸酸化的硫酸铁溶液,乙固体完全溶解,得到透明溶液.
①写出其离子方程式 .
②若所得溶液中阳离子浓度均约为0.1mol/L,再向所得混合溶液中加丙,最先得到沉淀(不同浓度的阳离子开始和完全以氢氧化物沉淀的pH如图).
③向上述混合液中加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相)R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶.请设计实验方案,验证有机相中含有铜元素 . 
【答案】
(1)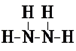
(2)N2H6SO4;N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣622kJ/mol
(3)N2H4+4CuO=2Cu2O+N2↑+2H2O
(4)Cu2O+2Fe3++2H+=2Cu2++2Fe2++H2O;Fe(OH)3;取有机层,加入盐酸或稀硫酸,振荡后水层呈蓝色,则证明有机相中含有铜元素
【解析】解:甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中两种元素组成.常温下,甲是一种含氮质量分数为87.5%的液态化合物,相对分子质量与空气中某种主要成份的相对分子质量相同,而空气的主要成分为氧气和氮气,如为氮气,则相对分子质量为28,没有符合物质,如为氧气,则相对分子质量为32,则该化合物含N的质量为32×87.5%=28,则甲含有N、H两种元素,分子式为N2H4 , 乙和丙是铜的两种常见氧化物,乙是新制的氢氧化铜与乙醛反应的还原产物,则乙为Cu2O,丙为CuO.(1)甲为N2H4 , 结构式为 ![]() ,所以答案是:
,所以答案是: ![]() ;(2)肼是一种二元碱,则可以与2个H+结合,N2H4与硫酸反应的方程式为:N2H4+H2SO4=N2H6SO4 , 则产物为N2H6SO4 , n(N2H4)=
;(2)肼是一种二元碱,则可以与2个H+结合,N2H4与硫酸反应的方程式为:N2H4+H2SO4=N2H6SO4 , 则产物为N2H6SO4 , n(N2H4)= ![]() =0.5mol,燃烧时生成一种常见液态物质和氮气,液态物质为生成水,放出311kJ热量,则热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣622kJ/mol,所以答案是:N2H6SO4;N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣622kJ/mol;(3)甲和丙反应的产物中含有乙和一种气态单质,该气体单质为氮气,反应的方程式为:N2H4+4CuO=2Cu2O+N2↑+2H2O,所以答案是:N2H4+4CuO=2Cu2O+N2↑+2H2O;(4)向Cu2O固体中加入过量硫酸酸化的硫酸铁溶液,Cu2O固体完全溶解,得到透明溶液,应生成硫酸铜和硫酸亚铁,①反应的离子方程式为:Cu2O+2Fe3++2H+=2Cu2++2Fe2++H2O,所以答案是:Cu2O+2Fe3++2H+=2Cu2++2Fe2++H2O;
=0.5mol,燃烧时生成一种常见液态物质和氮气,液态物质为生成水,放出311kJ热量,则热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣622kJ/mol,所以答案是:N2H6SO4;N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣622kJ/mol;(3)甲和丙反应的产物中含有乙和一种气态单质,该气体单质为氮气,反应的方程式为:N2H4+4CuO=2Cu2O+N2↑+2H2O,所以答案是:N2H4+4CuO=2Cu2O+N2↑+2H2O;(4)向Cu2O固体中加入过量硫酸酸化的硫酸铁溶液,Cu2O固体完全溶解,得到透明溶液,应生成硫酸铜和硫酸亚铁,①反应的离子方程式为:Cu2O+2Fe3++2H+=2Cu2++2Fe2++H2O,所以答案是:Cu2O+2Fe3++2H+=2Cu2++2Fe2++H2O;
②反应后硫酸铁过量,由图象可知Fe3+完全沉淀时所需pH较小,则加入CuO消耗氢离子时,溶液pH不断增大,首先析出的沉淀是Fe(OH)3 , 所以答案是:Fe(OH)3;
③由可逆反应2RH(有机相)+Cu2+(水相)R2Cu(有机相)+2H+(水相)可知,可在有机相中加入盐酸或稀硫酸,则平衡向逆向移动,如溶液变成蓝色,可说明有机相中含有Cu2+ , 所以答案是:取有机层,加入盐酸或稀硫酸,振荡后水层呈蓝色,则证明有机相中含有铜元素.


科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸中,合金完全溶解,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3mol/L的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述正确的是( )
A.反应中转移电子的总数为0.3mol
B.反应过程中,消耗硝酸的物质的量为0.3mol
C.沉淀完全时消耗NaOH溶液的体积为100mL
D.开始加入合金的质量可能为3.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铜电极的叙述正确的是
A.铜锌原电池中铜是负极B.用电解法精炼粗铜时粗铜作阴极
C.在镀件上电镀铜时可用铜作阳极D.电解食盐水时铜作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影晌生成H2的总置,可向盐酸中加入的物质是
A.CH3COONa固体 B.NaOH溶液C.(NH4)2SO4粉末D.K2SO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1为实验室制备、收集少量HCl的装置.
①制备HCl所用药品为浓硫酸和浓盐酸,则甲的最佳装置应选用图2中的 . 
②请解释能用浓硫酸和浓盐酸制备HCl气体的原因 .
③装置丙用来吸收过量的HCl气体,为防止倒吸,则烧杯中应该装入水和 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和生活中有着重要的应用,下列说法正确的是( )
A.“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物有关
B.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料
C.白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
D.能够改善食品的色、香、味,并有防腐、保鲜作用的食品添加剂,须限量使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是
![]()
A. 最简单气态氢化物的热稳定性:R>Q
B. 最高价氧化物对应水化物的酸性:Q<W
C. 原子半径:T>Q>R
D. 含T的盐溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应 4(NH4)2SO4===N2↑+ 6NH3↑+ 3SO2↑+ SO3↑+ 7H2O 的产物气体通入BaCl2溶液,下列判断正确的是
A. 无沉淀生成 B. 肯定没有BaSO3生成
C. 得到的沉淀是纯净物 D. 得到的沉淀是BaSO4和BaSO3组成的混合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com