
【题目】酸性重铬酸盐溶液中加入乙醚和H2O2发生反应![]() +4H2O2+2H+=2CrO(O2)2+5H2O。上层出现蓝色,一段时间后上层蓝色逐渐褪去且水相变为绿色(Cr3+)。下列说法错误的是( )
+4H2O2+2H+=2CrO(O2)2+5H2O。上层出现蓝色,一段时间后上层蓝色逐渐褪去且水相变为绿色(Cr3+)。下列说法错误的是( )
A.溶液出现蓝色的反应属于非氧化还原反应
B.乙醚可用乙醇代替
C.该方法既可用于检验H2O2,又可用于检验![]()
D.水层逐渐变为绿色发生的离子反应为4CrO(O2)2+ 12H+=4Cr3++ 6H2O+7O2↑
【答案】B
【解析】
乙醚密度比水小,微溶于水,遇水出现分层,![]() 和H2O2反应生成CrO(O2)2,CrO(O2)2溶于乙醚出现蓝色;水相变为绿色,说明CrO(O2)2和下层水溶液反应生成了Cr3+,据此解答。
和H2O2反应生成CrO(O2)2,CrO(O2)2溶于乙醚出现蓝色;水相变为绿色,说明CrO(O2)2和下层水溶液反应生成了Cr3+,据此解答。
A.溶液出现蓝色的反应为![]() +4H2O2+2H+=2CrO(O2)2+5H2O,反应前后各元素化合价均没有变化,为非氧化还原反应,A正确;
+4H2O2+2H+=2CrO(O2)2+5H2O,反应前后各元素化合价均没有变化,为非氧化还原反应,A正确;
B.乙醇与水互溶且乙醇能被酸性重铬酸根离子氧化,不能用乙醇代替乙醚,B错误;
C.该反应有特征蓝色现象出现,故既可用于检验H2O2,又可用于检验![]() ,C正确;
,C正确;
D.根据现象可知,在水层中,CrO(O2)2中+6铬表现氧化性被还原成绿色的Cr3+,则过氧根表现还原性,由此可知:水层逐渐变为绿色发生的离子反应为4CrO(O2)2+ 12H+=4Cr3++ 6H2O+7O2↑,D正确;
答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关事实及原因的分析中,错误的是![]()
![]()
事实 | 原因 | |
A. | 分子内不同化学键之间存在键角 | 共价键具有方向性 |
B. |
|
|
C. | 不含金属元素的化合物均是共价化合物 | 非金属元素间不能形成离子键 |
D. |
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A.向AgNO3中滴加氨水至过量:Ag++NH3H2O=AgOH↓+![]()
B.向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2=I2+2H2O
C.向Na2S2O3溶液中加入足量稀硫酸:2![]() +4H+=
+4H+=![]() +3S↓+2H2O
+3S↓+2H2O
D.向苯酚钠溶液中通入少量CO2气体:2![]() +CO2+H2O→2
+CO2+H2O→2![]() +
+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水中含有砷会导致砷中毒,金属冶炼过程产生的含砷有毒废弃物需处理与检测。冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:

已知:①As2S3与过量的S2-存在反应:As2S3(s)+3S2-(aq)2![]() (aq);
(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)砷在元素周期表中的位置为_______;AsH3的电子式为______;
(2)下列说法正确的是_________;
a.酸性:H2SO4>H3PO4>H3AsO4
b.原子半径:S>P>As
c.第一电离能:S<P<As
(3)沉淀X为__________(填化学式);
(4)“一级沉砷”中FeSO4的作用是________。
(5)“二级沉砷”中H2O2与含砷物质反应的化学方程式为__________;
(6)关于地下水中砷的来源有多种假设,其中一种认为富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成![]() ,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为______________。
,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图有机物的正确命名为 ( )

A.2-乙基-3,3-二甲基戊烷B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基己烷D.3,4,4-三甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的电子气体有BCl3、N2O、SiH4及SiHCl3等。回答下列问题:
(1)气体B2H6与氯气混合可生成气态BCl3,每生成1.0 g BCl3放出5.9 kJ的热量,该反应的热化学方程式为______。
(2)25℃时反应 S(s) +H2(g)H2S(g) Kp1=6.0×105
Si(s)+2H2(g)SiH4(g) Kp2=7.8×106
则反应 Si(s)+2H2S(g)SiH4(g)+2S(s) Kp=_____(Kp为以分压表示的平衡常数,下同)。
(3)多晶硅制中发生一系列反应:
(I)4SiHCl3(g)Si(s)+3SiCl4(g)+2H2(g) △H1=a kJ /mol
(II)SiCl4(g)+H2(g)SiHCl3(g)+HCl(g) △H2=b kJ/mo1
(III)SiCl2(g)+H2(g)Si(s)+2HCl(g) △H3=c kJ/mo1
①反应SiHCl3 (g)SiCl2 (g) +HCl (g) △H=____kJ/mo1 (用含a、b、c的代数式表示)
②反应(I)(II)(III)的Kp与温度的关系如下图

属于吸热反应的是_________(填I、II或III);图中M点分压间满足关系:p(SiCl4)=______(用相关物质的分压p表示)。
(4)一种制取N2O的方法为 O2NNH2(aq)→N2O(g)+H2O(1),该反应的历程如下:
(I)O2NNH2(aq)![]() O2NNH-(aq) +H+(aq) (快速平衡)
O2NNH-(aq) +H+(aq) (快速平衡)
(II)O2NNH-(aq)![]() N2O(g) +OH-(aq) (慢)
N2O(g) +OH-(aq) (慢)
(III)H+(aq)+OH-(aq)![]() H2O(1) (快)
H2O(1) (快)
①活化能最大的反应步骤是_________(填I、II或III)。
②已知反应(I)的速率方程v(正)=k1c(O2NNH2),v(逆)=k -1 c(O2NNH-)c(H+),(k1、k -1分别为正逆反应速率常数,反应(I)达到平衡时,平衡常数K=__________(用k1、k -1表示)。
③已知总反应速率方程为v=K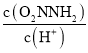 ,反应(II)的v(正)=k2c(O2NNH-),则K=________ (用k1、k -1、k2、k3表示)
,反应(II)的v(正)=k2c(O2NNH-),则K=________ (用k1、k -1、k2、k3表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丙叉环丙烷(n)由于其特殊的结构,一直受到结构和理论化学家的关注,它有如下转化关系。下列说法正确的是
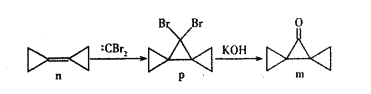
A. n分子中所有原子都在同一个平面上
B. n和:CBr2生成p的反应属于加成反应
C. p分子中极性键和非极性键数目之比为2:9
D. m分子同分异构体中属于芳香族化合物的共有四种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L容积不变的容器中,发生N2+3H2 ![]() 2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是
2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是
A. 1.6 mol B. 2.8 mol
C. 3.2 mol D. 3.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)、碲(Te)的单质和化合物在化工生产等方面具有重要应用。
(1)下列关于硒、碲及其化合物的叙述不正确的是_______。
A.Te 位于周期表的第五周期 Ⅵ A 族
B.Se 的氧化物通常有SeO2和SeO3
C.H2TeO4的酸性比H2SO4的酸性强
D.热稳定性H2Se比H2S弱,但比HBr强
(2)25℃ 时,硒酸的电离H2SeO4=H+ +![]() ;
;![]() H+ +
H+ +![]() Ka2 = 1×10-3,则0.1 mol·L-1NaHSeO4溶液的pH约为________;NaHSeO4溶液中的物料守恒表达式为____________。
Ka2 = 1×10-3,则0.1 mol·L-1NaHSeO4溶液的pH约为________;NaHSeO4溶液中的物料守恒表达式为____________。
(3)TeO2微溶于水,易溶于较浓的强酸和强碱。工业上常用铜阳极泥(主要含TeO2,还含有少量Ag、Au)为原料制备单质碲,其工艺流程如图:
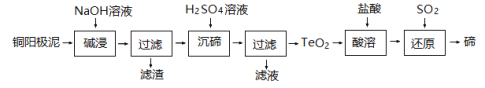
①铜阳极泥在碱浸前需烘干、研成粉末,目的是____________;
②“碱浸”时TeO2发生反应的化学方程式为_____________;
③“沉碲”时控制溶液的 pH 为 4.5~5.0,生成TeO2沉淀,酸性不能过强的原因是__________;
④“还原”得到固态碲为粗碲,对粗碲进行洗涤,判断洗涤干净的实验操作和现象是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com