
【题目】在一定条件下,乙烷和乙烯都能制备氯乙烷(C2H5Cl)。试回答:
(1)上述两种制备氯乙烷的方法中,__________________________________方法好。原因是________。
(2)请写出好的制备氯乙烷(C2H5Cl)的化学方程式______________________________;该反应的类型是______。
【答案】
(1)用乙烯制备氯乙烷; 乙烷与氯气的取代反应,副反应较多,而乙烯与氯化氢的加成反应的产物是唯一的,无副产物.
(2) CH2=CH2+HCl![]() CH3CH2Cl ,加成反应
CH3CH2Cl ,加成反应
【解析】
试题分析:(1)由乙烷与氯气在光照条件下发生反应得到的产物有:一氯乙烷,1,1﹣二氯乙烷,1,2﹣二氯乙烷,1,1,2﹣三氯乙烷,1,1,2,2﹣四氯乙烷,1,1,1,2﹣四氯乙烷,1,1,1,2,2﹣五氯乙烷,六氯乙烷和氯化氢,产物不唯一,而乙烯和卤化氢能发生加成反应得到氯乙烷,产物只有一种,
故答案为:用乙烯制备氯乙烷; 乙烷与氯气的取代反应,副反应较多,而乙烯与氯化氢的加成反应的产物是唯一的,无副产物.
(2)因烯烃与卤化氢能发生加成反应得到卤代烃,所以用乙烯制备氯乙烷的化学方程式是:CH2=CH2+HCl![]() CH3CH2Cl ,该反应的类型是加成反应.
CH3CH2Cl ,该反应的类型是加成反应.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】Cu2S 可用于制防污涂料,其可由热的铜在硫蒸气或H2S 中反应制得。
(1)铜元素在元素周期表中的位置为 ____________,Cu+的核外电子排布式为_________,基态铜原子核外电子共有__________种运动状态。
(2)Cu2S在一定条件下可被氧化为CuSO4。
①在SO42—中S原子的杂化轨道类型为________;SiO44—、PO43—与 SO42—互为________;其中Si、P、S第一电离能由大到小顺序为________________ ;
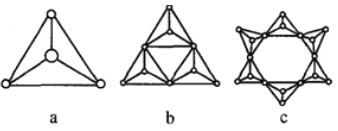
②硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元,硅氧四面体可以用图a 表示,图中b、c 是硅氧四面体结合成环状结构的两个例子,若在环状结构中硅的原子数为n,写出环状结构中硅酸根离子的通式_______________。
(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH),二者部分物理性质如下:
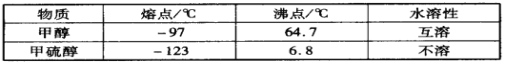
甲醇和甲硫醇在熔沸点和水溶性方面性质差异的原因是__________________________。
(4)某化合物由S、Fe、Cu 三种元素组成,其晶胞结构如下图所示(1 pm=10-10cm),该晶胞上下底面为正方形,侧面与底面垂直,则该晶体的密度ρ=_________g/cm3(保留三位有效数字)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图填空。
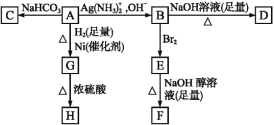
已知H是环状化合物C4H6O2,F的碳原子都在一条直线上。
(1)化合物A含有的官能团是 。
(2)B在酸性条件下与Br2反应得到E,E在足量的氢氧化钠醇溶液作用下转变成F,由E转变成F时发生两种反应,其反应类型分别是 。
(3)D的结构简式是 。
(4)1 mol A与2 mol H2反应生成1 mol G,其反应方程式是 。
(5)与A具有相同官能团的A的同分异构体的结构简式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝硅合金材料性能优良。铝土矿(含 30% SiO2、40.8% Al2O3和少量Fe2O3等)干法制取该合金的工艺如下:
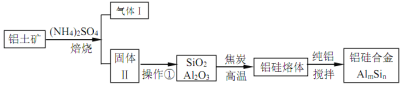
(1)铝硅合金材料中若含铁,会影响其抗腐蚀性。原因是______________。
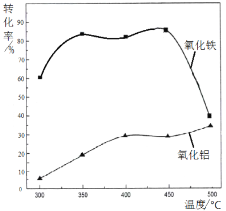
(2)焙烧除铁反应时 Fe2O3 转化为NH4Fe(SO4)2,Al2O3少部分发生类似反应。写出 Fe2O3发生反应的方程式:______________。 氧化物转化为硫酸盐的百分率与温度的关系如图,最适宜焙烧温度为______________。
(3)若操作①中所得溶液中加入过量NaOH 溶液,含铝微粒发生反应的离子方程式为:______________。
(4)用焦炭还原SiO2、Al2O3会产生SiC等中间体。写出中间体 SiC 再与Al2O3反应生成铝、硅单质的化学方程式并表出电子转移的方向和数目:______________ 。
(5)已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38。向 FeCl3和 AlCl3的混合溶液中逐滴加入NaOH 溶液,生成 Al(OH)3和Fe(OH)3沉淀,当两种沉淀共存时,上层溶液中 c(Al3+):c(Fe3+)=__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分解而变成乳酸,乳酸的结构简式为![]() 。已知有机物中若含有相同的官能团,则化学性质相似。完成下列问题:
。已知有机物中若含有相同的官能团,则化学性质相似。完成下列问题:
(1)写出乳酸分子中官能团的名称 。
(2)一定条件下乳酸能发生的反应类型有______________ (填序号)。
A.水解反应
B.取代反应
C.加成反应
D.中和反应
E.氧化反应
F.酯化反应
(3)写出过量乳酸与碳酸钠溶液反应的化学方程式 。
(4)乳酸在浓硫酸作用下,两分子相互反应生成链状结构的物质,写出此有机生成物的结构简式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物
(1)工业上尿素由CO2和NH3合成,写出其方程式 ___________________________.
(2)当氨碳比![]() 时,CO2的转化率随时间的变化关系如图所示。
时,CO2的转化率随时间的变化关系如图所示。

①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”)。
②NH3的平衡转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
(1) Y在元素周期表中的位置为_____________________________.
(2) 上述元素的最高价氧化物对应的水化物酸性最强的是_____________________ (写化学式),非金属气态氢化物还原性最强的是_______________(写化学式)。
(3) Y、G的单质或两元素之间形成的化合物可作水消毒剂的有__________________ (写出其中两种物质的化学式))。
(4) ZX的电子式为_________________;ZX与水反应放出气体的化学方程式为__________________。
(5) 熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),放电时,电池的正极反应 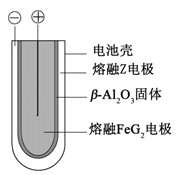
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。电解质溶液为KOH溶液,电池反应为:Cd +2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2,下列有关镍镉电池的说法正确的是
Cd(OH)2+2Ni(OH)2,下列有关镍镉电池的说法正确的是
A. 充电过程是化学能转化为电能的过程
B. 充电时阳极反应为Cd(OH)2+2e—="=" Cd + 2OH-
C. 放电时电池内部OH - 向正极移动
D. 充电时与直流电源正极相连的电极上发生Ni(OH)2转化为NiO(OH)的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
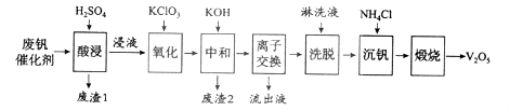
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com