
 ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
| A、CxHy |
| B、CxHy -x |
| C、CxH2y-2x |
| D、CxHy-2x |
查看答案和解析>>
科目:高中化学 来源: 题型:
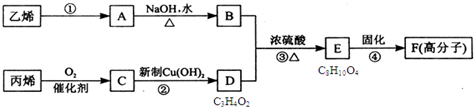
| A、反应④的反应类型是加聚 |
| B、物质A是卤代烃 |
| C、物质B催化氧化后可以得到乙醛 |
| D、1mol物质E最多可以消耗2molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
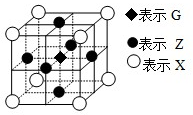 已知:E、G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大.E的简单阴离子最外层有2个电子,G原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同.T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于原子晶体;在元素周期表中Z元素位于第10列.
已知:E、G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大.E的简单阴离子最外层有2个电子,G原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同.T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于原子晶体;在元素周期表中Z元素位于第10列.查看答案和解析>>
科目:高中化学 来源: 题型:
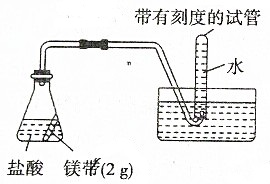 用如图所示的实验装置进行实验X及Y时,每隔半分钟分别测定放出气体的体积.下列选项中可正确表示实验X及Y的结果是( )
用如图所示的实验装置进行实验X及Y时,每隔半分钟分别测定放出气体的体积.下列选项中可正确表示实验X及Y的结果是( )| 实验 | 所用的酸 |
| X | 25mL 0.2mol/L |
| Y | 50mL 0.1mol/L |
A、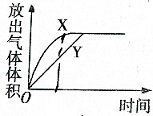 |
B、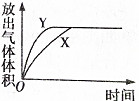 |
C、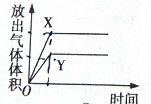 |
D、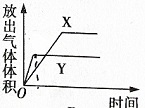 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com