
【题目】反应A(g)+B(g)→C(g) Δ H ,分两步进行:① A(g)+B(g)→X(g) Δ H1;② X(g)→C(g) Δ H2;反应过程中能量变化如图所示。下列说法正确的是
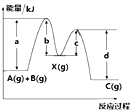
A.d是反应②的活化能
B.Δ H1 = (b - a) kJ ·mol-1
C.Δ H = - (b - c + d - a) kJ·mol-1
D.X是反应A(g) + B(g) → C(g) 的催化剂
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是 ( )
A. 向Ba(OH)2溶液中滴加NaHSO4溶液至沉淀刚好完全:Ba2+ + 2OH- + 2H+ + SO42- = BaSO4↓+ 2 H2O
B. AlCl3溶液中加入过量氨水:Al3++4OH-=== ![]() +2H2O
+2H2O
C. 向碳酸氢钙溶液中加入过量氢氧化钠:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
D. 澄清石灰水和碳酸钠溶液反应:Ca(OH)2+CO32-=CaCO3↓+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素W、X、Y、Z在元素周期表中的位置如图所示,这四种元素的最外层电子数之和为24,下列判断正确的是
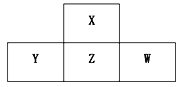
A.X、Z、W的原子半径依次增大
B.ZX2能使酸性高锰酸钾溶液褪色
C.Z元素的气态氢化物的沸点比X的高
D.W元素的氧化物的水化物酸性比Z的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,有A、B、C、D四种无色溶液,它们分别是溶CH3COONa液、NH4Cl溶液,盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH值相同。
则:(1)①B是___溶液,C是___。
②常温下若B溶液中c(OH-)与C溶液中的c(H+)相同,B溶液的pH用pHb表示,C溶液的pH用pHc表示,则pHb+pHc=___![]() 填某个数
填某个数![]() 。
。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则:(Ⅰ)上述关系一定不正确的是___![]() 填序号
填序号![]() 。
。
(Ⅱ)若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为___(填序号)。
(Ⅲ)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显___(填“酸性”、“碱性”或“中性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积均为2L的恒容密闭容器中发生反应:CO(g) + Cl2(g) ![]() COCl2(g)其中容器Ⅰ中5 min时到达平衡。
COCl2(g)其中容器Ⅰ中5 min时到达平衡。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 4.0 | 4.0 | 0 | 3.2 |
Ⅱ | 500 | 4.0 | a | 0 | 2.0 |
Ⅲ | 600 | 2.0 | 2.0 | 2.0 | 2.8 |
下列说法不正确的是
A.a = 2.2 mol
B.容器Ⅲ中前5 min的平均反应速率v(CO) = 0.08 mol·L-1·min-1
C.该反应在500℃时的平衡常数K = 5
D.若容器Ⅰ起始投料为CO 2.0 mol、Cl2 2.0 mol,平衡时CO转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是重要的化工原料,经一系列反应可得到HNO3、CO(NH2)2、HCN等产品。
(1)以氨气为原料合成HNO3工艺如下,写出N2O4转化为HNO3的反应方程式_____。
![]()
(2)以NH3和CO2为原料生产尿素的反应如下:
反应Ⅰ:2NH3(l) + CO2(g) ![]() NH2COONH4(l) Δ H1 = a kJ·mol-1
NH2COONH4(l) Δ H1 = a kJ·mol-1
反应Ⅱ:NH2COONH4(l) ![]() NH2CONH2(l) + H2O(l) Δ H2 = b kJ·mol-1
NH2CONH2(l) + H2O(l) Δ H2 = b kJ·mol-1
① 已知NH3(l) ![]() NH3(g) Δ H3 = c kJ·mol-1 反应2NH3(g) + CO2(g)
NH3(g) Δ H3 = c kJ·mol-1 反应2NH3(g) + CO2(g) ![]() NH2CONH2(l) + H2O(l) Δ H4=_____kJ·mol-1(用含a、b、c的式子表示),该反应能自发进行的主要原因是_____。
NH2CONH2(l) + H2O(l) Δ H4=_____kJ·mol-1(用含a、b、c的式子表示),该反应能自发进行的主要原因是_____。
② 一定条件下,往恒容密闭容器中投入4 mol NH3和 1 mol CO2,测得各组分物质的量随时间变化如图1。下列说法正确的是_____。
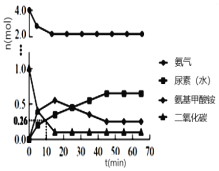
A.选择合适的碳氮比有利于提高产率
B.反应Ⅰ的活化能比反应Ⅱ小
C.过量氨气可以与反应生成的水结合,有利于尿素合成
D.气体物质的量不再变化时,反应达到平衡状态
(3)工业上利用氨气生产氢氰酸的反应为CH4(g) + NH3(g) ![]() HCN(g) + 3H2(g) Δ H>0
HCN(g) + 3H2(g) Δ H>0
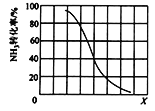
① 其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图所示。X代表的是_____(填“温度”或“压强”)。

② 其它条件一定时,向2 L密闭容器中加入n mol CH4和2 mol NH3,平衡时NH3体积分数随n变化的关系如图所示。平衡常数K=_____(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙是三种可溶性物质。其中甲是碱,乙、丙是盐,它们溶于水后电离产生的所有离子如下表所示:
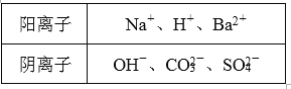
(1)甲的化学式为________________。
(2)乙溶液与丙溶液反应可生成气体M, 则M的化学式为________________,该反应的离子方程式为___________________________________________________。
(3)乙、丙溶液与甲溶液反应可分别生成白色沉淀A和B,其中B可溶于稀硝酸。
①乙的化学式为________________,如何鉴别乙中的阴离子:___________________________。
②B溶于稀硝酸的离子方程式为___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
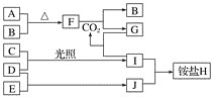
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com