
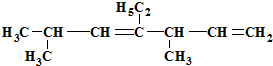 的名称是( )
的名称是( )| A、2,5-二甲基-4-乙基-3,6-庚二烯 |
| B、1,1,4-三甲基-3-乙基-2,5-己二烯 |
| C、3,6-二甲基-4-乙基-1,4-庚二烯 |
| D、2,5-二甲基-4-乙基-3,6-二庚烯 |
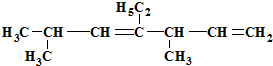 分子中含有两个碳碳双键,为二烯烃,选取含有两个碳碳双键的最长碳链为主链,最长碳链含有7个C,主链为庚二烯,据此进行正确命名,然后选择即可.
分子中含有两个碳碳双键,为二烯烃,选取含有两个碳碳双键的最长碳链为主链,最长碳链含有7个C,主链为庚二烯,据此进行正确命名,然后选择即可.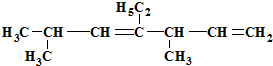 分子中含有两个碳碳双键,为二烯烃,选取含有两个碳碳双键的最长碳链为主链,最长碳链含有7个C,主链为庚二烯,编号距离碳碳双键最近的右端开始,碳碳双键在1、2号C和4、5号碳上,在3号、6号C上各含有1个甲基,在4号C含有1个乙基,该有机物名称为:3,6-二甲基-4-乙基-1,4-庚二烯,
分子中含有两个碳碳双键,为二烯烃,选取含有两个碳碳双键的最长碳链为主链,最长碳链含有7个C,主链为庚二烯,编号距离碳碳双键最近的右端开始,碳碳双键在1、2号C和4、5号碳上,在3号、6号C上各含有1个甲基,在4号C含有1个乙基,该有机物名称为:3,6-二甲基-4-乙基-1,4-庚二烯,

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
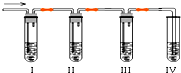 化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题:
化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeC13 |
| B、NaC1 |
| C、KNO3 |
| D、Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 13 |
| 2 |
| 13 |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| A、△H=-2 878 kJ?mol-1 |
| B、△H=-2 658 kJ?mol- |
| C、△H=-1 746 kJ?mol-1 |
| D、△H=-1 526 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| B、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C、用0.200 0 mol?L-1 NaOH标准溶液滴定HCl与CH3 COOH的混合液(混合液中两种酸的浓度均约为0.1 mol?L-1,至中性时,溶液中的酸未被完全中和 |
| D、相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol?L-1盐酸、③0.1 mol?L-1氯化镁溶液、④0.1 mol?L-1硝酸银溶液中,Ag+浓度:①>④=②>③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com