
【题目】X、Y、Z、W均为常见的短周期主族元素,常温下,其最高价氧化物对应的水化物溶液(浓度均为 0.01mol/L)的pH和原子半径的关系如下图所示。其中,Y为碳元素。下列有关说法正确的是

A. X是硫元素
B. Y的最高价氧化物的电子式为 ![]()
C. W的最高价氧化物对应的水化物中仅含离子键
D. Z的最高价氧化物对应水化物的化学式为HClO4
【答案】D
【解析】
X、Y、Z、W均为短周期主族元素,由其最高价氧化物对应水化物的pH和原子序数的关系图可以知道,X、Z对应的pH为2,高氯酸、硝酸均为一元强酸,原子半径Z>Y>X,Y为C,可以知道Z为Cl,X为N,W对应的pH为12,氢氧化钠为一元强碱,则W为Na,以此来解答。
由上述分析可以知道,X为N,Y为C,Z为Cl,W为Na,
A. X为N元素,不可能为硫元素,故A错误;
B. Y为C元素,其最高氧化物为CO2,电子式为![]() ,故B错误;
,故B错误;
C. W为Na元素,其最高价氧化物对应的水化物为NaOH,既含有离子键又含有共价键,故C错误;
D. Z为Cl元素,其最高价氧化物对应的水化物为HClO4,所以D选项是正确的。
所以D选项是正确的。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】工业上利用铁的氧化物在高温条件下循环裂解水制氢气的流程如下图所示。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
(2)反应III为:CO2(g)+C(s)![]() 2CO(g)
2CO(g) ![]() H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
(3)上述流程中铁的氧化物可用来制备含有Fe3+的刻蚀液,用刻蚀液刻蚀铜板时,可观察到溶液颜色逐渐变蓝,该反应的离子方程式为_________。刻蚀液使用一段时间后会失效,先加酸,再加入过氧化氢溶液,可实现刻蚀液中Fe3+的再生,该反应的离子方程式为_________。
(4)上述流程中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与Li<Na<K<Rb<Cs的变化规律不符合的是( )
A.与水或酸反应置换氢气越来越剧烈B.金属性由弱到强
C.氧化性由弱到强D.原子半径由小到大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下将1.92g铜粉投入一定量浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混合气体1.12 L,则反应消耗HNO3的物质的量为
A. 0.08molB. 0.06molC. 0.11molD. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应。硼与氯气反应生成三氯化硼(BCl3),生成的三氯化硼遇水水解产生白雾(已知:BCl3的熔点为-107.3℃,沸点为12.5℃ ),且三氯化硼用于制取乙硼烷(B2H6)。某兴趣小组设计如图所示装置制备三氯化硼。
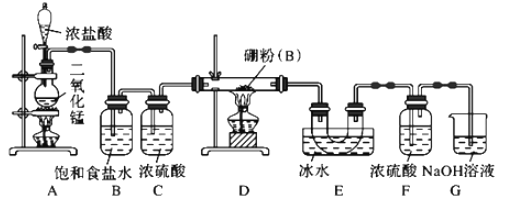
回答下列问题:
(1)装置A中发生反应的离子方程式为_____________________________。
(2)装置B中的作用是________________,装置E的作用是______________________。
(3)装置D中发生反应的化学方程式为______________________________________。
(4)装置F的作用是________________,可以用一个盛装________(填试剂名称)的干燥管代替装置F和G,使实验更简便。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;V和Z元素原子的最外层都只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子的L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。
回答下列问题:
(1)V的一种核素中质子数为中子数的![]() ,则该核素的名称为________,常用于制造________。
,则该核素的名称为________,常用于制造________。
(2)W元素在周期表中的位置为_______________________________。
(3)X元素的离子结构示意图为________。
(4)Z的最高价氧化物对应水化物的化学式为:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是重要的有机合成中间体,以下是用烯烃A和羧酸D合成它的一种路线:

回答下列问题:
(1)A的结构简式为__________。
(2)B→C的反应类型为__________。该反应还能生成一种与C互为同分异构体的副产物,该副产物的结构简式为____________。
(3) D→E的化学方程式为_____________。
(4) M是H的同分异构体,写出同时满足下列条件的M的结构简式_____________。(不考虑立体异构)
①1molM与足量银氨溶液反应生成4molAg;②核磁共振氢谱为两组峰。
(5)根据上述合成路线中的信息,某学习小组设计以丙二酸二乙酯和1,2-二溴乙烷为原料合成二甲酸环己烷的流程图如下。则甲的结构简式为_______,乙的结构简式为_______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com