
【题目】NA表示阿伏加德罗常数的值。室温下,下列关于 1 L 0.1 mol/L FeCl3 溶液的说法中正确的是
A.溶液中含有的 Fe3+离子数目为 0.1NA
B.加入 Cu 粉,转移电子数目为 0.1NA
C.加水稀释后,溶液中 c(OH-) 减小
D.加入 0. 15 mol NaOH 后,3c(Fe3+)+c(H+) = c(Na+) + c(OH-)
【答案】D
【解析】
A.Fe3+发生一定程度的水解,N(Fe3+)<0.1NA,故A错误;
B.Cu+2Fe3+=Cu2++2Fe2+,因加入Cu的量不确定,转移电子数目N(e-)≤0.1NA,无法确定,故B错误;
C.加水稀释使平衡Fe3++3H2O![]() 3H+ + Fe(OH)3向右移动,
3H+ + Fe(OH)3向右移动,![]() (H+ )增大,但c(H+ )减小,c(OH-)增大,故C错误;
(H+ )增大,但c(H+ )减小,c(OH-)增大,故C错误;
D.加入0.15 mol NaOH后,溶液中必有2c(Na+)=c(Cl-)(物料守恒)、3c(Fe3+)+c(Na+ )+c(H+)=c(OH-)+c(Cl-)(电荷守恒),可得3c(Fe3+)+c(H+)=c(Na+ )+c(OH-),故D正确;
答案选D。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如图:
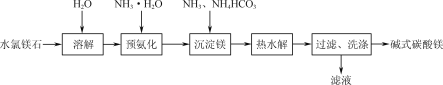
(1)为提高溶解速率,可以采取的措施有__(写一条)。
(2)检验碱式碳酸镁是否洗净的操作为___。
(3)预氨化过程中有Mg(OH)2沉淀生成,该过程发生反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A原子和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在加热下与足量的B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物。试根据以上叙述回答:
(1)元素名称:A_____,B______,C_______。
(2)D元素位于周期表中第_____周期_____族,它的最高价氧化物对应的水化物的化学式是_____________________。
(3)写出AB2与C2B2反应的化学方程式:____________。
(4)写出A单质与D元素的最高价氧化物对应水化物的浓溶液共热反应的化学方程式:___。若要设计实验验证该反应产物,则验证的产物顺序是_______(填写产物的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研团队研究将磷钨酸(H3PW12O40,以下简称HPW)代替浓硫酸作为酯化反应的催化剂,但HPW自身存在比表面积小、易溶于有机溶剂而难以重复使用等缺点,将其负载在多孔载体(如硅藻土、C等)上则能有效克服以上不足,提高其催化活性。用HPW负载在硅藻土上催化制取乙酸正丁酯的酯化率与HPW负载量的关系(温度:120℃,时间:2h)如图所示,下列说法不正确的是
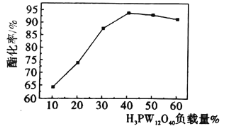
A.与HPW相比,HPW/硅藻土比表面积显著增加,有助于提高其催化性能
B.当HPW负载量为40%时达到饱和,酯化率最高
C.用HPW/硅藻土代替传统催化剂,可减少设备腐蚀等不足
D.不同催化剂对酯化率的影响程度主要取决于化学反应正向进行的程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)=2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1。对此反应速率的表示,正确的是( )
A.用A表示的反应速率是0.4 mol·(L·min)-1
B.分别用B、C、D表示反应的速率,其比是3∶2∶1
C.在2 min末的反应速率,用B表示是0.3 mol·(L·min)-1
D.在这2 min内用B和C表示的平均反应速率的值相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,硫酸盐 MSO4(M2+代表 Ba2+、Sr2+)的沉淀溶解平衡曲线如图所示。已知:p ( M2+ ) =-lgc ( M2+ ),p(SO42-)=-lgc(SO42-)。向 10mL 0.01 mol/L Na2SO4 溶液中滴入 1 滴(约 0. 05 mL) 0. 01 mol/L BaCl2 溶液岀现白色浑浊,而滴入 1 滴(约 0. 05 mL) 0. 01 mol/L SrCl2 溶液无浑浊出现。下列说法中错误的是
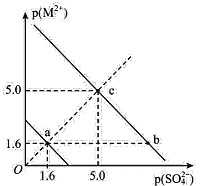
A.该温度下,溶度积常数 Ksp(BaSO4)<Ksp( SrSO4)
B.欲使c点对应BaSO4溶液移向b点,可加浓BaCl2溶液
C.欲使c点对应SrSO4溶液移向a点,可加浓SrCl2溶液
D.SrSO4(s)+Ba2+(aq)BaSO4(s)+Sr2+(aq)的平衡常数为106.8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g)ΔH<0,达到化学平衡状态,下列说法正确的是( )
2NH3(g)ΔH<0,达到化学平衡状态,下列说法正确的是( )
A.其他条件不变时,增大c(N2),H2的平衡转化率增大
B.其他条件不变时,降低温度,n(NH3)减小
C.其他条件不变时,增大压强,该反应的平衡常数增大
D.其他条件不变时,升高温度,该反应的化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积)。关于该固体混合物,下列说法正确的是

A. 一定含有Al,其质量为4.05g
B. 一定不含FeCl2,可能含有MgCl2和AlCl3
C. 一定含有MgCl2 和FeCl2
D. 一定含有(NH4)2SO4 和MgCl2,且物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水硫酸铜在加热条件下能发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气。某学生试图用如图所示装置来确定该化学反应中各物质的计量关系。
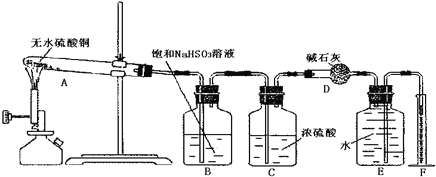
试回答:
(1)加热过程中,试管A中发生的实验现象可能有___。
(2)装置E和F的作用是___;
(3)该学生使用装置B的本意是除去混合气体中的三氧化硫以提纯氧气,他的做法正确吗?为什么?___。
(4)另一学生将9.6g无水硫酸铜充分加热使其完全分解后,用正确的实验方法除去了生成物中的二氧化硫和三氧化硫,最后测出氧气的体积为448mL(标准状况)。据此可计算出二氧化硫为___mol,三氧化硫为___mol。
(5)由上述实验数据可知无水硫酸铜受热分解的化学方程式:___。
(6)上述装置可以简化而不影响实验效果。请你提出一个简化方案,达到使装置最简单而不影响实验效果的目的:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com