
【题目】甲醇燃料电池的总反应为:2CH3OH +3O2= 2CO2 ↑+ 4H2O,下图是该电池的示意图。下列说法正确的是
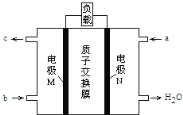
A.a 是氧气,b 是甲醇
B.质子从 N 电极区穿过质子交换膜移向 M 电极区
C.正极反应为:O2 +2H2O + 4e- = 4 OH-
D.当电路中有 3 mole- 转移时,电池中n(H+)变化为 0
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质性质的描述和该性质的应用均正确的是( )
A.氨气具有氧化性,用浓氨水检验氯气管道是否泄漏
B.氢氟酸具有强酸性.用氢氟酸蚀刻玻璃
C.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和结论均正确的是( )
选项 | 操作 | 现象 | 结论 |
A. | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉溶液后溶液变蓝色 | 氧化性:Cl2>I2 |
B. | 将可调节高度的铜丝伸入稀硝酸中 | 溶液变蓝 | 铜与稀硝酸发生置换反应 |
C. | 向溶液X中滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X中一定含有SO42- |
D. | 常温下将铝片放入浓硝酸中 | 无明显现象 | 铝与浓硝酸不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VIA 元素的各种性质可归纳整理如下:

回答下列问题:
(1)碲(Te)的氧化物分子式是____________________。
(2)硒酸与碲酸酸性较强的是____________________(填化学式)。
(3)比较键能:H—S H—Se(填“>”或“<”)。
(4)氢硒酸放在空气中,可能发生反应的化学方程式为______________________________。
(5)下图所示为 VIA 族元素单质与 H2反应过程中体系温度变化示意图,其中 a、b、c 分别表示VIA 族中某一元素的单质,下图为相同物质的量的单质与 H2反应过程中的体系温度变化。

则:c 代表__________。(均写单质名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
锂离子电池的广泛应用使得锂电池的回收利用一直是科学家关注的焦点。磷酸铁锂是锂电池中最有前景的正极材料,磷酸铁是其前驱体,充放电时可以实现相互转化。某研究性小组对废旧锂离子电池正极材料(图中简称废料,成份为LiFePO4、碳粉和铝箔)进行金属资源回收研究,设计实验流程如下:

已知:① FePO4可溶于稀H2SO4,不溶于水和其他的酸。
② Li2SO4、LiOH和Li2CO3在273K下的溶解度分别为34.2g、22.7g和1.54g,
在373K下,Li2CO3的溶解度为0.72g
③ Ksp[Al(OH)3]=10-32 Ksp[Fe(OH)3]=4×10-38
(1)操作1为: 。
(2)滤液A中通入过量CO2的化学方程式为: 。
(3)可以提高操作1浸出率的方法有(写出3种) 。
(4)完成操作3中的离子方程式: 。
(5)该锂电池充电时的阳极反应式: 。
(6)操作4中应选择试剂: 。
(7)沉淀C的成分: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是一种重要的化工产品,2SO2+O2![]() 2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
A.只要选择适宜的条件,SO2和O2就能全部转化为SO3
B.如果反应前充入由18O原子组成的O2,反应达到平衡状态时, 18O在所有物质中都存在
C.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零
D.在工业合成SO3时,只需要考虑反应速率的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是:( )
①化学性质相似的有机物是同系物
②分子组成相差一个或几个CH2原子团的有机物是同系物
③若烃中碳.氢元素的质量分数相同,它们必定是同系物
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似.
A.①②③④ B.只有②③ C.只有③④ D.只有①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】区别硝石(KNO3)和朴消(Na2SO4):“以火烧之,紫青烟起,乃真硝石也”--《本草经集注》,这里运用了硝石的哪些性质:
A.焰色反应 B.氧化性 C.还原性 D.不稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com