

| 1 |
| 2 |


 �¿α�������������ҵ�������γ�����ϵ�д�
�¿α�������������ҵ�������γ�����ϵ�д� ����ν����Ž̲��㽭���̴�ѧ������ϵ�д�
����ν����Ž̲��㽭���̴�ѧ������ϵ�д� �����Ļ������������������ϵ�д�
�����Ļ������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 L 1 mol?L-1��NaClO ��Һ�к���ClO-����ĿΪNA | ||
| B�����������ⸯʴ�ĸ�����Ӧ��Fe-3e-=Fe3+ | ||
| C���ж�һ�ֵ�ص����ӱ��ǣ���صijɱ� | ||
D����AlCl3��Һ�еμ�NaHCO3��Һ�������ӷ�Ӧ����ʽΪ��Al3++3HCO
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ��ͼװ����ʾ����ȷ�ⶨ�к��� ��ͼװ����ʾ����ȷ�ⶨ�к��� |
| B������50mL 0.55mo1?L-1������������Һ���ֱ���50mL 0.50mo1?L-1�������50mL0.50mo1?L-1�������ַ�Ӧ������Ӧ�ⶨ���к��Ȳ���� |
| C�����к͵ζ�ʵ���У��ζ���������ˮϴ�Ӻ����ñ�Һ��ϴ���ټӽ���Һ |
| D�������к͵ζ�����ʱ����������ƿ������ת����������Һ�����٣��۾�Ҫʼ��ע�ӵζ�������ҺҺ��ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Ϊ�ⶨij�ּ���������ԭ���������������ͼ��ʾ��װ�ã���װ�ã�����ˮ����������Ϊag��������Ϊbg�����������ļ��������ˮ�У���������ƿ������ȫ��Ӧ��װ�õ�������Ϊcg����
Ϊ�ⶨij�ּ���������ԭ���������������ͼ��ʾ��װ�ã���װ�ã�����ˮ����������Ϊag��������Ϊbg�����������ļ��������ˮ�У���������ƿ������ȫ��Ӧ��װ�õ�������Ϊcg�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.10mol?L-1��FeCl3��Һ��0.10mol?L-1��NaOH��Һ���������Ʊ�Fe��OH��3���� |
| B����FeSO4��Һ��������������NaOH��Һ�����ˡ�ϴ�ӡ���ɻ�ô�����Fe��OH��3���� |
| C����FeCl2��Һ�еμ�KSCN��Һ�������������ٵμӼ�����ˮ����Һ��ɺ�ɫ��˵��Fe2+���л�ԭ�� |
| D������������������������ŨHNO3�У�δ����������˵��Fe��ŨHNO3����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
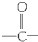 ���Ļ�����
���Ļ����� ��R��R����������Hԭ�ӣ��������Ϸ�Ӧ�����µ��л����ˮ�����ӻ��ɸ�����
��R��R����������Hԭ�ӣ��������Ϸ�Ӧ�����µ��л����ˮ�����ӻ��ɸ����� ��Ӧ�����л�����������
��Ӧ�����л�����������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��A B C D E |
| B��E C D B A |
| C��B A D C E |
| D��C D A B E |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| PCl3 |
| �� |
 ��д��������CΪԭ���Ʊ������ᣨ
��д��������CΪԭ���Ʊ������ᣨ ���ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�CH3CH2OH
���ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�CH3CH2OH| ŨH2SO |
| 170�� |
| H2 |
| ����/�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 -CH=CH2����D��HO-
-CH=CH2����D��HO- -CHO�������·����ϳɣ�
-CHO�������·����ϳɣ�
 -ONa+RCH2I��
-ONa+RCH2I�� -OCH2R+NaI
-OCH2R+NaI| һ������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com