
����Ŀ������β������NO�ķ�ӦΪ��N2(g)+O2(g)![]() 2NO(g)��һ�������£������ʵ�����N2(g)��O2(g)�ں����ܱ������з�Ӧ����ͼ����a��ʾ�÷�Ӧ���¶�T��N2��Ũ����ʱ��ı仯������b��ʾ�÷�Ӧ��ijһ��ʼ��Ӧ�����ı�ʱN2��Ũ����ʱ��ı仯������������ȷ����
2NO(g)��һ�������£������ʵ�����N2(g)��O2(g)�ں����ܱ������з�Ӧ����ͼ����a��ʾ�÷�Ӧ���¶�T��N2��Ũ����ʱ��ı仯������b��ʾ�÷�Ӧ��ijһ��ʼ��Ӧ�����ı�ʱN2��Ũ����ʱ��ı仯������������ȷ����

A.����b��Ӧ�������ı�����Ǽ����˴���
B.�¶�T�£����ŷ�Ӧ�Ľ��У����������ܶȼ�С
C.�¶�T�£��÷�Ӧ��ƽ�ⳣ��K =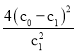
D.������b��Ӧ�������ı����¶ȣ����жϸ÷�Ӧ�����ȷ�Ӧ
���𰸡�CD
��������
A. ��ͼ��֪��b���ߵ�����ƽ��Ũ�ȼ�С��Ӧ��ƽ�ⷢ���ƶ�������ֻ�ܸı����ʣ�����ʹ��ѧƽ�ⷢ���ƶ�����b���߲��������ɴ���Ӱ��ģ�A����
B. ��Ӧ���������������壬���������m���䣬����Ϊ����������V���䣬��ô�ܶ���=![]() ���䣬B����
���䣬B����
C. ���ڷ�Ӧ��N2(g)+O2(g)![]() 2NO(g)����ʼʱ���ʵ�Ũ��c(N2)=c(O2)=c0 mol/L��c(NO)=0������ƽ��ʱc(N2)=c1 mol/L����Ӧ����(c0-c1) mol/L������ƽ��ʱc(O2)=c1 mol/L��c(NO)=2 (c0-c1) mol/L����÷�Ӧ�Ļ�ѧƽ�ⳣ��K=
2NO(g)����ʼʱ���ʵ�Ũ��c(N2)=c(O2)=c0 mol/L��c(NO)=0������ƽ��ʱc(N2)=c1 mol/L����Ӧ����(c0-c1) mol/L������ƽ��ʱc(O2)=c1 mol/L��c(NO)=2 (c0-c1) mol/L����÷�Ӧ�Ļ�ѧƽ�ⳣ��K=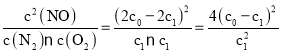 ��C��ȷ��
��C��ȷ��
D. ��ͼ��֪��b����ѧ��Ӧ���ʿ�(�仯���ȴ�)��������ƽ��Ũ�ȼ�С�������¶Ȼ�ѧ��Ӧ���ʼӿ죬��ѧƽ��������Ӧ�ƶ���������ӦΪ���ȷ�Ӧ������H>0��D��ȷ��
�ʺ���ѡ����CD��


 ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д� â���̸����������������ϵ�д�
â���̸����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��Һ��ֻ����OH-��H+��NH4+��Cl-�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳�������¼���
��c��Cl-����c��NH4+����c��H+����c��OH-��
��c��Cl-����c��NH4+����c��OH-����c��H+��
��c��NH4+����c��Cl-����c��OH-����c��H+��
��c��Cl-����c��H+����c��NH4+����c��OH-��
��1��������ϵһ������ȷ����_______________������ţ���
��2������Һ��ֻ��һ�����ʣ��������Ϊ__________������Һ������Ũ�ȵĴ�С��ϵΪ_______������ţ���
��3������ϵ����ȷ������Һ������Ϊ_________��
��4������������Ũ�ȹ�ϵ��c��NH4+��=c��Cl-���������Һ��_________������������������������������������
��5��25����pH=a������VamL��pH=14-a�İ�ˮVbmL��ϣ�����Һ�����ԣ���Va__________Vb���������=����ȷ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10mL0.1mol/LNaOH��Һ�м���0.1mol/L��һԪ��HA����ҺpH�ı仯������ͼ��ʾ������˵����ȷ���ǣ� ��

A.a����Һ�У�c(Na+)>c(A-)>c(H+)>c(HA)
B.a��c������Һ��ˮ�ĵ���̶���ͬ
C.b����Һ�У�c(Na+)=c(A-)+c(HA)
D.c����Һ�У�c(A-)>c(HA)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����0.100mol/L��NaOH��Һ�ζ�20.00ml��0.100mol/L��HNO2��Һ��lg![]() ������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ������˵���������
������NaOH��Һ����Ĺ�ϵ��ͼ��ʾ������˵���������
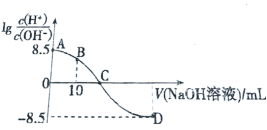
A.25��ʱ����0.100mol/L��HNO2��Һ��pHֵΪ2.75
B.B���Ӧ����Һ�У�2c(H+)+c(HNO2)=c(NO2-)+2c(OH-)
C.C���Ӧ��Һ��PH=7������NaOH��Һ�����Ϊ20.00ml
D.�ζ������д�A��D����Һ��ˮ�ĵ���̶���������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����ͼ��ʾװ���Ʊ�һ�����ױ�
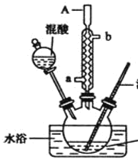 �ױ�
�ױ�
��֪.30��������Ҫ����Ϊһ�����ױ����¶ȹ���ʱ�����ɶ������ױ����������ױ���
ʵ�鲽������.
������Ũ�����Ũ���ᣨ�������1.3���Ļ������ᣩ
��������ƿ��װ15ml�ױ�
��װ������ҩƷ������װ������
����������ƿ�м�����ᣬ�����Ͻ���
�ݿ����¶ȣ���Լ��Ӧ10min��������ƿ���д���Һ�壨����ɫ��״������
�����һ�����ױ�������֪.�ױ����ܶ�Ϊ0.866g/ml���е�Ϊ110.6�������������ܶ�Ϊ1.20g/ml,�е�Ϊ210.9����
��������ʵ�飬�ش���������
��1��ʵ�鷽����ȱ��һ����Ҫ������������___________����ʵ��Ĺؼ��ǿ����¶���30�������ڣ�����¶ȹ��ߣ������ĺ����_____________________________________��
��2���������ƻ���ķ���_______________________________________________________��Ũ�����������______________________________��
��3��A������������_________________��ˮ����________________��
��4��д���ױ�����ᷴӦ���ɼ������ױ��Ļ�ѧ����ʽ___________________________��
��5�������Ʒ������ͼ��ʾ

����2��������_________________��
��6�����ⶨ����Ʒ1Ϊһ�����ױ�����˴Ź�����������3���壬����ṹ��ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ũ���������������Һ�У���������ɫ���壬����Һ���Ϻ�ɫ��ȥ������һ������ԭ��Ӧ����ϵ������KCl��Cl2��ŨH2SO4��H2O��KMnO4��MnSO4��K2SO4�������ʡ����������գ�
(1)д��һ�����������������ʵ�������ԭ��Ӧ����ʽ����ƽ���������ת�Ʒ������Ŀ��___________________________��
(2)������Ӧ�У���������_____________��ÿת��1 mol���ӣ�����Cl2_____ L����״������
(3)�ڷ�Ӧ�����Һ�м���NaBiO3(��������ˮ)����Һ�ֱ�Ϊ�Ϻ�ɫ��BiO3-��Ӧ���Ϊ��ɫ��Bi3+��д����ʵ�����漰��Ӧ�����ӷ�Ӧ����ʽ��_________________��
(4)��������ʵ�飬д��������Ӧ�������������������������ǿ��˳��__________��
(5)����������ԭ��Ӧ��ϵ�У����ڵ�������Ԫ�صļ����Ӱ뾶�ɴ�С��˳��Ϊ________
(6)��ԭ�ӵ��������ӵĹ��ʽΪ___________����ԭ�Ӻ�����_______��ͬ�˶�״̬�ĵ��ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������100 mL 0.01 mol/L��ϡ���ᷴӦ����Ӧ����̫����Ϊ�˼ӿ�˷�Ӧ���ʶ����ı�H2�IJ���������ʹ�����·����е�( )
�ټ�H2O �ڼ�NaOH����۵��뼸��Ũ���� �ܼ�CH3COONa���� �ݼ�NaCl��Һ ���뼸������ͭ��Һ �������¶�(����������ӷ�) �����10 mL 0.1 mol/L����
A.�٢ޢ�B.�ۢݢ�C.�ۢߢ�D.�ޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ļ���ԭ�ϣ���ҵ�������������Ƶ����ƣ��Ʊ����Ƶķ�Ӧԭ��Ϊ��Na2SO4��s��+4H2��g��Na2S��s��+4H2O��g����Q����֪�ÿ��淴Ӧ��1000��ʱ�ﵽƽ�⣬�����ַ�Ӧ���ں��º��ݣ��Իش��������⣺
��1���˿��淴Ӧ��ƽ�ⳣ������ʽ�ɱ�ʾΪ______����ֻ�ı�һ��Ӱ�����أ���ƽ���ƶ�ʱ��Kֵ______�仯������һ����������һ����������Kֵ���ʱ���淴Ӧ����______��������������������С��������������
��2���÷�Ӧ�ﵽƽ��ʱ����˵���������______��
a��������ѹǿ���ֲ���
b��������ˮ���������ʵ���֮�ȱ��ֲ���
c����������Fe3O4���壬ƽ�����淴Ӧ�����ƶ�
d���Ƴ�����Na2S���壬ƽ��������Ӧ�����ƶ�
��3�����¶��£���2Lʢ��2.84g Na2SO4���ܱ�������ͨ��H2���壬10���Ӻ��ù�������Ϊ2.264g����10������H2��ƽ����Ӧ����Ϊ______��
��4����Ba��ClO��2��Һ��ͨ������SO2�������Һ�е�������______��
��5�������������еμӷ�̪����Һ��Ϊ��ɫ�����ڸ���Һ���ٵ��������BaCl2��Һ��������______���������ӷ���ʽ������ƽ��ԭ�����н��ͣ�______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������FeCO3�������������Ҫ�ɷ֣���FeCO3���ȵ�200�濪ʼ�ֽ�ΪFeO��CO2�����ڿ����и�������FeCO3������Fe2O3���ݱ�����һ��������Fe2O3�ɱ����黹ԭΪ���������Ľ��������䷴ӦΪ��Fe2O3(s) + 3CH4(g)![]() 2Fe(s) + 3CO(g) + 6H2(g)-Q
2Fe(s) + 3CO(g) + 6H2(g)-Q
��1��ԭ������Ϊ26����Ԫ��λ��Ԫ�����ڱ��ĵ�________����__________�塣
��2����Ӧ��5L���ܱ������н��У�2min��ﵽƽ�⣬���Fe2O3�ڷ�Ӧ����������4.8g����ö�ʱ����H2��ƽ����Ӧ����Ϊ____________________��
��3�����̶�������Fe2O3(s)��CH4(g)���ں��º�ѹ�����У���һ�������·�Ӧ���ܱ����÷�Ӧ�ﵽƽ��״̬����__________________��
A��CH4��ת���ʵ���CO�IJ���
B����������ƽ����Է�����������
C��v��(CO)��v��(H2)=1�U2
D�����������������
��4��FeO����CO���л�ԭ����֪��t��ʱ�� FeO(s) +CO(g) ![]() Fe(s) + CO2(g) K��0.5����1 L�ܱ������м���0.04 mol FeO(s)����ͨ��x molCO��t��ʱ��Ӧ�ﵽƽ�⡣��ʱFeO(s)��ת����Ϊ50%����x��__________________________��
Fe(s) + CO2(g) K��0.5����1 L�ܱ������м���0.04 mol FeO(s)����ͨ��x molCO��t��ʱ��Ӧ�ﵽƽ�⡣��ʱFeO(s)��ת����Ϊ50%����x��__________________________��
��5��Fe2O3���������Ʊ�FeCl3 ��FeCl3��ˮ��Һ�е�ˮ���������
Fe3�� + H2O![]() Fe(OH)2+ + H�� K1
Fe(OH)2+ + H�� K1
Fe(OH)2+ + H2O![]() Fe(OH)2+ + H�� K2
Fe(OH)2+ + H�� K2
Fe(OH)2+ + H2O![]() Fe(OH)3 + H�� K3
Fe(OH)3 + H�� K3
����ˮ�ⷴӦ��ƽ�ⳣ��K1��K2��K3�ɴ�С��˳����____________________��
��6��ͨ����������������ˮ�����ۺ����ɾۺ�������ӷ���ʽΪ��xFe3++yH2O![]() Fex(OH)(3x-y)+ y+yH+����ʹƽ�������ƶ��ɲ��õķ�����_________________________������ĸ ����
Fex(OH)(3x-y)+ y+yH+����ʹƽ�������ƶ��ɲ��õķ�����_________________________������ĸ ����
A����ˮϡ�� B����������NaCl����
C������ D����������Na2CO3����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com