
【题目】误服铊盐会导致人体急性中毒,普鲁士蓝[KFe2(CN)6]可用作铊盐的解毒剂。
(1)Fe3+的价电子轨道表示式为___,与N同周期的主族元素中,第一电离能比N大的元素有___种。
(2)普鲁士蓝与硫酸作用可形成HCN,HCN的中心原子的杂化轨道类型为___,分子的立体构型是___,分子中σ键与π键数目之比为___。
(3)普鲁士蓝中的化学键不含有___(填字母)。
a.离子键
b.共价键
C.配位键
d.金属键
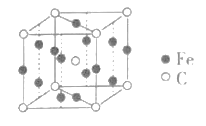
(4)已知FexCy的晶胞结构如图所示,则其化学式为___,铁原子的配位数是___。
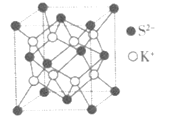
(5)如图为K2S的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是ρg·cm-3,试计算K+与S2-的最短距离为___nm(阿伏加德罗常数用NA表示)。
【答案】![]() 1 sp 直线形 1:1 d Fe3C 2
1 sp 直线形 1:1 d Fe3C 2 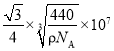
【解析】
(1)Fe是26号元素,电子排布式为1s22s22p63s23p63d64s2,因此Fe3+的价电子轨道表示式为![]() ,与N同周期的主族元素中,第一电离能比N大的元素有F共1种;故答案为:
,与N同周期的主族元素中,第一电离能比N大的元素有F共1种;故答案为:![]() ;1。
;1。
(2)HCN的中心原子价层电子对数为![]() ,其杂化轨道类型为sp,分子的立体构型是直线形,分子结构为H—C≡N,因此分子中σ键与π键数目之比为1:1;故答案为:sp;直线形;1:1。
,其杂化轨道类型为sp,分子的立体构型是直线形,分子结构为H—C≡N,因此分子中σ键与π键数目之比为1:1;故答案为:sp;直线形;1:1。
(3)a. 普鲁士蓝含有K+和[Fe2(CN)6]-,因此含有离子键,故a不符合题意;b. CN-含有共价键,故b不符合题意;c. [Fe2(CN)6]-含有配位键,故c不符合题意;d. 该离子化合物中不含金属键,故d符合题意;综上所述,答案为d。
(4)已知FexCy的晶胞结构如图所示,Fe的个数为![]() ,C的个数为
,C的个数为![]() ,则其化学式为Fe3C,以棱心的Fe分析,铁原子的配位数是2;故答案为:Fe3C;2。
,则其化学式为Fe3C,以棱心的Fe分析,铁原子的配位数是2;故答案为:Fe3C;2。
(5)如图为K2S的晶胞与CaF2晶胞结构相似,一个晶胞中有8个K+和4个S2,根据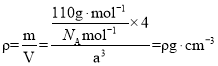 ,得到晶胞参数
,得到晶胞参数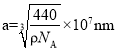 ,K+与S2的最短距离即为体对角线的四分之一,则
,K+与S2的最短距离即为体对角线的四分之一,则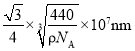 ;故答案为:
;故答案为: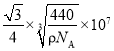 。
。


科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
A.现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B.5.6 g CO和22.4 L CO2中含有的碳原子数一定相等
C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D.a g Cl2中有b个氯原子,则阿伏加德罗常数NA的数值可表示为35.5b/a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铁和铁粉的混合物19.2 g,恰好溶于150 mL某浓度的稀硫酸,并收集到3.36 L(标准状况下)的气体.向反应后的溶液中滴加硫氰化钾溶液,不显血红色.求:
(1)与稀硫酸反应的铁的物质的量.___________
(2)稀硫酸的物质的量浓度._____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置,X、Y为两个电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列叙述正确的是
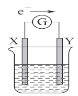
A.外电路中的电流方向为:X→外电路→Y
B.若两个电极分别为Zn和碳棒,则X为碳棒,Y为Zn
C.若两个电极都是金属,则它们的活动性为X>Y
D.X极上发生的是还原反应,Y极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利尿酸在北京2008年奥运会上被禁用,它是一种兴奋剂,其结构简式如图所示。下列叙述正确的是
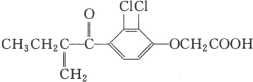
A.该有机物分子式为C13H16O4Cl2
B.1 mol利尿酸能与6 mol H2发生加成反应
C.利尿酸能使溴水褪色
D.利尿酸能与不能与NaOH溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
A.酸式滴定管在装酸液前未用标准盐酸溶液润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与如图图像有关的叙述,正确的是( )
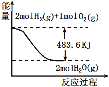
A.H2O(g)的能量低于H2(g)和O2(g)的能量之和
B.表示的热化学方程式为:H2(g)+![]() O2(g)=H2O(g)+241.8kJ
O2(g)=H2O(g)+241.8kJ
C.表示1molH2(g)完全燃烧生成水蒸气吸收241.8kJ热量
D.表示2molH2(g)所具有的能量一定比2mol气态水所具有的能量多483.6kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固态或气态碘分别与氢气反应的热化学方程式如下:
①H2(g)+I2(?)2HI(g)△H=-9.48kJmol-1
②H2(g)+I2(?)2HI(g)△H=+26.48kJmol-1
下列判断不正确的是( )
A.![]() 中的I2为气态,
中的I2为气态,![]() 中的I2为固态
中的I2为固态
B.![]() 的反应物总能量比
的反应物总能量比![]() 的反应总能量低
的反应总能量低
C.1mol固态碘升华时将吸热35.96kJ
D.反应![]() 的产物比反应
的产物比反应![]() 的产物热稳定性更好
的产物热稳定性更好
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定的密闭容器中存在如下反应:N2(g)+3H2![]() 2NH3(g) △H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出如下关系图,分析正确的是
2NH3(g) △H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出如下关系图,分析正确的是
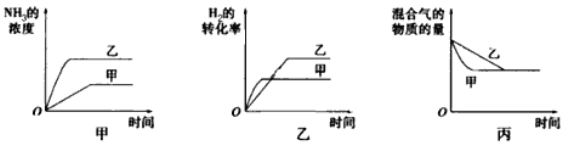
A. 图甲研究的是温度对反应的影响,且甲的温度比乙高
B. 图乙研究的是压强对反应的影响,且甲的压强比乙大
C. 图乙研究的是温度对反应的影响,且甲的温度比乙高
D. 图丙研究的是不同催化剂对反应的影响,且乙使用的催化剂效率比甲高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com