
 .
. .
. ;化合物ABC是氢氰酸,结构式为
;化合物ABC是氢氰酸,结构式为 .
. ;
; .
.

科目:高中化学 来源: 题型:
| A、将22.4 L HCl气体溶于水稀释至200 mL |
| B、将36.5 g HCl气体溶于200 mL水中 |
| C、取10 mol/L的盐酸100 mL加水100 mL |
| D、取10 mol/L的盐酸100 mL加水稀释至200 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3++3H2O═Fe(OH)3+3H+ |
| B、HSO3-+H2O?H2SO3+OH- |
| C、CH3COO-+H2O?CH3COOH+OH- |
| D、A13++3HCO3-═Al(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
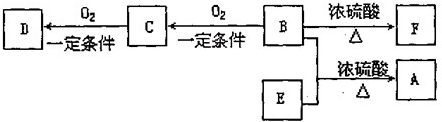
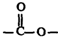 基团.
基团.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打是弱电解质,其水溶液导电能力很弱 |
| B、氨气是非电解质,但氨水能导电 |
| C、稀释醋酸溶液,可以促进醋酸分子电离使溶液pH减小 |
| D、硫酸是强电解质,在水溶液和熔融状态下均能导电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com