
【题目】生产、生活中下列过程不涉及氧化还原反应的是 ( )
A.多吃水果(富含维生素C)美容养颜B.铝的表面生成致密的氧化薄膜
C.久置于空气中,浓硫酸的体积增大D.食品袋内装有还原铁粉的小袋防食品变质
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E为元素周期表中前四周期元素,且原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。试回答下列有关的问题:
(1)写出基态D原子的外围电子排布式:______,E元素位于元素周期表______。
(2)A、B、C三种元素的第一电离能最大的是______![]() 用元素符号表示
用元素符号表示![]() 。这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______
。这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______ ![]() 写化学式
写化学式![]() 。
。
(3)D可形成化合物![]() 。
。
![]() 中配位体的VSEPR模型名称是_____________。该化合物中阴离子的中心原子的轨道杂化类型为_____________。
中配位体的VSEPR模型名称是_____________。该化合物中阴离子的中心原子的轨道杂化类型为_____________。
![]() 个
个![]() 中含有的
中含有的![]() 键数目为______个。
键数目为______个。
(4)已知B、C两种元素形成的化合物通常有两种。这两种化合物中_____________![]() 填化学式
填化学式![]() 为非极性分子,另一种化合物的电子式为_____________。
为非极性分子,另一种化合物的电子式为_____________。
(5)![]() 离子能与
离子能与![]() 离子形成ESCN沉淀。
离子形成ESCN沉淀。![]() 离子对应的酸有硫氰酸
离子对应的酸有硫氰酸![]() 和异硫氰酸
和异硫氰酸![]() ,这两种酸沸点更高的是______(填名称),原因是__________。
,这两种酸沸点更高的是______(填名称),原因是__________。
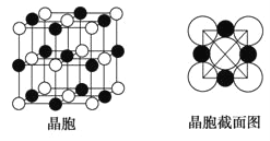
(6)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为A、C形成化合物的晶胞结构图以及晶胞的截面图,晶胞中距离一个![]() 最近的
最近的![]() 有______个,距离一个
有______个,距离一个![]() 最近的
最近的![]() 围成的图形是_____________
围成的图形是_____________![]() 写名称
写名称![]() 。若晶体密度为
。若晶体密度为![]()
![]() ,阿伏加德罗常数的值用
,阿伏加德罗常数的值用![]() 表示,则
表示,则![]() 的半径为____________________
的半径为____________________![]() 用含
用含![]() 与
与![]() 的式子表达
的式子表达![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组进行实验:向硫酸酸化的过氧化氢溶液中加入碘化钾、淀粉和硫代硫酸钠的混合溶液,一段时间后溶液变蓝。查阅资料知体系中存在两个主要反应:
反应i:H2O2(aq) + 2I-(aq) + 2H+(aq) I2(aq) + 2H2O(l) ΔH1 = -247.5 kJ/mol
反应ii:I2(aq) + 2S2O32-(aq) 2I-(aq) + S4O62-(aq) ΔH2 = -1021.6 kJ/mol
(1)H2O2与S2O32-反应的热化学方程式为______。
(2)下列实验方案可证实上述反应过程。将实验方案补充完整(所用试剂浓度均为0.01 mol/L)。
a.向酸化的H2O2溶液中加入________溶液,溶液几秒后变为蓝色。
b._________,溶液立即褪色。
(3)探究c(H+)对反应速率的影响,实验方案如下表所示。(所用试剂除H2O以外,浓度均为0.01 mol/L)
实验序号 | a | b | |
试 剂 | H2O2/mL | 5 | ______ |
H2SO4/mL | 4 | 2 | |
Na2S2O3/mL | 8 | _____ | |
KI(含淀粉)/mL | 3 | _____ | |
H2O | 0 | ______ | |
将上述溶液迅速混合 观察现象 | 溶液变蓝所需时间 为t1秒 | 溶液变蓝所需时间 为t2秒 | |
① 将实验b补充完整。
② 对比实验a和实验b,t1_____t2(填“>”或“<”)。
③ 结合(2)中现象解释溶液混合后一段时间才变蓝的原因________。
④ 利用实验a的数据,计算t1时间内H2O2与S2O32-反应的平均反应速率(用H2O2浓度的变化表示)________mol/(L·s)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:Ⅰ.2SO2(g) + O2(g)![]() 2SO3(g)ΔH=-196.6 kJ· mol-1
2SO3(g)ΔH=-196.6 kJ· mol-1
Ⅱ.2NO(g) + O2(g) ![]() 2NO2(g)ΔH=-113.0 kJ· mol-1
2NO2(g)ΔH=-113.0 kJ· mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=____kJ· mol-1。
SO3(g)+NO(g)的ΔH=____kJ· mol-1。
(2)一定条件下,将NO2(g)与SO2(g)以体积比2∶1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是____。
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变 D.每消耗1 mol SO3的同时生成1 mol NO
(3)CO可用于合成甲醇,化学方程式为CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图甲所示,该反应的ΔH____0(填“>”或“<”)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图甲所示,该反应的ΔH____0(填“>”或“<”)。

(4)依据燃烧的反应原理,合成的甲醇可以设计成如图乙所示的原电池装置。
①该电池工作时,OH-向____(填“正”或“负”)极移动。
②该电池正极的电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质加入水中或与水发生反应后,溶液温度降低的是( )
A. 生石灰与水反应 B. 氢氧化钠固体加入水中
C. 浓硫酸加入水中 D. 硝酸铵晶体加入水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从经济效益和环境保护的观点出发,由铜制取硝酸铜最适宜的方法是
A. Cu与浓HNO3―→Cu(NO3)2
B. Cu与稀HNO3―→Cu(NO3)2
C. Cu![]() CuO
CuO![]() Cu(NO3)2
Cu(NO3)2
D. Cu+AgNO3―→Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴酸银(AgBrO3)溶解度随温度变化曲线如图3-4-2所示。下列说法错误的是( )
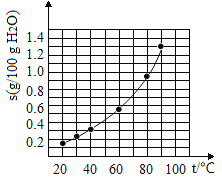
A. 溴酸银的溶解是放热过程
B. 温度升高时溴酸银的溶解速率加快
C. 60℃时溴酸银的Ksp约等于6×10-4
D. 若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷![]() 是第四周期ⅤA族元素,可以形成
是第四周期ⅤA族元素,可以形成![]() 、
、![]() 、
、![]() 、
、![]() 等 化合物,有着广泛的用途
等 化合物,有着广泛的用途![]() 回答下列问题:
回答下列问题:
(1)写出砷的原子序数______________
(2)工业上常将含砷废渣![]() 主要成分为
主要成分为![]() 制成浆状,通入
制成浆状,通入![]() 氧化,生成
氧化,生成![]() 和单质硫
和单质硫![]() 写出发生反应的化学方程式 _____________________________________________
写出发生反应的化学方程式 _____________________________________________ ![]() 该反应需要在加压下进行,原因是 _______________________________________
该反应需要在加压下进行,原因是 _______________________________________
(3)已知:![]()
![]()
![]()
则反应![]() 的
的![]() ________________________
________________________
(4)![]() 时,将
时,将![]() 、
、![]()
![]() 和20mLNaOH溶液混合,发生反应:
和20mLNaOH溶液混合,发生反应:![]() 溶液中
溶液中![]() 与反应时间
与反应时间![]() 的关系如图所示.
的关系如图所示.

①下列可判断反应达到平衡的是 ______ ![]() 填标号
填标号![]() .
.
![]() 溶液的pH不再变化
溶液的pH不再变化 ![]()
![]()
![]() 不再变化
不再变化 ![]()
![]()
②![]() 时,
时,![]() ______
______![]() 填“大于”“小于”或“等于”
填“大于”“小于”或“等于”![]()
③![]() 时,
时,![]() ______
______![]() 时
时![]() 填“大于”“小于”或“等于”
填“大于”“小于”或“等于”![]() ,理由是 ____________________
,理由是 ____________________
④若平衡时溶液的![]() ,则该反应的平衡常数K为 ______________
,则该反应的平衡常数K为 ______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com