
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.常温常压下,11.2L氧气所含的原子数为NA
B.标准状况下,1.12L氦气所含的原子数为0.1NA
C.1.8 g NH4+离子中含有的电子数为NA
D.15.6 g Na2O2与过量CO2反应时,转移的电子数为0.4NA
科目:高中化学 来源: 题型:
【题目】联胺是火箭的燃料,一种用联胺制成的燃料电池示意图如图(总反应为:N2H4+O2=N2+2H2O),下列说法正确的是( )
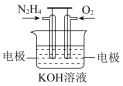
A.该电池工作时,电子从负极经电解质溶液到正极
B.电池工作一段时间后,溶液的pH减小
C.负极的电极反应式为:N2H4-4e-=N2↑+4H+
D.当电路中通过0.1 mol电子时,负极消耗0.56 L的氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅是一种高密度、柔软的蓝灰色金属。2019年7月23日,铅被列入有害水污染物名录。请回答下列问题。
(1)Pb位于第六周期,与C元素同族。请写出它的外围电子排布式___________,对比以下三种氧化物的熔沸点![]() 、
、![]() 、
、![]() ,从小到大分别为_____________,请解释原因:____________________。
,从小到大分别为_____________,请解释原因:____________________。
(2)铅在自然界主要以方铅矿(PbS)及白铅矿(![]() )的形式存在,也存在于铅矾(
)的形式存在,也存在于铅矾(![]() )中。
)中。![]() 中心原子轨道的杂化类型___________,
中心原子轨道的杂化类型___________,![]() 的空间构型____________。
的空间构型____________。
(3)四乙基铅[![]() ]曾广泛用作汽油中的抗爆剂,由Pb提供空轨道,有机原子团提供孤电子对形成,该化合物中存在化学键类型有_____________
]曾广泛用作汽油中的抗爆剂,由Pb提供空轨道,有机原子团提供孤电子对形成,该化合物中存在化学键类型有_____________
A.金属键 B.离子键 C.共价键 D.配位键
(4)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(![]() )半导体作为吸光材料,
)半导体作为吸光材料,![]() 具有钙钛矿(
具有钙钛矿(![]() )的立方结构,其晶胞如图所示:
)的立方结构,其晶胞如图所示:
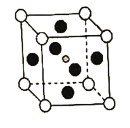
①比较元素电负性:C_________N(填“>”或“<”),比较基态原子第一电离能:C________Pb(填“>”或“<”)
②![]() 晶胞中与金属阳离子(M)距离最近的卤素阴离子(X)形成正八面体结构,则M在晶胞中处于_____________位置,X在晶胞中处于________位置。
晶胞中与金属阳离子(M)距离最近的卤素阴离子(X)形成正八面体结构,则M在晶胞中处于_____________位置,X在晶胞中处于________位置。
③![]() 晶体的晶胞边长为a nm,其晶体密度为d
晶体的晶胞边长为a nm,其晶体密度为d![]() ,则阿伏加德罗常数的值NA的计算表达式为_____________
,则阿伏加德罗常数的值NA的计算表达式为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.1.8 g NH4+含有的电子数为NA
B.1 L 1 mol·L-1的NaAlO2水溶液中含有的氧原子数为2NA
C.标况下,22.4 L NO与11.2 L O2充分反应后,生成物的分子总数为NA
D.50 mL 18 mol·L-1的浓硫酸与足量的铜片共热,生成SO2的分子数为0.45NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
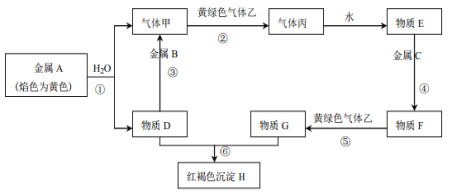
请回答下列问题:
(1)写出 B、乙的化学式:B_______________、乙_______________。
(2)写出下列反应的化学方程式:
反应⑤ ___________________________________________________________;
反应⑥____________________________________________________________。
(3)写出下列反应的离子方程式:
反应①___________________________________________________________;
反应③___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稠环芳香烃是指两个或两个以上的苯环通过共用环边所构成的多环有机化合物。常见的稠环芳香烃如萘、蒽、菲、芘等,其结构分别为
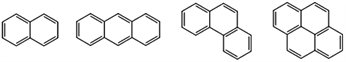
萘 蒽 菲 芘
下列说法不正确的是
A. 萘的分子式为C10H8,与H2完全加成后,产物的分子式为C10H18
B. 蒽、菲、芘的一氯代物分别有3种、5种、5种
C. 上述四种物质的分子中,所有碳原子均共平面
D. 上述四种物质均可与浓硝酸发生硝化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时将nmol·L-1氨水滴入10mLymol·L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法不正确的是( )
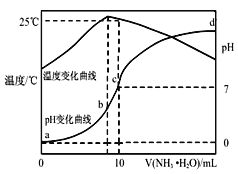
A.y=1.0
B.a点时Kw<1×10-14
C.b点c(NH4+)<c(Cl-)=![]() mol·L-1
mol·L-1
D.25℃时,NH4Cl的水解常数(Kh)可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室探究SO2性质的装置如图所示。下列说法错误的是( )
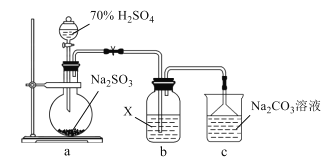
A.装置a中的反应可用铜片和浓硫酸代替
B.若X为H2S溶液,装置b中产生淡黄色沉淀
C.若X为含HCl、BaCl2的FeCl3溶液,装置b中产生白色沉淀
D.反应后装置c中溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)中提取氧化铝的两种工艺流程如图:
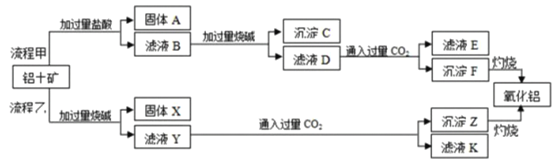
请回答下列问题:
(1)固体A的主要成分是___(写名称)。
(2)铝土矿与过量盐酸反应的离子方程式为___、___。
(3)电解熔融氧化铝可制得单质铝,写出该反应化学方程式____;已知氯化铝的熔点更低,工业中为何不用电解熔融氯化铝的方法制备该单质___。
(4)得到的单质铝可以跟强碱溶液放出氢气,每转移6.02×1025个电子,实际上参与反应的氧化剂为___mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com