
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

2)整个过程中的还原剂是 。
3)把KI换成KBr,则CCl4层变为__色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若庄Kl与Cl2反应制KIO3,至少需要消耗Cl2 L(标准状况,保留2位小数)。
【答案】1)I2+5Cl2+6H2O→2HIO3+10HCl;2)KI、I2;3)红棕、HBrO3>Cl2>HIO3;4)10.58。
【解析】此题考查氧化还原反应的配平、氧化剂和还原剂、氧化性强弱的判断、化学计算知识。分析反应从开始滴加少许氯水时,其将KI中的I元素氧化成碘单质;等CCl4层变紫色后,再滴加氯水时,其将碘单质进一步氧化成碘酸。1)根据氧化还原反应方程式的配平原则,分析反应中的化合价变化,I元素的化合价从0→+5,升高5价,Cl元素的化合价从0→-1,降低1价,综合得失电子守恒和质量守恒,可配平出:I2+5Cl2+6H2O→2HIO3+10HCl;2)分析整个过程中化合价升高的都是I元素,还原剂为:KI和I2;3)KI换成KBr时,得到的是溴单质,则其在CCl4中呈红棕色;继续滴加氯水时,颜色不变,可知氯水不能将溴单质氧化成HBrO3,故其氧化性强弱顺序为:HBrO3>Cl2>HIO3;4)综合写出反应方程式:KI+3Cl2+3H2O=KIO3+6HCl,根据化学方程式计算,按最小值计算时,1000kg加碘食盐中含碘20g,根据质量守恒,可知:换算成碘酸钾的质量为:33.70g,物质的量为:0.16mol,则需要消耗Cl2的体积为:( 20g/127g.mol-1)×3×22.4L/mol=10.58L。
20g/127g.mol-1)×3×22.4L/mol=10.58L。
解法点拨:守恒定律是自然界最重要的基本定律,是化学科学的基础。在化学反应中,守恒包括原子守恒、电荷守恒、得失电子守恒等。任何化学反应在反应前后应遵守电荷或原子守恒。电荷守恒即反应前后阴阳离子所带电荷数必须相等 ;原子守恒(或称质量守恒),也就是反应前后各元素原子个数相等;得失电子守恒是指在氧化还原反应中,失电子数一定等于得电子数,即得失电子数目保持守恒。比如此题中我们就牢牢抓住了守恒,简化了计算过程,顺利解答。
;原子守恒(或称质量守恒),也就是反应前后各元素原子个数相等;得失电子守恒是指在氧化还原反应中,失电子数一定等于得电子数,即得失电子数目保持守恒。比如此题中我们就牢牢抓住了守恒,简化了计算过程,顺利解答。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
向某晶体的水溶液加入含Fe2+的溶液后,无明显变化,当滴加几滴溴水后,混合液出现红色,那么由此得出的下列结论错误的是( )
A.该晶体中一定含有SCN-
B.Fe3+的氧化性比Br2的氧化性强
C.Fe2+与SCN-不能形成红色的化合物
D.Fe2+被Br2氧化成Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
己知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O
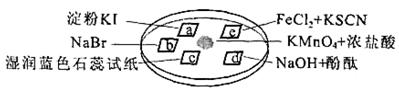
对实验现象的“解释或结论”正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+ > Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
科研、生产中常涉及钠、硫及其化合物。
(1)实验室可用无水乙醇处理少量残留的金属钠,化学反应方程式为 。要清洗附着在试管壁上的硫,可用的试剂是 。
(2)下图为钠硫高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+ S=Na2
S=Na2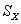 ,正极的电极反应式为 。M(由Na2O和Al2O3制得)的两个作用是 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的 倍。
,正极的电极反应式为 。M(由Na2O和Al2O3制得)的两个作用是 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的 倍。
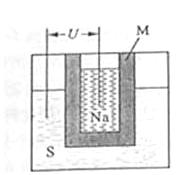
(3)Na2S溶液中离子浓度由大到小的顺序为 ,向该溶液中加入少量固体CuSO4,溶液PH
(填“增大”“减小”或“不变”),Na2S溶液长期放置有硫析出,原因为 (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
 右图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是
右图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是
A.烧瓶中立即出现白烟
B.烧瓶中立即出现红棕色
C.烧瓶中发生的反应表明常温下氨气有还原性
D.烧杯中的溶液是为了吸收有害气体
查看答案和解析>>
科目:高中化学 来源: 题型:
用浓氯化铵溶液处理过的舞台幕布不易着火。其原因是( )
①幕布的着火点升高 ②幕布的质量增加 ③氯化铵分解吸收热量,降低了温度 ④氯化铵分解产生的气体隔绝了空气
A.①② B.③④ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
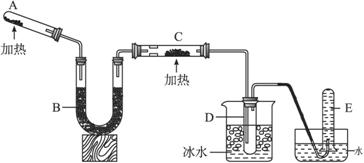
回答下列问题:
(1)A中加入的物质是_______________________,
发生反应的化学方程式是_______________________;
(2)B中加入的物质是____________,其作用是_______________________;
(3)实验时在C中观察到的现象是_______________________,发生反应的化学方程式是_______________________;
(4)实验时在D中观察到的现象是_________________,D中收集到的物质是____________,检验该物质的方法和现象是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
O3和H2O2都是常见的氧化剂,下列有关说法错误的是( )
A.O3和O2互为同位素
B.O3和H2O2的分子内都含有共价键
C.H2O2具有氧化性,可以用于消毒杀菌
D.高空中的O3层保护人类免受紫外线 伤害
伤害
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量的下列化合物在相应条件下完全分解后得到氧气最多的是
A.KClO3(加MnO2催化剂,加热) B.KMnO4(加热)
C.H2O2(水溶液,加MnO2催化剂) D.HgO(加热)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com