
【题目】(1)SO2和SO3是硫的两种氧化物,等温等压下,等质量的SO2和SO3所含分子个数比为________,氧原子个数比为________,等温等压下气体体积比_____________。
(2)100mL的某气体的质量为0.143g,该气体的相对分子质量:______________,
(3)设NA为阿伏加德罗常数的数值,如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积约是___________L(用含NA的式子表示)。
(4)配制100 mL1 mol/L的H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为__________mL。
(5)10.6gNa2CO3溶于水,配成500mL的溶液,溶液中溶质的物质的量________,Na+的物质的量浓度______________。
(6)标准状况下,5.6LNH3中氢原子的数目为_________________。
【答案】5:4 5:6 5:4 32 22.4bc/(aNA) 5.4 0.1mol 0.4mol/L 0.75NA
【解析】
(1)根据阿伏伽德罗定律及其推论分析;结合物质结构计算;
(2)根据M=![]() 分析计算;
分析计算;
(3)先求出其摩尔质量,然后再根据V=![]() 分析计算;
分析计算;
(4)先根据c=![]() 求出其浓度,再根据稀释定律计算;
求出其浓度,再根据稀释定律计算;
(5)利用n=![]() =cV分析作答;
=cV分析作答;
(6)根据n=![]() =
=![]() 分析计算。
分析计算。
(1)阿伏伽德罗定律及其推论可知,体积之比等于分子数之比等于物质的量之比,则等质量的SO2和SO3所含分子个数比为![]() =
=![]() =
=![]() =
=![]() =
=![]() ;SO2中含有2个氧原子,SO3中含有3个氧原子,氧原子个数比为
;SO2中含有2个氧原子,SO3中含有3个氧原子,氧原子个数比为![]() =
=![]() ;
;
(2)M=![]() =
=![]() =32g/mol,即相对分子质量为32;
=32g/mol,即相对分子质量为32;
(3)摩尔质量M=![]() =
=![]() g/mol,V=
g/mol,V=![]() =
=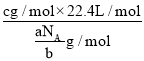 =
=![]() L;
L;
(4)c=![]() =
=![]() =18.4mol/L,V浓=
=18.4mol/L,V浓=![]() =
=![]() =0.0054L=5.4mL;
=0.0054L=5.4mL;
(5)n=![]() =
=![]() =0.1mol,c=
=0.1mol,c=![]() =
=![]() =0.2mol/L,c(Na+)=0.4mol/L;
=0.2mol/L,c(Na+)=0.4mol/L;
(6)n=![]() =
=![]() =0.25mol,氢原子的物质的量为0.25mol×3=0.75mol,氢原子的数目为0.75NA。
=0.25mol,氢原子的物质的量为0.25mol×3=0.75mol,氢原子的数目为0.75NA。


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】用下图表示的一些物质或概念间的从属关系中正确的是
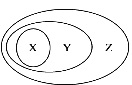
X | Y | Z | |
A | 水 | 单质 | 纯净物 |
B | 非金属氧化物 | 酸性氧化物 | 氧化物 |
C | 电解质 | 化合物 | 纯净物 |
D | 化合反应 | 氧化还原反应 | 化学反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了抵御海水的侵蚀,往往会在船体上安装大型的锌块,利用原电池反应:2Zn+2H2O+O2 = 2Zn(OH)2,下列说法正确的是
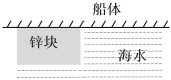
A. 锌块作为原电池的负极,发生还原反应而被腐蚀
B. 海水中的电解质如NaCl起到了导电的作用
C. 正极的电极反应式为:Zn - 2e-=Zn2+
D. 实际应用中,需用锌块覆满船体,完全隔绝海水以防止钢铁被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚铁可用于制备补血剂。某研究小组制备了 FeCO3,并对 FeCO3 的性质和应用进行了探究。
已知:①FeCO3 是白色固体,难溶于水②Fe2++6SCN-Fe(SCN)64-(无色)
Ⅰ.FeCO3 的制取(夹持装置略)
实验i
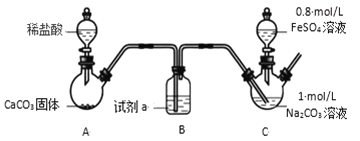
装置 C 中,向 Na2CO3 溶液(pH=11.9)通入一段时间 CO2 至其 pH 为 7,滴加一定量 FeSO4溶液,产生白色沉淀,过滤、洗涤、干燥,得到 FeCO3 固体。
(1)试剂 a 是________。
(2)向 Na2CO3 溶液通入 CO2 的目的是________。
(3)C 装置中制取 FeCO3 的离子方程式为________。
Ⅱ.FeCO3 的性质探究
实验ii
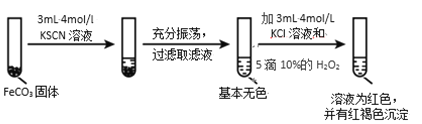
实验iii
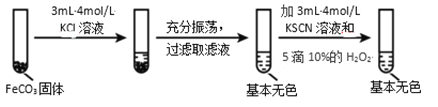
(4)对比实验ⅱ和ⅲ,得出的实验结论是________。
(5)依据实验ⅱ的现象,写出加入 10%H2O2 溶液的离子方程式________。
Ⅲ.FeCO3的应用
(6)FeCO3 溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂,此反应的离子方程式为____。
(7)该实验小组用 KMnO4 测定补血剂中亚铁含量进而计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于 100%,其原因是____(不考虑操作不当引起的误差)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
①氧化剂与还原剂的物质的量比是_______;如果反应生成0.3mol的单质碘,则转移的电子数目是_______。
②先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是_____;
③若采用下图实验装置将四氯化碳和I2的混合溶液分离。
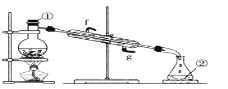
写出图中仪器的名称:①_____;该装置还缺少的仪器是_____;冷凝管的进水口是:_____(填g或f)。
(2)实验室常用MnO2和浓盐酸制氯气,反应原理:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①实验室用MnO2和浓盐酸制氯气的离子方程式:__________________________
②上述反应中氧化剂:__________,还原剂:__________,被氧化的HCl和未被氧化的HCl的比值______________。
③a : Cl2+2I-=I2+2Cl-; b: Cl2+2Fe2+=2Fe3++Cl-; c:2Fe3++2I-=I2+2Fe2+。 Cl2、I2、Fe3+的氧化性由强到弱的顺序:_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:

(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、②的化学方程式是___________________、__________________。
(2)基态铜原子的核外电子排布式为________,硫、氧元素相比,第一电离能较大的是________。
(3)反应①和②生成的气体分子的中心原子的杂化类型是________,分子的空间构型是________。
(4)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________(填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
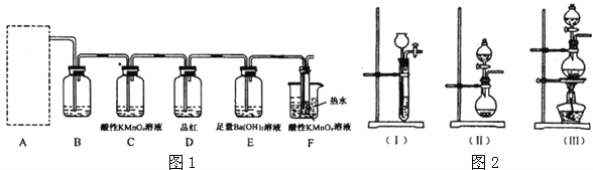
试回答下列问题:
①图1的A中最好选用下列装置_________(填编号);
②图1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;
③图1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;
④某学生按图2进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因_________,其反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请选择适当的化学试剂和实验用品,用下图所示的装置(C中盛放的是过氧化钠)进行实验,证明过氧化钠可在呼吸面具和潜水艇中做供氧剂。
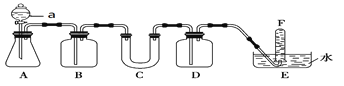
(1)A是实验室制取CO2的装置,写出A中发生反应的离子方程式________________。
(2)B中所加试剂是饱和NaHCO3溶液,它的作用是________________。
(3)写出C中发生反应的化学方程式__________________。
(4)F中得到的气体是__________,验证该气体的方法是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温,将10mL浓度为![]() 的
的![]() 、
、![]() 两种一元碱溶液分别加水稀释,曲线如图,V是溶液体积(mL),
两种一元碱溶液分别加水稀释,曲线如图,V是溶液体积(mL),![]() 。已知:
。已知:![]() ;
;![]() 。下列说法正确的是( )
。下列说法正确的是( )
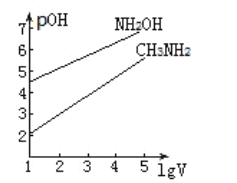
A.该温度下,![]() 的数量级为
的数量级为![]()
B.当![]() 时,水的电离程度:
时,水的电离程度:![]()
C.用等浓度盐酸分别滴定两种碱溶液至![]() ,消耗盐酸的体积:
,消耗盐酸的体积:![]()
D.等浓度的![]() 和
和![]() 两种盐溶液中离子总浓度相等
两种盐溶液中离子总浓度相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com