
【题目】有机物A只含有C、H、O三种元素,常用作有机合成的中间体。16.8 g该有机物燃烧生成44.0 g CO2和14.4 g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1。
(1)A的分子式是 ,A的结构简式是
(2)有机物B是A的同分异构体,1 mol B可与1 mol Br2加成。该有机物中所有碳原子在同一个平面上,没有顺反异构现象。B的结构简式是
【答案】(1)C5H8O(2)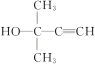 (3)
(3)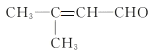
【解析】
题分析:(1)质谱图表明其相对分子质量为84,16.8g有机物的物质的量是16.8g÷84g/mol=0.2mol,完全燃烧生成44gCO2和14.4g水,物质的量分别是1mol、14.4g÷18g/mol=0.8mol,所以根据原子守恒可知有机物分子中碳原子和氢原子的个数分别是1mol÷0.2mol=5、0.8mol×2/0.2mol=8,因此含有的氧原子个数是![]() ,因此分子式为C5H8O;红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1,因此结构简式为
,因此分子式为C5H8O;红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1,因此结构简式为 。
。
(2)有机物B是A的同分异构体,1 mol B可与1 mol Br2加成,说明含有一个碳碳双键,该有机物中所有碳原子在同一个平面上,没有顺反异构现象,因此B的结构简式是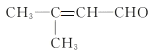 。
。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】硫及其主要的化合物在化学研究及生产生活中都有重要的应用。
(1)硫的气态氢化物H2S是一种臭鸡蛋气味的气体,写出它的电子式 ,H2S的水溶液在空气中放置时,会逐渐变浑浊,这说明H2S有强的 性。
(2)硫单质在一定条件下能与硫化钠反应分别生成多硫化钠(与Na2O2结构相似),反应方程式为:Na2S+(x-1)S=Na2Sx
①Na2Sx中所合化学键的类型有 。
②已知向多硫化钠溶液中滴加稀盐酸,溶液变浑浊,且有臭鸡蛋气味的气体生成,写出发生反应的离子方程式: 。
(3)硫代硫酸钠(Na2S2O3)俗名叫大苏打,在中学化学实验中利用它和稀硫酸的反应探究温度对化学反应速率的影响。
①写出Na2S2O3与稀硫酸反应的化学方程式: 。
②S2O32-有很强的配位能力,照相底片上未曝光的溴化银在定影液(含Na2S2O3)中由于形成一个配位数为2的配离子而溶解,该配离子的化学式为: 。
(4)锅炉水垢中的硫酸钙因难溶于酸而很难清洗,通常采取的方法为先用饱和碳酸钠溶液处理,再用稀盐酸除去;写出用饱和碳酸钠溶液处理时发生反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如右图装置。下列叙述不正确的是( )

A、a和b分别与电源的负极正极相连时,电解氯化钠溶液产生氯气。
B、a和b用导线连接时,碳棒上发生的反应为:O2+2H2O+4e-=4OH-
C、若往溶液中加少许硫酸,无论a和b是否连接,铁片均会溶解,溶液逐渐变成浅绿色
D、若氯化钠溶液改为氯化铵溶液,a和b连接,碳棒上有气泡产生。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸正丁酯是无色透明有愉快果香气味的液体,可由乙酸和正丁醇制备。反应的化学方程式如下:![]()
发生的副反应如下:
有关化合物的物理性质见下表:
化合物 | 密度(g·cm-3) | 水溶性 | 沸点(℃) |
冰乙酸 | 1.05 | 易溶 | 118.1 |
正丁醇 | 0.80 | 微溶 | 117.2 |
正丁醚 | 0.77 | 不溶 | 142.0 |
乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
已知:乙酸正丁酯、正丁醇和水组成三元共沸物恒沸点为90.7℃。
合成:
方案甲:采用装置甲(分水器预先加入水,使水面略低于分水器的支管口),在干燥的50mL圆底烧瓶中,加入11.5mL(0.125mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸和2g沸石,摇匀。按下图安装好带分水器的回流反应装置,通冷却水,圆底烧瓶在电热套上加热煮沸。在反应过程中,通过分水器下部的旋塞分出生成的水(注意保持分水器中水层液面仍保持原来高度,使油层尽量回到圆底烧瓶中)。反应基本完成后,停止加热。
方案乙:采用装置乙,加料方式与方案甲相同。加热回流,反应60min后停止加热。

提纯:甲乙两方案均采用蒸馏方法。操作如下:

请回答:
(1)a处水流方向是 (填“进水”或“出水”),仪器b的名称 。
(2)合成步骤中,方案甲监控酯化反应已基本完成的标志是 。
(3)提纯过程中,步骤②是为了除去有机层中残留的酸,检验有机层已呈中性的操作是 ;步骤③的目的是 。
(4)下列有关洗涤过程中分液漏斗的使用正确的是 。
A.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
B.洗涤时振摇放气操作应如图所示
C.放出下层液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
D.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中

(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是 ;若按图丁放置温度计,则收集到的产品馏分中还含有 。
(6)实验结果表明方案甲的产率较高,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。
如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e-=2O2-)。

(1)d电极的名称为___________,d电极上的电极反应式为____________________
(2)如图2所示用惰性电极电解100 mL 0.5 mol·L-1 AgNO3溶液,a电极上的电极反应式为___________,若a电极产生560mL(标准状况)气体,则所得溶液的C(H+)=___________(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入_________(填序号)其物质的量为_______mol
a Ag2O b.AgOH c.AgNO3 d.Ag2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用N2和H2可以实现NH3的工业和成,而氨又可以进一步制备硝酸。已知:
①N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
②N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
③2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
氨催化氧化完全生成一氧化氮气体和水蒸气的热化学方程式为 。
(2)研究在其他条件不变时,改变起始物氢气的物质的量对N2(g)+3H2(g)![]() 2NH3(g)反应的影响实验结果如图所示(图中T表示温度,n表示物质的量):
2NH3(g)反应的影响实验结果如图所示(图中T表示温度,n表示物质的量):

图像中T2和T1的关系是:T2 T1(填“高于”“低于”“等于”“无法确定”)。
a、b、c三点中,N2转化率最高的是 (填字母)。
若容器容积为1L,T2℃在起始体系中加入1molN2,n(H2)=3mol,经过5min反应达到平衡时H2的转化率为60%,则v(NH3)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3molP和2.5molQ置于密闭容器中,发生如下反应:3P(g)+Q(g)![]() xM(g)+2N(g),5min后达到平衡生成1molN,经测定M的平均速率是0.1mol/(L·min),下列叙述不正确的是
xM(g)+2N(g),5min后达到平衡生成1molN,经测定M的平均速率是0.1mol/(L·min),下列叙述不正确的是
A.P的平均反应速率为0.15mol/(L·min)
B.Q的平衡浓度为1mol/L
C.Q的转化率为25%
D.x等于2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 地球上的生命是在氧元素的基础上建立的
B. 大量元素是指含量占生物体总重量千分之一以上的元素
C. 微量元素在生物体含量很少,是生物体所非必需的元素
D. 自然界中的生物和非生物都是由化学元素组成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质之间的化学反应,反应产物一定为纯净物的是( )
A.CH3—CH===CH—CH3+Br2 (CCl4) →
B.CH2===CH—CH2—CH3+HCl![]()
C.CH3—CH===CH2+H2O ![]()
D.CH3CH3+Cl2![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com