
【题目】实验室用MnO2和浓盐酸制氯气的反应为MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g纯MnO2被还原,那么:
MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g纯MnO2被还原,那么:
(1)被氧化的氯化氢的质量为________________________________________________。
(2)转移电子的物质的量为________________________________________________。
(3)纺织工业中常用氯气作漂白剂,漂白布匹后,过量的氯需要除去,通常可用Na2SO3作“脱氯剂”,脱氯后的产物为Na2SO4,氯变为-1价。若把本题中产生的Cl2完全转化,需要Na2SO3的质量为_________。
【答案】14.6 g 0.4 mol 25.2 g
【解析】
(1)消耗二氧化锰的物质的量是17.4g÷87g/mol=0.2mol,则根据方程式可知
MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑ 被氧化HCl
MnCl2+2H2O+Cl2↑ 被氧化HCl
1mol 2mol
0.2mol 0.4mol
所以被氧化的氯化氢的质量为0.4mol×36.5g/mol=14.6g;
(2)反应中氯元素化合价从-1价升高到0价,失去1个电子,这说明每氧化1mol氯化氢转移1mol电子,所以转移电子的物质的量为0.4mol;
(3)被氧化的氯化氢的物质的量是0.4mol,生成氯气是0.2mol。氯气与亚硫酸钠反应生成硫酸钠和氯化钠,反应中亚硫酸钠中的S化合价升高,氯气中Cl化合价降低,设需要Na2SO3的物质的量是x,根据电子守恒可知x×(6-4)=0.2mol×2×(1-0),解得x=0.2mol,因此需要Na2SO3的质量是0.2mol×126g/mol=25.2g。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12。
(1)该温度下,水的离子积常数Kw=________________。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=_________,此时该溶液中由水电离的c(OH-)=____________。
(3)该温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了强化安全管理,某油库引进了一台空气中汽油含量的测量仪,其工作原理如图所示 (用强酸性溶液作电解质溶液)。下列说法中不正确的是
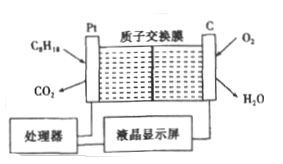
A. 石量电极作正极,电极表面有物质被还原
B. 铂电极的电极反应式为: C8H18+16H2O-50e-=8CO2+50H+
C. H+由质子交换膜左侧向右侧迁移
D. 标况下每消耗5.6 L O2电路中通过1mol 电子,经过电解质形成闭合回路
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 硫酸铁中加入少量氨水:Fe3++3OH-=Fe(OH)3↓
B. 电解饱和食盐水:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C. 碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O
D. 将铝投入CuSO4溶液中:Al+Cu2+=Cu+Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。回答下列问题:
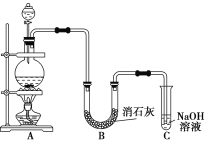
(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,写出反应的化学方程式并用双线桥法表示出反应中电子转移的方向和数目_____________________;若在标准状况下收集到22.4 L氯气,则被氧化的HCl的物质的量是______。
(2)漂白粉将在U形管中产生,其化学方程式是______________。
(3)C装置的作用是_______________________________________。
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是______________________________________________________________。
②试判断另一个副反应__________________________________(用化学方程式表示)。为避免此副反应的发生,可将装置做何改进________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断中一定正确的是( )
A. NaCl及Na2O2固体中阴、阳离子数之比均为1:1
B. 等质量的O2与O3中,氧原子的个数比为3:2
C. 分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:2
D. 10 mL 0.3 mol·L-1 NaCl溶液与30 mL 0.1 mol·L-1 AlCl3溶液中Cl -物质的量浓度比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如右图所示。据图判断正确的是
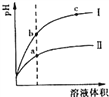
A. Ⅱ为盐酸稀释时的pH值变化曲线
B. b点溶液的导电性比c点溶液的导电性强
C. a点KW的数值比c点KW的数值大
D. b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com