
下列反应类型中,一定不属于氧化还原反应的是( )
|
| A. | 化合反应 | B. | 置换反应 | C. | 分解反应 | D. | 复分解反应 |
| 氧化还原反应.. | |
| 专题: | 氧化还原反应专题. |
| 分析: | 根据有元素化合价变化的反应为氧化还原反应来分析解答. |
| 解答: | 解:A、没有单质参加的化合反应,没有元素的化合价变化,则不属于氧化还原反应,但有单质参加的化合反应,存在元素的化合价变化,则属于氧化还原反应,故A不选; B、置换反应中一定存在元素的化合价变化,则一定属于氧化还原反应,故B不选; C、没有单质生成的分解反应,没有元素的化合价变化,则不属于氧化还原反应,但有单质生成的分解反应,存在元素的化合价变化,则属于氧化还原反应,故C不选; D、复分解反应中一定没有元素的化合价变化,则一定不属于氧化还原反应,故D选; 故选D. |
| 点评: | 本题考查四种基本反应类型与氧化还原反应的关系,明确反应中是否存在元素的化合价变化是解答本题的关键,较简单. |


科目:高中化学 来源: 题型:
有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
| 实验 装置 |
|
|
|
|
| 部分实 验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物在生产和生活中有着广泛的应用。
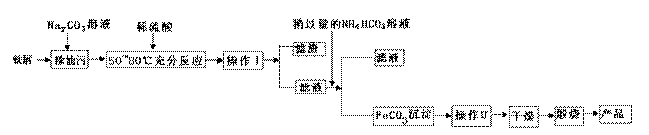
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:回答下列问题:
①操作Ⅰ、Ⅱ的名称分别是____ 、____。
②写出在空气中煅烧FeCO3的化学方程式 ;
③.煅烧如果不充分,产品中将有Fe2+ 存在,试设计实验检验产品中有无Fe2+ 。
(2)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定。
a. 称取2.850g绿矾(FeSO4·7H2O)产品,配成250mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①写出酸性KMnO4溶液与FeSO4 溶液反应的离子方程式
②计算上述样品中FeSO4·7H2O的质量分数为 [ 已知M(FeSO4·7H2O)=278g/mol]
③滴定达到终点时锥形瓶中溶液颜色变化为
④下列操作会导致样品中FeSO4·7H2O的质量分数的测定结果偏高的有_____________。
a.未干燥锥形瓶
b.盛装标准液的滴定管没有用标准液润洗
c. 滴定结束时仰视刻度线读数
d.量取待测液的滴定管没有润洗
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为
A. A﹥B﹥E﹥D B. A﹥B﹥D﹥E C. D﹥E﹥A﹥B D. D﹥A﹥B﹥E
查看答案和解析>>
科目:高中化学 来源: 题型:
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液c ;
A、B是两块电极板,通过导线与直流电相连。请回答以下问题:
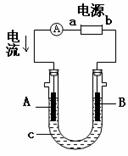 (1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
① B是 极(填“阴”或“阳”), B极逸出
(填:黄绿或无色)气体,同时B极附近溶液呈 色。
② 电解池中A极上的电极反应式为 。
B极上的电极反应式为 。
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
① A电极的材料是 ,电极反应式是 。
② B电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
③下列说法正确的是________。
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液。若阴极析出Cu的质量为12.8 g ,则阳极上产生的气体在标准状况下的体积为 L 。
(4)利用反应2Cu+O2+2H2SO4===2CuSO4+2H2O可制备CuSO4,若将该反应设计为电解池,其电解质溶液需用 ,阳极材料是用 ,阴极电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作中正确的是( )
|
| A. | 用25 mL量筒量取4.0 mol/L的盐酸5.62 mL |
|
| B. | 用托盘天平称取5.57 g KCl固体 |
|
| C. | 配制450 mL 0.2 mol/L H2SO4溶液时应选用500 mL容量瓶 |
|
| D. | 容量瓶使用前需检查是否漏水,具体操作是向容量瓶中注入适量水,盖好瓶塞,用食指压住瓶塞,将瓶底向上并摇晃几下,如无水洒出则说明该容量瓶一定不漏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在指定的条件下,下列各组离子能大量共存的是( )
A.使甲基橙变红的溶液中:Fe2+、Na+、I-、NH4+
B.强碱性溶液中:K+、Na+、ClO-、S2-
C.0.1 mol·L-1 NaAlO2溶液中:H+、Na+、Cl-、SO42-
D.由H2O电离出的c(H+)=10-11mol/L溶液中:Na+、HCO3-、AlO2-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g) 2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是
① 容器中气体的密度不再发生变化 ② X、Y、Z的浓度不再发生变化
③ 容器中的压强不再发生变化 ④ 单位时间内生成2n mol Z,同时消耗2n mol Y
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com