
����Ŀ�������ѣ�DME������Ϊ��21���͵����ȼ�������ɺϳ����Ʊ������ѵ���Ҫԭ�����£�
��CO(g)+2H2(g)![]() CH3OH(g) ��H 1=��90.7 kJ��mol-1 K1
CH3OH(g) ��H 1=��90.7 kJ��mol-1 K1
��2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ��H 2=��23.5 kJ��mol-1 K2
CH3OCH3(g)+H2O(g) ��H 2=��23.5 kJ��mol-1 K2
��CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H 3=��41.2kJ��mol-1 K3
CO2(g)+H2(g) ��H 3=��41.2kJ��mol-1 K3
�ش��������⣺
��1����Ӧ3H2(g)��3CO(g)![]() CH3OCH3(g)��CO2(g)����H��____kJ��mol-1���÷�Ӧ��ƽ�ⳣ��K=____����K1��K2��K3��ʾ��
CH3OCH3(g)��CO2(g)����H��____kJ��mol-1���÷�Ӧ��ƽ�ⳣ��K=____����K1��K2��K3��ʾ��
��2�����д�ʩ�У������CH3OCH3���ʵ���____��
A��ʹ�ù�����CO B�������¶� C������ѹǿ
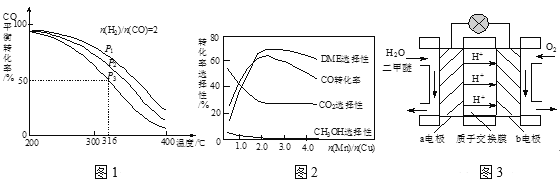
��3�����ϳ�����n(H2)/n(CO)=2ͨ��1 L�ķ�Ӧ���У�һ�������·�����Ӧ��4H2(g)+2CO(g)![]() CH3OCH3(g)+H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ1��ʾ������˵����ȷ����____��
CH3OCH3(g)+H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ1��ʾ������˵����ȷ����____��
A����H <0
B��P1>P2>P3:
C������P3��316��ʱ����ʼʱn(H2)/n(CO)=3����ﵽƽ��ʱ��COת����С��50��
��4������һ�����͵Ĵ�������Ҫ�ɷ���Cu-Mn�ĺϽ𣩣�����CO��H2�Ʊ������ѡ��۲�ͼ2�ش����⡣������n(Mn)/n(Cu)ԼΪ____ʱ�������ڶ����ѵĺϳɡ�
��5��ͼ3Ϊ��ɫ��Դ��������ȼ�ϵ�����Ĺ���ԭ��ʾ��ͼ��a�缫�ĵ缫��ӦʽΪ_____��
���𰸡�-246.1 K12��K2��K3 AC AB 2.0(2-3֮�伴��) CH3OCH3+3H2O-12e-=2CO2��+12H+
��������
(1)�����Ȼ�ѧ����ʽ��˹���ɼ���õ������ݻ�ѧƽ�ⳣ�������Ϸ�Ӧ��ѧ����ʽ��дƽ�ⳣ�������ƽ�ⳣ������ʽ����õ�ƽ�ⳣ����ϵ��
(2)���CH3OCH3���ʣ���ƽ�������ƶ�������Ӱ��ƽ������ط�����
(4)A�������¶ȶ�CO��ת���ʵ�Ӱ�������
B���÷�Ӧ������Ϊ�����С�ķ�����ѹǿ��COת���ʵ�Ӱ�������
C������P3��316��ʱ����ʼʱ![]() =3��������������������
=3��������������������
(5)����ͼ�����ɶ����ѵ����ֵ������
(6)���������£�������ʧ�������ɶ�����̼��
(1)��֪��CO(g)+2H2(g)![]() CH3OH( g)��H1=-90.7kJmol-1��K1=
CH3OH( g)��H1=-90.7kJmol-1��K1=![]() ����2CH30H(g)
����2CH30H(g)![]() CH30CH3(g)+H2O(g)��H2=-23.5kJmol-1��K2=
CH30CH3(g)+H2O(g)��H2=-23.5kJmol-1��K2=![]() ����CO(g)+H2O(g)
����CO(g)+H2O(g)![]() CO2(g)+H2(g)��H3=-41.2kJmol-1��K3=
CO2(g)+H2(g)��H3=-41.2kJmol-1��K3=![]() �����ݸ�˹���ɣ�����2+��+�۵�3CO(g)+3H2(g)
�����ݸ�˹���ɣ�����2+��+�۵�3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g)��H=-246.1kJmol-1��ƽ�ⳣ��K=
CH3OCH3(g)+CO2(g)��H=-246.1kJmol-1��ƽ�ⳣ��K=![]() = K12��K2��K3��
= K12��K2��K3��
(2)A������Ӧ���Ũ��ƽ�����ƣ�����ʹ�ù�����CO�������CH3OCH3���ʣ���A��ȷ��
B���÷�ӦΪ���ȷ�Ӧ�������¶�ƽ�����ƣ���CH3OCH3���ʻή�ͣ���B����
C���÷�Ӧ������Ϊ�����С�ķ�����������ѹǿƽ�����ƣ������CH3OCH3���ʣ���C��ȷ��
�ʴ�ΪAC��
(4)A����ͼ��֪���¶����ߣ�CO��ת���ʽ��ͣ�˵�������¶�ƽ�����ƣ���������Ϊ���ȷ�Ӧ������H��0����A��ȷ��
B���÷�Ӧ������Ϊ�����С�ķ�������ѹǿCO��ת������������P1��P2��P3����B��ȷ��
C������P3��316��ʱ����ʼʱ![]() =3������������������������������Ũ�ȣ�ƽ�����ƣ�CO��ת������������COת���ʴ���50%����C����
=3������������������������������Ũ�ȣ�ƽ�����ƣ�CO��ת������������COת���ʴ���50%����C����
�ʴ�ΪAB��
(5)��ͼ��֪��������![]() ԼΪ2ʱ��CO��ת����������ɶ����ѵ���ࣻ
ԼΪ2ʱ��CO��ת����������ɶ����ѵ���ࣻ
(6)���������£��������ڸ���ʧ�������ɶ�����̼����缫��ӦʽΪ��CH3OCH3-12e-+3H2O=2CO2��+12H+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ���ھ�����ˮ������Cr2O![]() ���ӣ���ͬʱ�ܻ����Դ��õ��м�ֵ�Ļ�ѧ��Ʒ��ͼΪ�乤��ԭ��������˵����ȷ���ǣ� ��
���ӣ���ͬʱ�ܻ����Դ��õ��м�ֵ�Ļ�ѧ��Ʒ��ͼΪ�乤��ԭ��������˵����ȷ���ǣ� ��
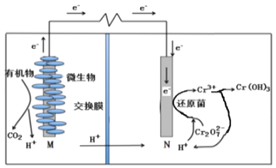
A.MΪ��Դ�������л��ﱻ��ԭ
B.��ع���ʱ��N��������ҺpH��С
C.����1molCr2O![]() ʱ��14molH+�ӽ���Ĥ������Ҳ�Ǩ��
ʱ��14molH+�ӽ���Ĥ������Ҳ�Ǩ��
D.Cr2O![]() ����Ũ�Ƚϴ�ʱ�����ܻ���ɻ�ԭ��ʧ��
����Ũ�Ƚϴ�ʱ�����ܻ���ɻ�ԭ��ʧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������G�Ǻϳɽ�ѹҩ����ɳ̹����Ҫ�м��壬���˹��ϳ�·�����£�
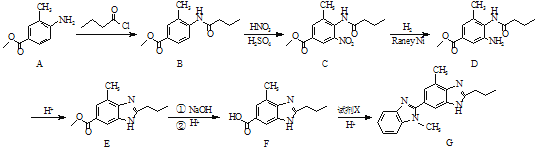
��1��C�к��������ŵ�����Ϊ��������_______��________��
��2��A��B�ķ�Ӧ����Ϊ______��
��3���Լ�X�ķ���ʽΪC7H10N2��д��X�Ľṹ��ʽ��________��
��4��A��һ��ͬ���칹��ͬʱ��������������д����ͬ���칹��Ľṹ��ʽ��______��
������-�����
�ڱ�������3�ֲ�ͬ��ѧ��������ԭ�ӡ�
��5����֪���ٱ�����![]() ���л�ԭ�ԣ��ױ�������
���л�ԭ�ԣ��ױ�������
��������ֱ����������Ϊ���������
��![]()
![]() CH3COO-+CH3NH2
CH3COO-+CH3NH2
���![]() ��
��![]() Ϊԭ���Ʊ�
Ϊԭ���Ʊ�![]() �ĺϳ�·������ͼ�����Լ����ã��ϳ�·������ͼʾ����������ɣ���______________________________
�ĺϳ�·������ͼ�����Լ����ã��ϳ�·������ͼʾ����������ɣ���______________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������£�һ�ݻ�������ܱ��������������������Ļ�����壬��ȼǡ����ȫ��Ӧ�ָ���ԭ״̬��ѹǿ��Ϊԭ����![]() ������ԭ������������������������________��
������ԭ������������������������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ijЩ�����������ڸ����µ��û���Ӧ��Ϊ�����ȷ�Ӧ�������磺4Al+3MnO2![]() 2Al2O3+3Mn�������й�˵���������
2Al2O3+3Mn�������й�˵���������
A.�÷�ӦΪ�û���Ӧ
B.��Ӧ��������ΪMnO2����������ΪMn
C.�ӷ�Ӧ���ԱȽϻ�ԭ�ԣ�Alǿ��Mn
D.��Ӧ������1mol Al2O3ʱ��ת�Ƶĵ�����Ϊ6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ��֤��SO2��Cl2��Ư���ԣ����������ͼ��ʾ��ʵ��װ�ã�
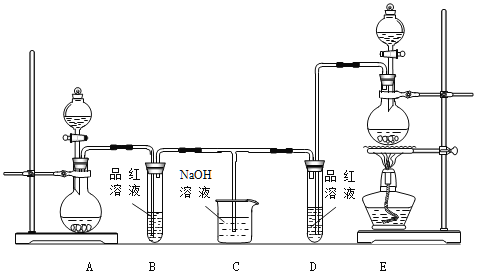
��1�������Ʊ�Cl2���ݵ�ԭ���ǣ�MnO2 + 4HCl��Ũ��![]() MnCl2 + 2H2O + Cl2����Ӧѡ����ͼA��Eװ���е� �����������Cl2����Ӧ��Ũ���������ֳ��������� �� ��
MnCl2 + 2H2O + Cl2����Ӧѡ����ͼA��Eװ���е� �����������Cl2����Ӧ��Ũ���������ֳ��������� �� ��
��2����Ӧ��ʼ����B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ����B��D�����Թ��е�Һ����ȣ�B�Թ��е������� ��
��3��NaOH��Һ�ֱ����������巴Ӧ�����ӷ���ʽ�� �� ��
��4����С��ͬѧ�����������Ϻ�ͨ��Ʒ����Һ��һ��ʱ���Ʒ����Һ��������ɫ���������ϵ�֪���������尴�����1:1��ϣ�����ˮ��Ӧ���������ֳ������ᣬ���ʧȥƯ�����ã��÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2.0 mol��L��1 CuSO4��1.0 mol��L1 H2SO4��Һ��������(�����Ϻ����Һ��������ڻ��ǰ������Һ�����֮��)���㣺
(1)�����Һ��CuSO4��H2SO4�����ʵ���Ũ��c(CuSO4)=________��c(H2SO4)=________��
(2)���Һ��H+��SO42�������ʵ���Ũ��c(H+)=________��c(SO42��)=________��
(3)����Һ�м������ۣ������㹻����ʱ�䣬������ʣ�ࡣ��ʱ��Һ�е����ʵ���Ũ��c(Fe2+)=________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ����仯�����˵��������ȷ����
A.�����������ͷ�Ӧ��������ըҩ��������
B.�ȼҵ�п����ð�����������ܵ��Ƿ�й©
C.��ҵ���Ʊ�����������NH3��O2��Ӧ����NO����һ��ת��ΪNO2��HNO3
D.Ϊ�����������֣��������̬��������Է��ϻ��ʹ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ2H2(g)+CO(g)![]() CH3OH(g)��ƽ�ⳣ�����±���������ͬ�����ʵ���Ͷ�ϣ�
CH3OH(g)��ƽ�ⳣ�����±���������ͬ�����ʵ���Ͷ�ϣ�
���CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ��ʾ�����д�С�Ƚ���ȷ����
ƽ�ⳣ�� | �¶�/�� | ||
500 | 700 | 800 | |
K | 2.50 | 0.34 | 0.15 |
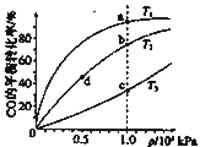
A.ƽ�᳣����K(a)��K(c)��K(b)=K(d)
B.����Ӧ���ʣ�v(a)��v(c)��v(b)=v(d)
C.�ﵽƽ������ʱ�䣺t(a)=t(c)��t(b)��t(d)
D.ƽ����Է���������M(a)=M(c)��M(b)��M(d)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com