
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
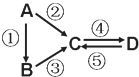
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_______________________________________;④反应离子方程式__________________________________________________。
(2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_________________________________。④反应的离子方程式_________________________。D中加入氢氧化钠的现象_____________________。
(3)若A是太阳能电池用的光伏材料,B常用于制作高档光学器材,C、D为钠盐,C的水溶液俗称水玻璃,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式___________________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为___________________________________________。
【答案】2Al+2OH-+2H2O=2AlO2-+3H2↑ AlO2-+CO2(过量)+2H2O=Al(OH)3↓+HCO3- 3Fe+4H2O(g)![]() Fe3O4+4H2 Fe+2Fe3+=3Fe2+ 生成的白色沉淀迅速变成灰绿色,最后变成红褐色 SiO2+2NaOH=Na2SiO3+H2O SiO2+Na2CO3
Fe3O4+4H2 Fe+2Fe3+=3Fe2+ 生成的白色沉淀迅速变成灰绿色,最后变成红褐色 SiO2+2NaOH=Na2SiO3+H2O SiO2+Na2CO3![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑
【解析】
(1)D物质具有两性,则其为Al2O3或Al(OH)3,因为A是单质,所以A为Al。由②③反应均要用强碱溶液,推知C为NaAlO2,④反应是通入过量的一种引起温室效应的主要气体,则D为Al(OH)3,B为Al2O3。②反应为Al与NaOH溶液反应,生成偏铝酸钠和氢气;④反应为NaAlO2与CO2、H2O等反应,生成Al(OH)3和NaHCO3。
(2)A是应用最广泛的金属Fe,黄绿色气体单质为Cl2,由反应②,可确定C为FeCl3,④反应用到Fe,则D为FeCl2,⑤反应为FeCl2与Cl2的反应。Fe与水高温下反应,生成Fe3O4和H2。④反应为FeCl3与Fe反应,生成FeCl2。FeCl3中加入氢氧化钠,发生复分解反应,生成的Fe(OH)2在空气中逐渐被氧化为Fe(OH)3。
(3)若A是太阳能电池用的光伏材料,则其为Si,B常用于制作高档光学器材,则其为SiO2,C、D为钠盐,C的水溶液俗称水玻璃,则C为Na2SiO3。④反应也是通入一种引起温室效应的主要气体,D的溶液显碱性,则其为Na2CO3。③反应为SiO2与NaOH溶液反应,生成Na2SiO3和水。⑤反应用到B,反应条件为高温,则⑤为SiO2与Na2CO3反应,生成Na2SiO3和CO2气体。
(1)由分析可知,A为Al,B为Al2O3,C为NaAlO2,D为Al(OH)3;反应②为Al与NaOH溶液反应,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑;反应④为NaAlO2与CO2、H2O等反应,离子方程式为AlO2-+CO2(过量)+2H2O=Al(OH)3↓+HCO3-;答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;AlO2-+CO2(过量)+2H2O=Al(OH)3↓+HCO3-;
(2)由分析知,A为Fe,黄绿色气体为Cl2,C为FeCl3,D为FeCl2;Fe与水高温下反应,化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;反应④为FeCl3与Fe反应,离子方程式为Fe+2Fe3+=3Fe2+;FeCl3中加入氢氧化钠,发生复分解反应,生成的Fe(OH)2,在空气中逐渐被氧化为Fe(OH)3,现象为生成的白色沉淀迅速变成灰绿色,最后变成红褐色;答案为:3Fe+4H2O(g)
Fe3O4+4H2;反应④为FeCl3与Fe反应,离子方程式为Fe+2Fe3+=3Fe2+;FeCl3中加入氢氧化钠,发生复分解反应,生成的Fe(OH)2,在空气中逐渐被氧化为Fe(OH)3,现象为生成的白色沉淀迅速变成灰绿色,最后变成红褐色;答案为:3Fe+4H2O(g)![]() Fe3O4+4H2;Fe+2Fe3+=3Fe2+;生成的白色沉淀迅速变成灰绿色,最后变成红褐色;
Fe3O4+4H2;Fe+2Fe3+=3Fe2+;生成的白色沉淀迅速变成灰绿色,最后变成红褐色;
(3)由分析知,A为Si,B为SiO2,C为Na2SiO3,D为Na2CO3;反应③为SiO2与NaOH溶液反应,化学方程式为SiO+2NaOH=Na2SiO3+H2O;反应⑤为SiO2与Na2CO3反应,化学方程式为SiO2+Na2CO3![]() Na2SiO3+CO2↑;答案为:SiO2+2NaOH=Na2SiO3+H2O;SiO2+Na2CO3
Na2SiO3+CO2↑;答案为:SiO2+2NaOH=Na2SiO3+H2O;SiO2+Na2CO3![]() Na2SiO3+CO2↑。
Na2SiO3+CO2↑。


科目:高中化学 来源: 题型:
【题目】H、C、N、O、V(钒)五种元素形成的某分子结构如图所示,下列说法错误是
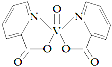
A.N原子核外存在3种不同能量的电子
B.基态V原子的价电子轨道表示式为![]()
C.基态O原子,电子占据的最高能级符号为2p
D.基态C、N两种原子中,核外存在相同对数自旋方向相反的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.标准状况下,22.4 L水中所含的分子数约为6.02×1023个
B.1 mol Cl2中含有的原子数为NA
C.标准状况下,aL氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023个
×6.02×1023个
D.常温常压下,11.2 L CO分子数是0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。一种合成阿魏酸的反应可表示为
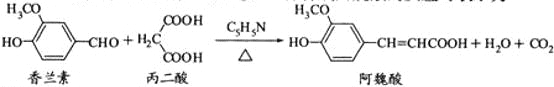
下列说法正确的是
A. 可用酸性![]() 溶液检测上述反应是否有阿魏酸生成
溶液检测上述反应是否有阿魏酸生成
B. 香兰素、阿魏酸均可与![]() 、
、![]() 溶液反应
溶液反应
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D. 与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃在一定条件下发生氧化反应,碳碳双键断裂,如:R1CH=CHR2,被氧化为![]() 和
和![]() ;
;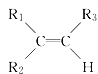 被氧化为
被氧化为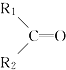 和
和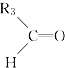 (R1 、R2 、R3 表示烃基或氢原子) 。由此推断分子式为C5H10 的烯烃所有可能的氧化产物有( )
(R1 、R2 、R3 表示烃基或氢原子) 。由此推断分子式为C5H10 的烯烃所有可能的氧化产物有( )
A.5 种B.6 种C.7 种D.8 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H 是合成抗炎药洛萦洛芬钠的关键中间体,它的一种合成路线如下:

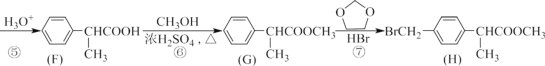
(1)A 的物质名称为_________,H 中非含氧官能团名称是_________。
(2)E 的结构简式为_________,反应⑥的反应类型为_________。
(3)应①的化学方程式为_________,反应⑥的化学方程式为_________。
(4)写出满足下列条件的 F 的同分异构体的结构简式_________。
I.能发生水解反应生成酸和醇
Ⅱ.能发生银镜反应
Ⅲ.核磁共振氢谱有 5 组峰且峰面积之比为 3:2:2:2:1
(5)仿照H 的合成线,设计一种由![]() 合成
合成![]() 的合成路线________。
的合成路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛。在压强为30MPa时,不同温度时合成氨平衡混合气体中NH3的体积分数如下:
温度/℃ | 200 | 300 | 400 | 500 | 600 |
氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
请回答:
(1)根据图中所示,合成氨的热化学方程式为___。
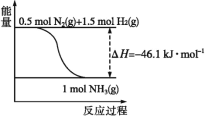
(2)将1molN2(g)和3molH2(g)通入一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量___92.2kJ(填“大于”“等于”或“小于”),原因是___;若加入催化剂,ΔH___(填“变大”“变小”或“不变”)。
(3)已知破坏1molN≡N键、1molH—H键需要吸收的能量分别为946kJ、436kJ,则破坏1molN—H键需要吸收的能量为___kJ。
(4)N2H4可视为NH3分子中的一个H被—NH2取代的产物。发射卫星用N2H4(g)为燃料,以NO2为氧化剂发生反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1。
则1molN2H4与NO2完全反应的热化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将200mL CuSO4和Fe2(SO4)3的混合溶液分成两等份,向其中一份加入足量铁粉,充分反应后测得固体质量保持不变;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干燥、称量,得到23.3g白色沉淀。请计算:
(1)原溶液中c(SO42-) = __________。
(2)原溶液中CuSO4和Fe2(SO4)3的物质的量比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。请回答下列问题:
X | Y | |
Z | W |
(1)元素Z位于周期表中第____周期____族。
(2)X、Y元素氢化物稳定性强弱顺序是____(用化学式表示)。
(3)Y、Z的最高价氧化物对应水化物的酸性强弱顺序是____(用化学式表示)。
(4)原子序数比Y多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是____ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com