
【题目】将氯气通过软管灌到鼠洞里能够灭鼠,这是利用氯气的毒性和 ( )
A.溶解性B.密度大于空气C.黄绿色D.漂白性
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】海水蕴藏着丰富的资源。下列有关海水综合利用的说法中,不正确的是
A.从海水中可提取食盐B.海水蒸馏可得淡水
C.直接电解海水可得镁D.从海水中可提取溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. SiO2、NO、SO2、SO3属于非金属氧化物,又属于酸性氧化物
B. NH3形成铵盐的过程属于氮的固定
C. 纯铁的熔点比生铁低
D. 可以用光洁无锈的铁丝代替铂丝作焰色反应实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下。

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(l)实验室用18.4mol/L的浓硫酸配制225mL4.8mol/L的H2SO4溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要__________________。
(2)酸浸时,为了提高浸取率除了增大酸的浓度外还可采取的措施有______(答出一点即可)。
(3)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式______。
(4)常温下,部分阳离子以氮氧化物形式沉淀时,溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ |
开始沉淀时的pH | 2.7 | — | — |
沉淀完全时的pH | 3.7 | 11.1 | 8 |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-溶液的pH不能超过8,其理由_______。
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液Ⅱ中的金属阳离子是____________。
(6)写出上述流程中用Na2SO3进行还原时发生反应的化学方程式_______,在实验室进行过滤操作时,为了加快过滤速率,可以采取的措施为_________(写一种方法即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2SO3溶液,可再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。下列说法正确的是
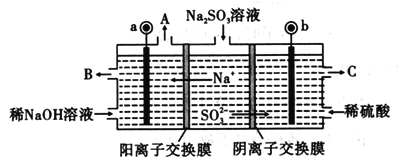
A. 电解过程中若消耗12.6gNa2SO3,则阴极区变化的质量为4.4g (假设该过程中所有液体进出口密闭)
B. b放电的电极反应式为SO32-+H2O-e-= SO42-+2H+
C. 电子由a经内电路流向b电极
D. 图中b极连接电源的正极,C 口流出的物质是亚硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃相对分子质量为86,如果分子中含有3个—CH3、2个—CH2—和1个![]() ,则该结构的烃的一氯取代物最多可能有几种(不考虑立体异构)
,则该结构的烃的一氯取代物最多可能有几种(不考虑立体异构)
A. 9种 B. 6种 C. 5种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾在工业上具有广泛的应用,某研究性学习小组利用如图所示的实验装置制备氯酸钾。回答下列问题:
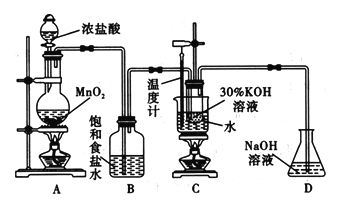
(1)写出装置C中发生反应的离子方程式:_______________________。
(2)若无B装置,则装置C中氯酸钾的产率将___________ (填“提高” “降低”或“无影响”)。
(3)在不同条件下KC1O3可将KI氧化为I2或KIO3。该小组设计了系列实验研究体系中硫酸浓度对反应产物的影响,实验的记录表如下表(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0. 20mol L-1KI/mL | V1 | 1.0 | 1.0 | 1.0 |
KC1O3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0mol L-1H2SO4/mL | 0 | 3.0 | V2 | 9.0 |
蒸馏水 | 9.0 | V3 | 3.0 | 0 |
实验现象 |
①实验设计表中V1=____________; V2 =_____________; V3 =_______________。
②设计1号试管实验的作用是_________________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为__________________。
(4)工业上可用KC1O3与Na2SO3在H2SO4存在下制备高效、低毒的消毒剂C1O2,该反应的化学方程式为______________________ ;利用该反应原理,若工业上使用122.5吨KClO3与足量的Na2SO3反应,生成的ClO2用于除去工业废水中的Mn2+,可得到MnO2固体165吨,则该反应的产率约为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2H、13C、15N、18O、34S等常用作环境分析指示物,下列对它们的说法正确的是( )
A. 34S原子核内的中子数为16 B. 16O与18O互称同位素
C. 13C和15N原子核内的质子数相差2 D. 2H的核外电子数比1H多一个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列运用与碳酸钠或碳酸氢钠能发生水解的事实无关的是
A. 实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞
B. 泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫
C. 厨房中常用碳酸钠溶液洗涤餐具上的油污
D. 可用碳酸钠与醋酸制取少量二氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com