
A、
| ||
| B、9m | ||
| C、2m | ||
| D、18m |
科目:高中化学 来源: 题型:
| A、用湿润的碘化钾淀粉试纸检验氯化氢气体中是否混有氯气 |
| B、次氯酸具有酸性,可与碳酸钠反应产生二氧化碳气体 |
| C、新制氯水的酸性一定比久置的氯水强 |
| D、干燥氯气能使有色布条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg(OH)2和稀盐酸反应 |
| B、Ba(OH)2溶液滴入稀H2SO4中 |
| C、KOH溶液和稀HNO3反应 |
| D、CO2通入Ca(OH)2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
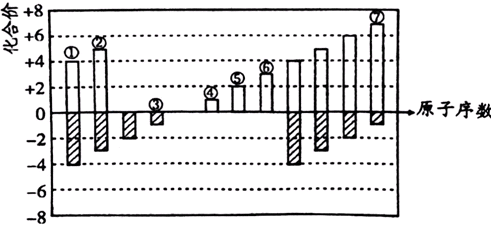
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:Na+>Mg2+>Al3+>Cl-;原子半径:Na>Mg>Al>Cl |
| B、稳定性:HF>H2O>NH3>CH4; 还原性:HF<H2O<NH3<CH4 |
| C、碱性:CsOH>KOH>Mg(OH)2>NaOH; 金属性:Cs>K>Mg>Na |
| D、酸性:HClO>H2SO4>H2CO3;非金属性Cl>S>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,16g CH4含有CH4分子数为NA |
| B、常温常压下,22.4L CO2含有CO2分子数为NA |
| C、1mol Na燃烧生成Na2O2失去的电子数为2NA |
| D、0.5mol?L-1的CuCl2溶液中含Cl-数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 分类组合 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | Na2CO3 | H2SO4 | NaHCO3 | SO2 | CO2 |
| B | NaOH | HCl | NaCl | Na2O | CO |
| C | NaOH | CH3COOH | MgCl2 | Na2O2 | SO2 |
| D | KOH | HNO3 | CaCO3 | CaO | SO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
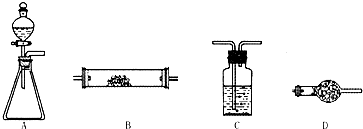
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com