
����Ŀ���ں����ܱ������д�������ƽ�⣺CO(g)+H2O(g)![]() CO2(g)+H2(g)��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶�T�Ĺ�ϵ��ͼ��ʾ������˵���������
CO2(g)+H2(g)��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶�T�Ĺ�ϵ��ͼ��ʾ������˵���������

A. ��ӦCO(g)+H2O(g)![]() CO2(g)+H2(g)����H��0
CO2(g)+H2(g)����H��0
B. ��T2ʱ������Ӧ����״̬D����һ��������������
C. ƽ��״̬A��C��ȣ�ƽ��״̬A��c(CO)С
D. ��T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2
���𰸡�BD
��������
����A��ƽ��״̬A��C��ȣ�C���¶ȸߣ���֪��H��0�������¶�ƽ�����ƣ�COŨ�ȼ�С������A��COŨ�ȴ�A����B��T2ʱ��Ӧ���е�״̬D��c(CO2)����ƽ��Ũ�ȣ��ʷ�Ӧ���淴Ӧ���У���һ������(��)����(��)����B��ȷ��C����ͼ��֪���¶�Խ��ƽ��ʱc(CO2)Խ��˵�������¶�ƽ��������Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ���У�������Ӧ�����ȷ�Ӧ������H��0����C����D���÷�Ӧ����Ӧ�����ȷ�Ӧ�������¶�ƽ��������Ӧ�ƶ�����ѧƽ�ⳣ������K1��K2����D��ȷ����ѡBD��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(Ca3N2)��һ����Ҫ�Ļ����Լ�����ˮ����ˮ�⡣ʵ���ҿ��ɵ����Ƽ����Ƶõ����ƣ�ʵ��װ������ͼ(ʡ�Բ��̶ֹ�װ��)��
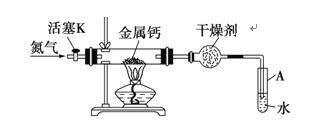
(1)�������������Ļ�ѧ����(�������ۼ����������Ӽ���)_________��
(2)���θ�����еĸ������ѡ��(����дһ��)_________����ϻ�ѧ����ʽ����������_________��
(3)�Ʊ�������ĩ�˵��ܱ���ʼ�ղ����Թ�A��ˮ�У�Ŀ���Ǣٱ��ڹ۲�N2�����٣���_________��
(4)�Ʊ������ƵIJ������裺�ٰ�ͼʾ���Ӻ�ʵ��װ�ã���_________���۴���K��ͨ��N2���ܵ�ȼ�ƾ��ƣ����з�Ӧ���ݷ�Ӧ������Ϩ��ƾ��ƣ�����ͨN2��ʹװ����ȴ�����£����װ�ã�ȡ�����
(5)���������Тۺ͢�_________(������������������)������������_________��
(6)���������Ӱ��ʵ���Ƶ�Ca3N2�Ĵ��ȡ�Ϊ�ⶨ�����ƵĴ��ȣ�ʵ�������ȡһ�����Ĺ�������������ˮ�У���ʹ������ȫ�ݳ����ռ������干6.72 L(�����㵽��״��)����������ͨ��װ����������CuO��Ӳ�ʲ������г�ַ�Ӧ�����Ӳ�ʲ������й�����������6.4 g����Ca3N2�Ĵ���Ϊ_________(�ðٷ�����ʾ������һλС��)(ע�������ܱ���������ͭ����������һ�ֶԻ�������Ⱦ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���ܱ��������м���һ��Ħ���������ɻ����ĸ���(��Ȳ���)�������ֳ������֣�����߳���8molN2���ұ߳���CO��CO2�Ļ�����干64gʱ�����崦����ͼλ��(�����¶Ȳ���)��
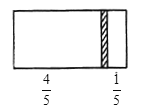
��1���ұ���������ʵ���Ϊ___��
��2���ұ�������CO��CO2������֮��Ϊ__��
��3�����ı��ұ�CO��CO2�ij�������ʹ���崦�ھ����Ҷ�1/3���������¶Ȳ��䣬��ǰ�����γ�����������ڵ�ѹǿ֮��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ�������
A. �����£�4.6gNO2�����к��еķ�����Ϊ0.1NA
B. ���³�ѹ�£�22.4L SO2�к��еķ�����С��NA
C. 0.1mol�����μӷ�Ӧʱת�Ƶĵ�����Ϊ0.2NA
D. �ú���0.1mol FeCl3�ı�����Һ���Ƶ��������������У���������������0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4molA�����2molB������2 L�������л�ϣ�����һ�������·������·�Ӧ��2A(g)+B(g) ![]() 2C(g)������2 s����C��Ũ��Ϊ0.6mol��L-1���������м���˵����
2C(g)������2 s����C��Ũ��Ϊ0.6mol��L-1���������м���˵����
��������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3 mol��L-1��s-1 ��
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol��L-1��s-1��
��2sʱ����A��ת����Ϊ30�� ��
��2sʱ����B��Ũ��Ϊ1.4mol��L��1��
������ȷ���ǣ� ��
A. �٢� B. �٢� C. �ڢ� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����![]() ����ʾ����
����ʾ����![]() ����
����![]()
A. ����ʯ��ˮ��![]() ��Һ��Ӧ B.
��Һ��Ӧ B. ![]() ��
��![]() ��Һ��Ӧ
��Һ��Ӧ
C. NaOH��Һ��![]() ��Һ��Ӧ D.
��Һ��Ӧ D. ![]() ��Һ��HI��Һ��Ӧ
��Һ��HI��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.�����������ᳫ����̼�������������Ƕ�Ӧ��ע��������⡣Ŀǰ��һЩ�����Ѹ�����Ȼ����CNG����ȼ�ϣ��Լ��ٶԿ�����Ⱦ����֪��16g������ȫȼ������Һѹ̬ˮ�ų�890kJ����,1mol̼��ȫȼ�����ɶ�����̼�ų�393.5kJ������ͨ������Ƚϣ���д���б���ȷ��0.01����
��������1g | ȼ�շų�������/kJ | ����CO2������/g |
̼ | 32.80 | _________ |
���� | _________ | 2.75 |
���ݱ����е����ݣ���Ȼ����ú��ȣ�����Ȼ����ȼ�ϵ��ŵ��� ____________��
II.���Ϲ�����仯�����2009��12��7��18���ڸ籾�����ٿ����й�������ŵ��2020�꣬��λGDP������̼�ŷű�2005���½�40%��45%��
(1)��CO2�������ϳ�CH3OCH3(�� �� )�ǽ����ԴΣ�����о�����֮һ��
��֪��CO(g)+2H2(g)= CH3OH(g) ��H1 = -90.7kJ��mol��1
2CH3OH(g)= CH3OCH3(g)+H2O(g) ��H2 = -23.5kJ��mol��1
CO(g)+H2O(g)= CO2(g)+H2(g) ��H3= -41.2kJ��mol��1
��CO2�������ϳ�CH3OCH3(g)���Ȼ�ѧ����ʽΪ��_____________________________ ��
(2)�����£�һ����̶����ܱ������д��ڷ�ӦCO(g)+H2O(g) ![]() CO2(g)+H2(g) ��H<0��������CO��Ũ�ȣ���˷�Ӧ���ʱ�___________������������������С����������������
CO2(g)+H2(g) ��H<0��������CO��Ũ�ȣ���˷�Ӧ���ʱ�___________������������������С����������������
(3)�ڴ�����һ���¶ȡ�ѹǿ�����£�CO��H2�ɷ�Ӧ���� �״���CO(g)��2H2(g)![]() CH3OH(g)�� CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ����p1_______________ p2 ������>���� ��<������ = ��,��ͬ�����÷�Ӧ����H___________0��
CH3OH(g)�� CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ����p1_______________ p2 ������>���� ��<������ = ��,��ͬ�����÷�Ӧ����H___________0��

(4)��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ѧ���ļ������γ�(���)1mol��ѧ��ʱ�ͷ�(������)����������֪����P4O6�ķ��ӽṹ��ͼ��ʾ,���ṩ���»�ѧ���ļ��ܣ�E(P-P)=akJ��mol-1��E(P-O)=bkJ��mol-1��E(O=O)=ckJ��mol-1����ӦP4(����)ȼ������P4O6���Ȼ�ѧ����ʽΪ(��Ӧ����a��b��c��ʾ)��_____________________��
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��80 ��ʱ��2 L�ܱ������г���0.40 mol N2O4��������ӦN2O4(g)![]() 2NO2(g)����H����53 kJ/mol������������ݡ������ж���ȷ����
2NO2(g)����H����53 kJ/mol������������ݡ������ж���ȷ����
ʱ��/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol��L��1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
A. �����¶ȸ÷�Ӧ��ƽ�ⳣ��K��С
B. �÷�Ӧ�� ��S <0
C. ��Ӧ��ƽ��ʱ����15.9 kJ
D. 100 sʱ��ͨ��0.40 mol N2O4������ƽ��ʱN2O4�����������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�������������Ͷ����������γ�����ʱ������еİ��й�(��ͼ��ʾ)������������ȷ����

A. ͼ���漰�����ʶ��ǵ����
B. SO2��SO3�Ĺ��������ȹ���
C. ͼ���漰������������һ�������¾�����������
D. ������ͼ���������ˮ�ķ�Ӧ������Ƴ�ԭ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com