
【题目】下列说法正确的是( )
A. 葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体
B. 淀粉、纤维素和油脂都属于天然高分子化合物
C. 油脂、淀粉、蔗糖和葡萄糖在一定条件下都能发生水解反应
D. 肌醇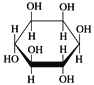 与葡萄糖
与葡萄糖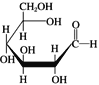 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此均属于糖类化合物
的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此均属于糖类化合物
【答案】A
【解析】
A.葡萄糖、果糖的分子式均为C6H12O6,结构不同,二者互为同分异构体,A正确;
B.淀粉、纤维素属于天然高分子化合物,油脂是高级脂肪酸甘油酯,是油和酯的统称,油是不饱和高级脂肪酸甘油酯,脂肪是饱和高级脂肪酸甘油酯,油脂式量小,不是高分子化合物,B错误;
C.油脂水解的最终产物是高级脂肪酸和丙三醇;淀粉水解最终产物是葡萄糖;蔗糖水解生成葡萄糖和果糖,葡萄糖是单糖,不能水解,C错误;
D.肌醇分子式为C6H12O6,葡萄糖分子式为C6H12O6,肌醇和葡萄糖的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,但因糖类是多羟基醛或多羟基酮及其缩聚物和某些衍生物的总称,所以肌醇不属于糖类化合物,D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】有机物D的结构简式:![]() ,学名肉桂酸,又名β-苯丙烯酸,主要用于香精香料、食品添加剂、医药工业、美容、农药、有机合成等方面,其合成路线(部分反应条件略去)如下所示:
,学名肉桂酸,又名β-苯丙烯酸,主要用于香精香料、食品添加剂、医药工业、美容、农药、有机合成等方面,其合成路线(部分反应条件略去)如下所示:
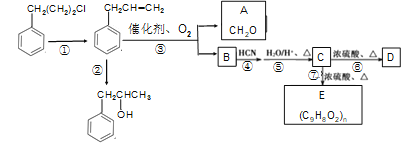
已知: ⅰ CH3CH=CH2![]() CH3CHO + HCHO;
CH3CHO + HCHO;
ⅱ RCHO![]()
![]()
![]()
![]()
完成下列填空:
(1)C中含氧官能团名称是___________________,E的结构简式为____________________。
(2)反应②的反应类型是_________________,A的名称是__________________。
(3)反应①发生所需的试剂是____________________________________。反应⑥的化学方程式为___________________________________________________。
(4)D的分子式是_______________________,与D具有相同官能团的同分异构体有多种,
其中一种的结构简式为______________________。
(5)设计一条以溴乙烷为原料合成乳酸(![]() )的路线(其它试剂任选,合成路线常用的表示方式为:
)的路线(其它试剂任选,合成路线常用的表示方式为:![]() )。___________________________________________。
)。___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究碳、硅元素的非金属性的相对强弱,根据要求完成下列各小题
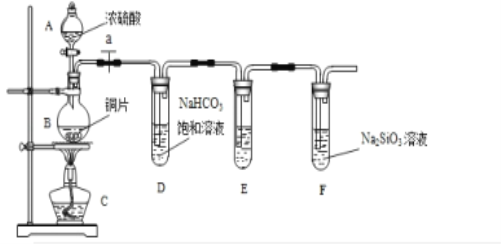
(1)实验装置: 填写所示仪器名称A__________ B___________.
(2)实验步骤:连接仪器、____________、加药品后,打开a、然后滴入浓硫酸,加热.
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是___________________.装置E中足量酸性KMnO4溶液的作用是_______________;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是___________ ;
③试管D中发生反应的离子方程式是_____________________________________.
④若将铜片改为木炭,其它药品不变,也可以对该实验目的进行探究,请写出在该实验中木炭与浓硫酸反应的化学方程式_________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白。
主族\周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为___。
(2)④与⑤两种元素相比较,原子半径较大的是___(填元素符号);在非金属元素的最高价氧化物所对应的水化物中,酸性最强的化合物是___(填化学式)。在金属元素氧化物所对应的水化物中,碱性最强的化合物是___(填化学式),具有两性的化合物是___(填化学式)。
(3)④,⑤,⑥,⑦四种元素形成的简单离子,半径由大到小的顺序为___(填化学式)。
(4)元素①和元素⑦形成化合物属于___化合物(填“离子”或者“共价”)。请用电子式表示⑥和④组成化合物的形成过程:________。
(5)由②和氢元素形成的两种多原子分子,A为10电子结构B为18电子结构,B可由A与次氯酸钠反应制得,该反应的离子方程式为:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
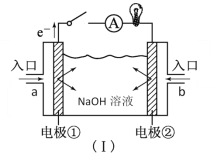
【题目】(1)如图装置(Ⅰ)为以NaOH溶液为电解质溶液的氢氧燃料电池。装置(Ⅰ)中a和b为气体进口,其中a口进入的是(填名称)____,写出电极②发生反应的电极反应式______。
(2)将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图的装置:(以下均假设反应过程中溶液体积不变)。
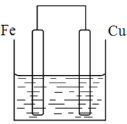
①铁片上的电极反应式为_____。
②溶液中的铜离子移向____(填铁电极或铜电极)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常温下同浓度的强酸、强碱等体积混合后由水电离出的c(H+) =10-7mol·L-l
B. 常温下pH =2的盐酸和pH =12的氨水等体积混合后c(C1-)+c(H+)=c(NH4+)+c(OH-)
C. 常温下0.1 mol.L-1的Na2A溶液的pH=10,则该溶液中由水电离的c(OH-)= 10 -10 mol.L-l
D. 常温下向10 mL0.1 mol.L-1的CH3 COOH溶液中滴加相同浓度的氨水,在滴加过程中,![]() 将减小
将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解的产物,设计如下实验方案:
![]()
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是____________________________________。
(2)试剂2为______________,其作用是__________________,使检验水解产物的实验得以顺利进行。
(3)反应①的化学方程式为__________________________________________________。
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是__________。
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的________(填”能”或”否”),若不能,其原因是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 生成物的总能量大于反应物的总能量时,ΔH<0
B. 在其他条件不变的情况下,使用催化剂可以改变反应的焓变
C. ΔH<0、ΔS >0的反应在低温时不能自发进行
D. 一个化学反应的ΔH只与反应体系的始态和终态有关,而与反应的途径无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示,根据判断出的元素回答问题:
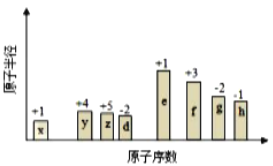
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式____________________。
(4)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如图所示:
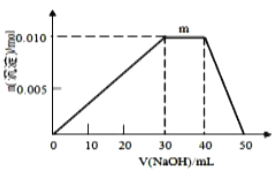
①R中存在的化学键有________________。
②写出m点反应的而离子方程式________________________________。
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后产生沉淀的物质的量为_______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com