
【题目】氢是重要而洁净的能源。要利用氢气作为能源,必须解决好安全有效地储存氢气的问题。镧(La)镍(Ni)合金是一种储氢材料,这种合金的晶体结构已经测定,其基本结构单元如图所示,有关其说法正确的是
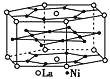
A.不属于金属晶体
B.该合金的化学式为La7Ni12
C.其熔点比组分金属低,硬度比组分金属大
D.设该结构单元的体积为Vcm3,NA为阿伏加德罗常数,合金的摩尔质量为M g/mol。则该合金的密度为ρ= 3![]() g/ cm3
g/ cm3
【答案】CD
【解析】
A.该晶体是由金属形成的合金,属于金属晶体,A项错误;
B.根据其基本结构单元示意图可知,La原子位于结构单元的上下面心,以及12个顶点上,所以该结构单元中含La原子数为12×![]() +2×
+2×![]() =3;Ni原子位于结构单元内部的有6个,位于上下底面的共计12个,位于侧面的共计6个,所以该结构单元中含有Ni的原子数为18×
=3;Ni原子位于结构单元内部的有6个,位于上下底面的共计12个,位于侧面的共计6个,所以该结构单元中含有Ni的原子数为18×![]() +6=15,则La和Ni的原子数比为3:15=1:5,所以该合金的化学式可表示为LaNi5,B项错误;
+6=15,则La和Ni的原子数比为3:15=1:5,所以该合金的化学式可表示为LaNi5,B项错误;
C.合金的熔点比组分金属低,硬度比组分金属大,C项正确;
D.由B选项可知,1个该结构单元中含有LaNi5的个数为3个,所以该合金的密度为ρ= 3![]() g/ cm3,D项正确;
g/ cm3,D项正确;
答案选CD。


科目:高中化学 来源: 题型:
【题目】将质量为mg的铜屑完全溶于适量浓硝酸中,反应后得到NO2、NO的混合气体,将所得气体通入300mL2molL-1NaOH溶液中,恰好完全反应,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为0.2mol,则m的值为( )
A.12.8B.19.2C.25.6D.51.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极下列叙述不正确的是( )

A.a极是负极,该电极上发生氧化反应
B.b极发生的电极反应是O2+4OH--4e-=2H2O
C.电池总反应方程式为2H2+O2=2H2O
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淮南是我国重要的煤炭生产基地,通过煤的气化和液化,能使煤炭得以更广泛的应用。
I.工业上先将煤转化为CO,再利用CO和水蒸气反应制H2时,存在以下平衡:
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
(1)向2L恒容密闭容器中充入CO和H2O(g),800℃时测得部分数据如下表。
t/min | 0 | 1 | 2 | 3 | 4 |
n(H2O)/mol | 1.20 | 1.04 | 0.90 | 0.70 | 0.70 |
n(CO)/mol | 0.80 | 0.64 | 0.50 | 0.30 | 0.30 |
则从反应开始到2min时,用H2表示的反应速率为_________________;该温度下反应的平衡常数K=___________________(小数点后保留1位有效数字)。
(2)相同条件下,向2L恒容密闭容器中充入1molCO、3mol H2O(g)、2molCO2(g)、2mo1 H2(g),此时v正________v逆(填“>” “<” 或 “=”)。
Ⅱ.一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)CH3OH(g)△H=﹣105kJmol﹣1.向体积为2L的密闭容器中充入2mol CO和4mol H2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如右图中Ⅰ、Ⅱ、Ⅲ曲线所示:
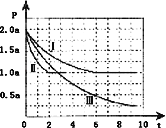
(1)Ⅱ和Ⅰ相比,改变的反应条件是______.
(2)反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=______.
(3)反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=______.
(4)比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1_____T3(填“>”“<”“=”),判断的理由是_________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示![]() 部分产物略去
部分产物略去![]() ,则下列有关物质的推断不正确的是
,则下列有关物质的推断不正确的是![]()
![]()
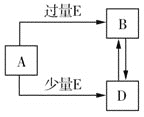
A.若A是碳,则E可能为氧气
B.若A是![]() 溶液,则E可能为HCl
溶液,则E可能为HCl
C.若A是![]() ,E是稀
,E是稀![]() 溶液,则D为
溶液,则D为![]()
D.若A是![]() 溶液,D可能是
溶液,D可能是![]() ,E不可能是氨水
,E不可能是氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院长春应用化学研究所在甲醇(CH3OH)燃料电池方而获得新突破,研制出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示:
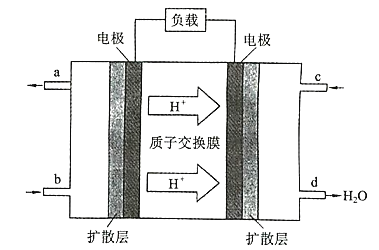
(1)该电池工作时,b处通入的物质为 ______________ ,c 通入 的物质为______。
(2)该电池负极的电极反应式为 _________________ 。
(3)工作一段时间后,当12.8g甲醇完全反应生成 CO2时时,有_________×6.02×1023个电子发生转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g) H=196kJ·moL1,一段时间后达平衡,反应过程中测定的部分数据见下表:
2SO3(g) H=196kJ·moL1,一段时间后达平衡,反应过程中测定的部分数据见下表:
反应时间/min | n(SO2)/mol | n(O2)/mol |
0 | 2 | 1 |
5 | 1.2 | |
10 | 0.4 | |
15 | 0.8 |
下列说法不正确的是
A. 反应在前5min的平均速率为v (SO2)=0.08mol·L1·min1
B. 保持温度不变,向平衡后的容器中再充入0.2molSO2和0.2mol SO3时,v (正)>v (逆)
C. 保持其他条件不变,若起始时向容器中充入2molSO3,达平衡时吸收78.4kJ的热量
D. 相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积均为0.25 L的两个密闭容器中发生反应:X2(g)+3Y2(g) ![]() 2XY3(g) ΔH=-92.6 kJ·mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:
2XY3(g) ΔH=-92.6 kJ·mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:
起始时各物质物质的量/mol | 达平衡时体系能量的变化 | |||
容器 | X2 | Y2 | XY3 | |
容器①恒温恒容 | 1 | 3 | 0 | 放热 23.15 kJ |
容器②恒温恒压 | 1 | 3 | 0 | Q(Q>0) |
下列叙述正确的是( )
A. 容器①、②中反应物X2的转化率相同
B. 达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
C. 容器①、②达到平衡时间相同
D. 容器②, Q大于23.15 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A. 图甲 中的ΔH1>ΔH2
中的ΔH1>ΔH2
B. 图乙 表示可逆反应A(s)+3B(g)2C(g) ΔH>0
表示可逆反应A(s)+3B(g)2C(g) ΔH>0
C. 图丙 表示充满NO2气体的试管,倒置于水槽中,向其中缓慢通入氧气直至试管中全部充满水,假设溶质不扩散,溶质的物质的量浓度与通入氧气的体积关系
表示充满NO2气体的试管,倒置于水槽中,向其中缓慢通入氧气直至试管中全部充满水,假设溶质不扩散,溶质的物质的量浓度与通入氧气的体积关系
D. 由图丁 可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com