
【题目】2015年2月16日李克强总理到东北调研经济情况,重点走访了钢铁厂,鼓励钢铁厂提高钢铁质量和产量,铁及其化合物在日常生活中应用广泛。
(1)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4 H+=4Fe3++2H2O,则另一反应的离子方程式为__________;
(2)氧化铁是重要工业颜料,下面是制备氧化铁的一种方法,其流程如下:

①操作Ⅰ的名称是__________;操作Ⅱ为洗涤,洗涤操作的具体方法为__________;
②滤液A中加入稍过量的NH4HCO3溶液生成沉淀同时有一种气体产生,写出其化学方程式: __________;
(3)如果煅烧不充分,产品中将有FeO存在,称取3.0 g氧化铁产品,溶解,在250 mL容量瓶中定容;量取25.00 mL待测溶液于锥形瓶中,用酸化的0.01000 mol/L KMnO4溶液滴定至终点,重复滴定2-3次,消耗KMnO4溶液体积的平均值为20.00 mL,
①该实验中的KMnO4溶液需要酸化,用于酸化的酸是__________(填字母序号)。
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
②计算上述产品中Fe2O3的质量分数为__________。
【答案】2 Fe3++SO2+2H2O="2" Fe2++SO42-+4H+ 过滤 沿玻璃棒往漏斗中加入适量蒸馏水至浸没沉淀,让蒸馏水自然流下,重复2-3次 FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O c 76%
【解析】
(1)根据方程式4Fe2++O2+ 4H+=4Fe3++2H2O和题干信息、可知,另一个反应的离子方程式为2 Fe3++SO2+2H2O="2" Fe2++SO42-+4H+,故答案为:2 Fe3++SO2+2H2O="2" Fe2++SO42-+4H+;
(2)①根据流程图可知,操作Ⅰ是过滤;洗涤的具体操作方法为:沿玻璃棒往漏斗中加入适量蒸馏水,浸没沉淀,让蒸馏水自然流下,重复2一3次,故答案为:过滤;沿玻璃棒往漏斗中加入适量蒸馏水至浸没沉淀,让蒸馏水自然流下,重复2-3次;
②根据题给的信息,化学方程式为: FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O,故答案为:FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O;
(3)①由于高锰酸钾溶液具有强氧化性,盐酸在常温下即可被其氧化,故一般用稀硫酸酸化,所以答案选c(硝酸不论稀、浓均具有强氧化性),故答案为:c;
②根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,可知样品中FeO的质量为0. 02 L×0. 01 mol/L×5×72 g/mol×10="0." 72 g,所以产品中Fe2O3的质量分数为((3. 0 g-0. 72 g)/3. 0 g×100%= 76%,故答案为:76%。


科目:高中化学 来源: 题型:
【题目】已知有:H、C、O、S、Cl、Fe六种元素,则回答下列有关其性质:
![]() 原子价电子的排布为 ______ ;Cl位于周期表中位置: ______ ;C原子核外有 ______ 个能级。
原子价电子的排布为 ______ ;Cl位于周期表中位置: ______ ;C原子核外有 ______ 个能级。
![]() 用“
用“![]() ”或“
”或“![]() ”填空:还原性:HCl ______
”填空:还原性:HCl ______ ![]() ,半径:C ______ O
,半径:C ______ O
![]() 在NaOH溶液中用Fe作阳极,通过电解制取
在NaOH溶液中用Fe作阳极,通过电解制取![]() 的电极反应式为: ______
的电极反应式为: ______
![]() 已知1molS完全燃烧生成
已知1molS完全燃烧生成![]() 放出akJ热量;又知
放出akJ热量;又知![]() ;
;![]() ;则请写出1mol固体S生成气体
;则请写出1mol固体S生成气体![]() 的热化学方程式为 ______
的热化学方程式为 ______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。工业上合成尿素的反应如下:2NH3(g)+CO2(g) ![]() CO(NH2)2(l)+H2O(l) △H<0。回答下列问题:
CO(NH2)2(l)+H2O(l) △H<0。回答下列问题:
(1)已知工业上合成尿素分两步进行,相关反应如下:
反应Ⅰ:2NH3(g)+CO2(g) ![]() NH2COONH4(s) △H1<0
NH2COONH4(s) △H1<0
反应Ⅱ:NH2COONH4(s) ![]() CO(NH2)2(l)+H2O(l) △H2>0
CO(NH2)2(l)+H2O(l) △H2>0
①△H=________________(用△H1、△H2表示)
②下列示意图中[a表示2NH3(g)+CO2(g),b表示NH2COONH4(s),c表示CO(NH2)2(l)+H2O(l)],能正确表示尿素合成过程中能量变化曲线是(填编号)______。
(2)某实验小组模拟工业上合成尿素的条件,在恒定温度下,将氨气和二氧化碳按2:1的物质的量之比充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计),经20min达到平衡,各物质浓度的变化曲线如下图所示。

①可以判断该化合反应已经达到化学平衡的是_________。(填编号)
A.![]() B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中氨气的体积分数不变 D.密闭容器中混合气体的密度不变
②在上述条件下,从反应开始至20min时,二氧化碳的平均反应速率为____________。
③该反应的平衡常数表达式K=____________。
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如下图所示。

阳极室中发生的反应依次为_____________________、____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯(PS)和聚对苯二甲酸乙二醇酯(PET)材料具有高韧性、质轻、耐酸碱等性能,在生产生活中应用广泛。这两种聚合物可按下图路线合成,请回答下列问题:

(1)A的分子式为______,其核磁共振氢谱有______组(个)吸收峰。
(2)含有苯环的B的同分异构体有______种。
(3)D为苯乙烯,其结构简式为______,官能团为______。
(4)F的名称为______,由E→G的反应类型是______(填“缩聚”或“加聚”)反应。
(5)已知:
![]()
![]()
![]()
![]()
![]()
写出由BrCH2CH2Br制备HOOC-CH2CH2-COOH的合成路线:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g)△H<0,若反应在恒容密闭容器中进行,如表由该反应相关图象作出的判断正确的是( )
N2O5(g)+O2(g)△H<0,若反应在恒容密闭容器中进行,如表由该反应相关图象作出的判断正确的是( )
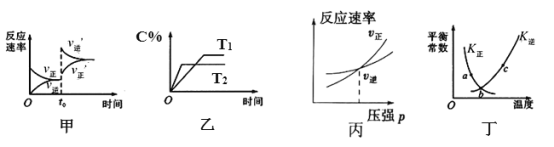
A.甲图中改变的反应条件为升温
B.乙图中温度T2>T1,纵坐标可代表NO2的百分含量
C.丙图为充入稀有气体时速率变化
D.丁图中a、b、c三点只有b点已经达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是( )
A.1mol碳正离子(CH3+)所含的电子总数为9NA
B.25℃,pH=13的Ba(OH)2 溶液中含有OH-的数目为0.1NA
C.常温常压下,过氧化钠与水反应时,生成8g氧气转移的电子数为0.5NA
D.1mol雄黄(As4S4),结构如图:![]() ,含有2NA个S-S键
,含有2NA个S-S键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是一种自然界分布较广的元素,在很多化合物中都含有该元素,回答下列问题:


(1)装置A中反应的化学方程式为______________________________________。
(2)使分液漏斗中液体顺利流下的操作是_________________________。
(3)选用上面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F的顺序连接装置即可证明,乙同学认为该方案不合理,其理由是_________
②丙同学设计的合理实验方案为A→C→________→________→D→F,其中装置C的作用是______,证明亚硫酸的酸性强于次氯酸的实验现象是____________
(4)K2S2O8具有强氧化性,可通过电解H2SO4和K2SO4的混合溶液制得,其阳极反应式为_________,称取0.250 0 g 产品于碘量瓶中,加100 mL水溶解,再加入8.000 g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以淀粉为指示剂,用 c mol/L的Na2S2O3标准液滴定至终点,消耗Na2S2O3标准液V mL,则样品中K2S2O8的纯度为________%(用含c、V的代数式表示,已知:S2O82-+2I-===2SO42-+I2 ;2S2O32-+I2===2S4O82-+2I- )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A.标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA
B.标准状况下,2.24L NO和2.24L O2混合后气体分子数为0.15 NA
C.0.1mol Na2O2与足量的潮湿的二氧化碳反应转移的电子数为0.1NA
D.加热条件下,1mol Fe投入足量的浓硫酸中,生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池以满足不同的需要。电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水中电池反应可表示为:5MnO2+2Ag+2NaCl===Na2Mn5O10+2AgCl
①该电池的负极反应式是____________;
②在电池中,Na+不断移动到“水”电池的________极(填“正”或“负”);
③外电路每通过4 mol电子时,生成Na2Mn5O10的物质的量是________;
(2)中国科学院应用化学研究所在甲醇(CH3OH是一种可燃物)燃料电池技术方面获得新突破。甲醇燃料电池的工作原理如图所示。

①该电池工作时,b口通入的物质为_________;
②该电池负极的电极反应式_________;
③工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有________个电子转移。
(3)Ag2O2是银锌碱性电池的正极活性物质,当银锌碱性电池的电解质溶液为KOH溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:_________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com