
【题目】由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象。
Ⅰ.甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用转化中得到的合成气制备甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g),某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图:
CH3OH(g),某温度下,在容积为2L的密闭容器中进行该反应,其相关数据见图:
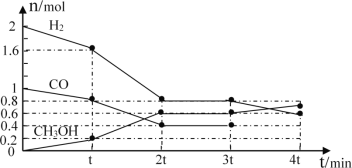
①根据图计算,从反应开始到tmin时,用H2浓度变化表示的平均反应速率υ(H2)=__。
②tmin至2tmin时速率变化的原因可能是__(要求答出所有可能原因)。
Ⅱ.一定温度下,向一容积为5L的恒容密闭容器中充入0.4molSO2和0.2molO2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的
2SO3(g) ΔH=-196kJ·mol-1。当反应达到平衡时,容器内压强变为起始时的![]() 。请回答下列问题:
。请回答下列问题:
①SO2的转化率为__;
②达到平衡时反应放出的热量为__。
【答案】![]() 使用催化剂、升高温度 90% 35.28 kJ
使用催化剂、升高温度 90% 35.28 kJ
【解析】
Ⅰ. ① 从反应开始到tmin时,氢气的物质的量由2mol减小到1.6mol则氢气的速率为: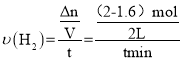 =
=![]() ,故答案为:
,故答案为:![]() 。
。
②tmin至2tmin时速率加快,升温、加压、使用催化剂均可以使反应速率加快,但因容器体积不变,所以加压不符合,可能的条件是使用了催化剂或者升高了温度,故答案为:使用催化剂、升高温度。
Ⅱ.根据题意设氧气的变化量为xmol,列出三段式。
2SO2(g) | +O2(g) | 2SO3(g) | ||
起始物质的量(mol) | 0.4 | 0.2 | ||
转化物质的量(mol) | 2x | x | 2x | |
平衡物质的量(mol) | 0.4-2x | 0.2-x | 2x |
当反应达到平衡时,容器内压强变为起始时的![]() ,由压强之比等于气体的物质的量之比,则
,由压强之比等于气体的物质的量之比,则![]() ,解得x=0.18,
,解得x=0.18,
①SO2的转化率为![]() ,故答案为:90%。
,故答案为:90%。
②由热化学方程式可知,每消耗1mol氧气,放出热量为196kJ,则平衡时消耗的氧气为0.18mol,放出热量为![]() ,故答案为:35.28 kJ。
,故答案为:35.28 kJ。


科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中一定能大量共存的是
A. 无色透明溶液中: H+、Na+、MnO![]() 、SO
、SO![]()
B. 碱性溶液中:Na+、K+、SiO![]() 、NO
、NO![]()
C. 能溶解Al2O3的溶液中:Mg2+、Cu2+、HCO![]() 、Cl-
、Cl-
D. 含有Fe2+的溶液中:H+、Ca2+、NO![]() 、AlO
、AlO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
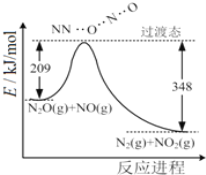
【题目】(1)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2,其△H=___kJ·mol-1。
(2)已知:①C(s)+O2(g)=CO2(g) ΔH=akJ·mol-1
②CO2(g)+C(s)=2CO(g) ΔH=bkJ·mol-1
③Si(s)+O2(g)=SiO2(s) ΔH=ckJ·mol-1
工业上生产粗硅的热化学方程式为__。
(3)在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需117kJ/mol~125kJ/mol的热量,但1,3—环己二烯失去2个氢原子变成苯是放热反应,△H=-23.4kJ/mol,以上事实表明苯加氢生成环己烷是__反应。(填放热或吸热)
(4)X、Y两元素的原子,当它们分别获得两个电子形成稀有气体元素电子层结构时,X放出的热量大于Y放出的热量;Z、W两元素的原子,当它们分别失去一个电子形成稀有气体元素原子的电子层结构时,吸收能量W大于Z。则X、Y和Z、W分别形成的化合物中,离子化合物可能性最大的是__。(填化合物的化学式)
(5)称取等质量为(ag)胆矾两份。把一份溶于bg水中,测知其溶解时吸收Q1kJ热量;把另一份脱水后溶于bg水中,测得其溶解时放热Q2kJ。从以上数据可知,1mol胆矾脱水需__kJ热量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表是某食品包装袋上的说明,从表中的配料中分别选出一种物质在相应的横线上。
品名 | ××× |
配料 | 鲜鸡蛋、精面粉、白砂糖、精炼植物油、奶油、奶粉、食盐、柠檬汁等 |
保质期 | 240天 |
生产日期 | 标于包装袋袋封口上 |
(1)富含蛋白质的物质是___________________________;
(2)富含糖类的物质是____________________________;
(3)富含油脂的物质是____________________________;
(4)富含维生素的物是___________________________。
Ⅱ.钢铁在潮湿的空气里很快就被腐蚀,原因是在钢铁的表面形成了一层电解质溶液的薄膜,跟钢铁里的铁和少量的碳构成无数微小的原电池,请写出两极发生的主要的电极式为:负极________________;正极_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物只含C、H、O三种元素,取4.6g该有机化合物完全燃烧,测得只生成0.2molCO2和5.4g水,其质谱图和核磁共振氢谱如图所示,回答下列问题: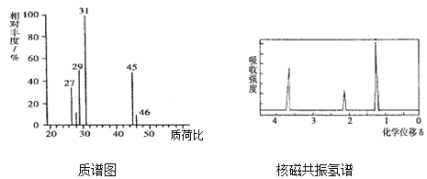
(1)该有机物的相对分子质量为:______________
(2)该有机物的分子式为:______________
(3)该有机物的结构简式为:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
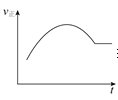
A.绝热恒容密闭容器中通入A和B,发生反应:2A(g)+B(g)2C(g),图为其正反应速率随时间变化的示意图,则该反应为放热反应
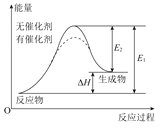
B.催化剂能降低反应的活化能,提高活化分子的百分含量,从而加快化学反应速率如图显示的是催化反应与无催化反应过程中的能量关系
C.将BaO2放入密闭真空容器中,反应2BaO2(s)2BaO(s)+O2(g)达到平衡时体系压强为P,保持温度不变,t0时刻将容器体积缩小为原来的一半,体系重新达到平衡,体系压强变化如图所示

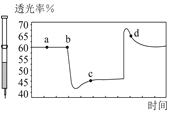
D.将一定量的NO2充入针筒中后封口,发生反应2NO2(g)N2O4(g),如图表示在拉伸和压缩针筒活塞的过程中气体透光率随时间的变化气体颜色越深,透光率越小。则c点与a点相比,c(NO2)增大,减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①1mol晶体硅中含有2molSi—Si键。
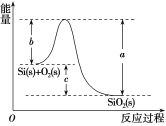
②Si(s)+O2(g)===SiO2(g) ΔH,其反应过程与能量变化如图所示。
③
化学键 | Si—O | O=O | Si—Si |
断开1 mol共价键所需能量/kJ | 460 | 500 | 176 |
下列说法中正确的是( )
A.晶体硅光伏发电是将化学能转化为电能B.二氧化硅稳定性小于硅的稳定性
C.ΔH=-988kJ·mol-1D.ΔH=(a-c)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法不正确的是
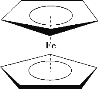
A.二茂铁属于分子晶体
B.环戊二烯中碳原子的杂化方式有sp3和sp2
C.1mol 环戊二烯( ![]() )中含有σ键的数目为5NA
)中含有σ键的数目为5NA
D.二茂铁分子中的化学键有极性共价键、非极性共价键和配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,电池总反应为4Al+3O2+6H2O=4Al(OH)3。下列说法不正确的是( )
A.正极的电极反应为O2+2H2O+4e-=4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大其与氧气的接触面积
D.该电池通常只需要更换铝板就可继续使用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com