
ЁОЬтФПЁПГЃЮТЯТЃЌПижЦЬѕМўИФБф0.1molЁЄL-1ЖўдЊШѕЫсH2C2O4ШмвКЕФpHЃЌШмвКжаЕФH2C2O4ЁЂHC2O4-ЁЂC2O42-ЕФЮяжЪЕФСПЗжЪ§ІФ(X)ЫцpOHЕФБфЛЏШчЭМЫљЪОЁЃвбжЊpOH=-lgc(OH-)ЃЌ![]() ЁЃЯТСаа№ЪіДэЮѓЕФЪЧЃЈ ЃЉ
ЁЃЯТСаа№ЪіДэЮѓЕФЪЧЃЈ ЃЉ
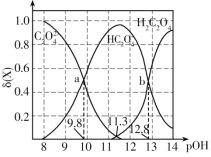
A.ЗДгІH2C2O4+C2O42-![]() 2HC2O4-ЕФЦНКтГЃЪ§ЕФжЕЮЊ103
2HC2O4-ЕФЦНКтГЃЪ§ЕФжЕЮЊ103
B.ШєЩ§ИпЮТЖШЃЌaЕувЦЖЏЧїЪЦЯђгв
C.pH=3ЪБЃЌ![]() =100.6ЃК1
=100.6ЃК1
D.ЮяжЪЕФСПХЈЖШОљЮЊ0.1molЁЄL-1ЕФNa2C2O4ЁЂNaHC2O4ЛьКЯШмвКжаЃКc(Na+)>c(C2O42-)>c(HC2O4-)>c(H+)>c(OH-)
ЁОД№АИЁПB
ЁОНтЮіЁП
AЃЎЗДгІH2C2O4+C2O42-![]() 2HC2O4-ЕФЦНКтГЃЪ§K=
2HC2O4-ЕФЦНКтГЃЪ§K=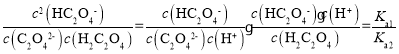 ЃЌaЕуc(C2O42-)= c(HC2O4-)ЃЌДЫЪБpOH=9.8ЃЌдђc(OH-)=10-9.8mol/LЃЌc(H+)=10-4.2mol/LЃЌдђKa2=
ЃЌaЕуc(C2O42-)= c(HC2O4-)ЃЌДЫЪБpOH=9.8ЃЌдђc(OH-)=10-9.8mol/LЃЌc(H+)=10-4.2mol/LЃЌдђKa2=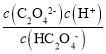 = 10-4.2ЃЛЭЌРэbЕуc(HC2O4-)=c(H2C2O4)ПЩЕУKa1=10-1.2ЃЌЫљвдЗДгІЕФЦНКтГЃЪ§K=
= 10-4.2ЃЛЭЌРэbЕуc(HC2O4-)=c(H2C2O4)ПЩЕУKa1=10-1.2ЃЌЫљвдЗДгІЕФЦНКтГЃЪ§K=![]() ЃЌЙЪAе§ШЗЃЛ
ЃЌЙЪAе§ШЗЃЛ
BЃЎЮТЖШЩ§ИпЃЌЫЎЕФЕчРыГЬЖШдіДѓЃЌЫЎЕФРызгЛ§БфДѓЃЌpHгыpOHжЎКѓаЁгк14ЃЌдђЭМЯёећЬхНЋЯђзѓвЦЖЏЃЌЙЪBДэЮѓЃЛ
CЃЎ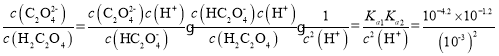 =100.6ЃК1ЃЌЙЪCе§ШЗЃЛ
=100.6ЃК1ЃЌЙЪCе§ШЗЃЛ
DЃЎH2C2O4ЕФKa1=10-1.2ЃЌKa2=10-4.2ЃЌдђHC2O4-ЕФЫЎНтЦНКтГЃЪ§Kh1=![]() ЃЌМДЦфЕчРыГЬЖШДѓгкЦфЫЎНтГЬЖШЃЌЫљвдДПNaHC2O4ШмвКжаc(C2O42-)>c(H2C2O4)ЃЌМгШыЕШЮяжЪЕФСПХЈЖШNa2C2O4ЁЂВнЫсФЦЛсЕчРыГіДѓСПЕФC2O42-ЃЌдђШмвКжаДцдкc(C2O42-)>c(HC2O4-)ЃЌОнЭМПЩжЊЕБc(C2O42-)>c(HC2O4-)ЪБШмвКГЪЫсадЃЌФЦРызгВЛЫЎНтЃЌЫљвдЛьКЯШмвКжаРызгХЈЖШДѓаЁЙиЯЕЮЊc(Na+)>c(C2O42-)>c(HC2O4-)>c(H+)>c(OH-)ЃЌЙЪDе§ШЗЃЛ
ЃЌМДЦфЕчРыГЬЖШДѓгкЦфЫЎНтГЬЖШЃЌЫљвдДПNaHC2O4ШмвКжаc(C2O42-)>c(H2C2O4)ЃЌМгШыЕШЮяжЪЕФСПХЈЖШNa2C2O4ЁЂВнЫсФЦЛсЕчРыГіДѓСПЕФC2O42-ЃЌдђШмвКжаДцдкc(C2O42-)>c(HC2O4-)ЃЌОнЭМПЩжЊЕБc(C2O42-)>c(HC2O4-)ЪБШмвКГЪЫсадЃЌФЦРызгВЛЫЎНтЃЌЫљвдЛьКЯШмвКжаРызгХЈЖШДѓаЁЙиЯЕЮЊc(Na+)>c(C2O42-)>c(HC2O4-)>c(H+)>c(OH-)ЃЌЙЪDе§ШЗЃЛ
ЙЪД№АИЮЊBЁЃ


 гЂВХЕуНђЯЕСаД№АИ
гЂВХЕуНђЯЕСаД№АИ КьЙћзгШ§МЖВтЪдОэЯЕСаД№АИ
КьЙћзгШ§МЖВтЪдОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРЯЪѓФмдкЖрЗњЬМЛЏЮяШмвКФкВПЧБЫЎгЮЖЏЃЌПЦбЇМвдЄВтЖрЗњЬМЛЏЮяПЩФмГЩЮЊбЊвКЬцДњЦЗЁЃШЋЗњБћЭщ(C3F8)ЪЧвЛжжГЃМћЕФЖрЗњЬМЛЏЮяЃЌЯТСаЖдИУЮяжЪЕФа№ЪіжаВЛе§ШЗЕФЪЧ(ЁЁЁЁ)
A. дзгАыОЖCБШFЕФДѓ
B. ШЋЗњБћЭщЕФЕчзгЪНЮЊ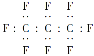
C. ШЋЗњБћЭщЗжзгжажЛКЌІвМќ
D. ШЋЗњБћЭщЗжзгжаМШКЌМЋадМќгжКЌЗЧМЋадМќ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТЭМЪЧЪЕбщЪвжЦШЁSO2ВЂбщжЄSO2ЕФФГаЉаджЪЕФзАжУЃЌЧыЛиД№ЃК
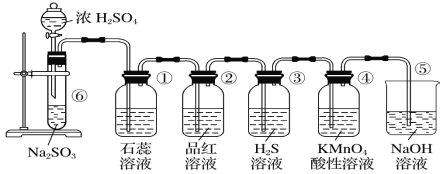
ЃЈ1ЃЉдкЂожаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ________ЁЃ
ЃЈ2ЃЉЂйжаЕФЪЕбщЯжЯѓЮЊЪЏШяШмвК__________ЃЌжЄУїSO2ЕФЫЎШмвКЯд_______адЁЃ
ЃЈ3ЃЉЂкжаЕФЦЗКьШмвК________ЃЌжЄУїSO2га________адЁЃ
ЃЈ4ЃЉЂлжаЕФЪЕбщЯжЯѓЪЧ________________________ЃЌжЄУїSO2га____________адЁЃ
ЃЈ5ЃЉЂмжаЕФЪЕбщЯжЯѓЪЧ______ЃЌжЄУїSO2га______адЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаа№ЪіВЛе§ШЗЕФЪЧ![]()
![]()
A.NH3взвКЛЏЃЌАБГЃгУзїжЦРфМС
B.ГЃЮТЯТЃЌПЩвдгУЬњЁЂТСжЦШнЦїЪЂзАХЈСђЫсЛђХЈЯѕЫс
C.яЇбЮЪмШШвзЗжНтЃЌвђДЫжќДцяЇЬЌЕЊЗЪЪБвЊУмЗтБЃДцЃЌВЂЗХдквѕСЙЭЈЗчДІ
D.гыН№ЪєЗДгІЪБЃЌЯЁHNO3ПЩФмБЛЛЙдЮЊИќЕЭМлЬЌЃЌдђЯЁHNO3бѕЛЏадЧПгкХЈHNO3
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвжЦБИДЮСђЫсЧтФЦМзШЉ(NaHSO2ЁЄHCHOЁЄ2H2O)ЕФВНжшШчЯТЃКЯђЩеЦПжаЕФбЧСђЫсФЦШмвКЭЈШыSO2жЦЕУNaHSO3ЁЃНЋзАжУAжаЕМЦјЙмЛЛГЩЯ№ЦЄШћЃЌдйМгШыаПЗлКЭМзШЉШмвКЃЌдк80ЁЋ90ЁцЯТЃЌЗДгІдМ3hЃЌРфШДжСЪвЮТЃЌГщТЫЃЌНЋТЫвКжУгкецПееєЗЂвЧеєЗЂХЈЫѕЃЌРфШДНсОЇЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧЃЈ ЃЉ
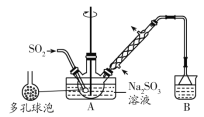
A.ПЩгУбЧСђЫсФЦЙЬЬхКЭ70%СђЫсРДжЦШЁЖўбѕЛЏСђЦјЬх
B.ЖрПзЧђХнЕФзїгУЪЧдіДѓЦјЬхгыШмвКЕФНгДЅУцЛ§ЃЌЪЙЗДгІГфЗжНјаа
C.зАжУBжаЪдМСПЩвдЪЧNaOHЛђNa2CO3ШмвК
D.зАжУAжаПЩВЩгУгЭдЁЛђЩГдЁМгШШ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏбЇаЫШЄаЁзщгћдкЪЕбщЪвЬНОПТШЦјЕФаджЪМАФЃФтЙЄвЕжЦШЁЦЏАзЗлЩшМЦСЫШчЭМзАжУНјааЪЕбщЃК
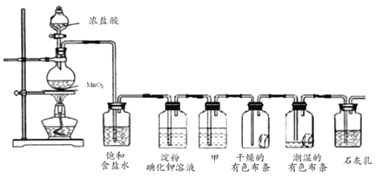
ЧыАДвЊЧѓЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉдВЕзЩеЦПжажЦТШЦјЕФЛЏбЇЗНГЬЪН________ЃЛ
ЃЈ2ЃЉЕэЗлЕтЛЏМиШмвКжаЙлВьЕНЕФЯжЯѓЪЧ________ЃЛ
ЃЈ3ЃЉШєИЩдяЕФгаЩЋВМЬѕВЛЭЪЩЋГБЪЊЕФгаЩЋВМЬѕЭЪЩЋЃЌдђМзжаЪЂЗХ________ЃЛ
ЃЈ4ЃЉ![]() гыЪЏЛвШщЗДгІжЦШЁЦЏАзЗлЕФЛЏбЇЗНГЬЪНЮЊ________ЃЛ
гыЪЏЛвШщЗДгІжЦШЁЦЏАзЗлЕФЛЏбЇЗНГЬЪНЮЊ________ЃЛ
ЃЈ5ЃЉгУЯТСаСНжжЗНЗЈжЦШЁТШЦјЃКЂйгУКЌТШЛЏЧт146gЕФХЈбЮЫсгызуСПЕФЖўбѕЛЏУЬЗДгІЃЛЂкгУ87gЖўбѕЛЏУЬгызуСПЕФХЈбЮЫсЗДгІЃЌдђЫљЕУТШЦј________ЁЃ
A.ЂкБШЂйЖр B.ЂйБШЂкЖр C.вЛбљЖр D.ЮоЗЈБШНЯ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЮЊФЩУзЖўбѕЛЏУЬШМСЯЕчГиЃЌЦфЕчНтжЪШмвКГЪЫсадЃЌвбжЊЃЈCH2OЃЉnжаЬМЕФЛЏКЯМлЮЊ0МлЃЌгаЙиИУЕчГиЕФЫЕЗЈе§ШЗЕФЪЧ

A. ЗХЕчЙ§ГЬжазѓВрШмвКЕФpHНЕЕЭ
B. ЕБВњЩњ22gCO2ЪБЃЌРэТлЩЯЧЈвЦжЪзгЕФЮяжЪЕФСПЮЊ4mol
C. ВњЩњ22gCO2ЪБЃЌФЄзѓВрШмвКЕФжЪСПБфЛЏЮЊЃК89g
D. ЕчзгдкЭтЕчТЗжаСїЖЏЗНЯђЮЊДгaЕНb
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЭЌЮТЁЂЭЌбЙЯТЃЌЕШЬхЛ§ЕФNH3КЭCH4СНжжЦјЬхЃЌЯТСагаЙиЫЕЗЈДэЮѓЕФЪЧЃЈЃЉ
A.ЫљКЌЗжзгЪ§ФПЯрЭЌB.жЪСПжЎБШЮЊ16ЃК17
C.ЫљКЌЧтдзгЮяжЪЕФСПжЎБШЮЊ3ЃК4D.УмЖШжЎБШЮЊ17ЃК16
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯђКЌга4 mol HNO3КЭ1 mol H2SO4ЕФЛьКЯШмвКжаж№НЅМгШыЬњЗлжСЙ§СПЃЌШмвКжаН№ЪєбєРызгaЁЂbгыЫљМгЬњЗлЕФЮяжЪЕФСПЕФЙиЯЕШчЭМЫљЪО(вбжЊЯЁЯѕЫсЕФЛЙдВњЮяжЛгаNO)ЁЃ
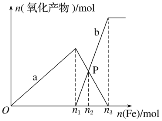
(1)bБэЪОЕФЙиЯЕЧњЯп_______(ЬюРызгЗћКХ)
(2)n1ЃН______
(3)PЕуЪБЃЌn(Fe2ЃЋ)ЃН______mol
(4)ЯђPЕуШмвКжаМгШыЭЗлЃЌзюЖрПЩШмНт________g
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com