
在一密闭容器中充入一定量的N2和O2,在电火花作用下发生反应N2+O2═2N0,经测定前3s用N2表示的反应速率为0.1mol/(L•s),则6S末N0的浓度为( )
|
| A. | 1.2 mol•L﹣1 | B. | 大于1.2 mol•L﹣1 | C. | 小于1.2 mol•L﹣1 | D. | 不能确定 |
| 反应速率的定量表示方法.. | |
| 专题: | 化学反应速率专题. |
| 分析: | 随反应进行N2浓度降低,反应速率降低,故3s~6s内N2的速率小于0.1mol/(L•s),即6s内N2的速率小于0.1mol/(L•s),速率之比等于化学计量数之比,据此计算v(NO)极值,再根据c=v•△t计算判断6s末NO的浓度. |
| 解答: | 解:随反应进行N2浓度降低,反应速率降低,故3s~6s内N2的速率小于0.1mol/(L•s),即6s内N2的速率小于0.1mol/(L•s),速率之比等于化学计量数之比,故v(NO)小于2×0.1mol/(L•s)=0.2mol/(L•s),故6s末NO的浓度小于6s×0.2mol/(L•s)=1.2mol/L, 故选C. |
| 点评: | 本题考查化学反应速率有关计算及影响因素等,难度不大,判断后3s的速率较前3s低是解题关键. |


科目:高中化学 来源: 题型:
据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学方程式为:5KClO3 + 6P=3P2O5 + 5KCl ,则下列有关叙述正确的是 ( )
A.上述反应是复分解反应
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)
C.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
D.上述反应中消耗3molP时,转移电子的物质的量为30mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质之间通过一步就能实现如图所示转化的是
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① |
| Na2O | Na2O2 | Na | NaOH |
| ② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
| ③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
| ④ | NO | NO2 | N2 | HNO3 |
A.①② B.②③. C.②④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.某酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a≤b-1
B.在滴酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的c (NH4+) = c(Cl-)
C.常温下,某硫酸溶液的pH=3,升高其温度,溶液pH增大
D.相同温度、相同体积、相同物质的量浓度的KI和KF溶液中,离子总数前者大于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ 氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
3SiO2+6C+2N2 Si3N4+6CO;DH <0。
Si3N4+6CO;DH <0。
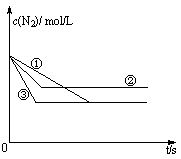 (1)在容积固定的密闭容器中,分别在三种不同的实验条件下进行上述制备反应,测得N2的物质的量浓度随时间的变化如右图所示,②和③分别仅改变一种反应条件。所改变的条件分别是:② ;③ 。
(1)在容积固定的密闭容器中,分别在三种不同的实验条件下进行上述制备反应,测得N2的物质的量浓度随时间的变化如右图所示,②和③分别仅改变一种反应条件。所改变的条件分别是:② ;③ 。
(2)1 000℃时,在2 L密闭容器中进行上述反应,若起始时N2浓度为4.0 mol/L,经1小时反应达到平衡状态,此时容器内气体总浓度为10.0 mol/L,则以CO表示的反应速率为 。若某时刻测得N2和CO的浓度均为6.0 mol/L,则反应的V正 V逆(填“大于”、“小于”、 “等于”)。
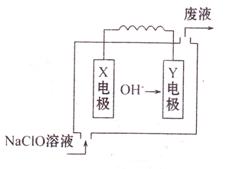
Ⅱ、右图为Mg—NaClO燃料电池结构示意图。已知电解质溶液为NaOH溶液,且两电极中有一电极为石墨电极。
Y电极材料为 。
X电极发生的电极反应式为 。
若该电池开始时加入1L 0.2mol/L的NaOH溶液,然后从下口充入1L 0.1mol/L的NaClO溶液(忽略整个过程的体积变化),当NaClO完全放电时溶液的PH=
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下的密闭容器中有如下反应:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)△H=﹣905.9kJ•mol﹣1,下列叙述正确的是( )
|
| A. | 4 mol NH3和5 mol O2反应,达到平衡时放出热量为905.9 kJ |
|
| B. | 平衡时v正(O2)=v逆(NO) |
|
| C. | 平衡后减小压强,混合气体平均摩尔质量增大 |
|
| D. | 平衡后升高温度,混合气体中NO含量降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
研究NO2、SO2、等大气污染气体的处理具有重要意义.
(1)NO2可用水吸收,相应的化学反应方程式为 3NO2+H2O=NO+2HNO3 .利用反应6NO2+8NH3 7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 6.72 L.
7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2在标准状况下是 6.72 L.
(2)已知:2SO2(g)+O2(g)⇌2SO3(g)△H=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)⇌2NO2(g)△H=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的△H= ﹣41.8 kJ•mol﹣1.
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 b .
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1mol SO3的同时生成1molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= .
查看答案和解析>>
科目:高中化学 来源: 题型:
普罗加比对癫痫、痉挛和运动失调均有良好的治疗效果,其结构如图所示,有关普罗加比的说法正确的是( )
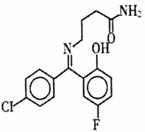
A.该分子在1H核磁共振谱中有12个峰
B.一定条件下,1 mol普罗加比最多能与2 mol H2发生加成反应
C.久置在空气中的普罗加比会因氧化而变质
D.普罗加比可以和NaOH溶液、Na2CO3溶液反应,也可以和盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素X核电荷数小于18,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1。下列有关X的说法中,不正确的是
A.X能形成化学式为X(OH)3的碱
B.X能形成化学式为NaXO3的含氧酸钠盐
C.X原子的最外层电子数和核电荷数不可能为偶数
D.X能与某些金属元素或非金属元素形成化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com