
【题目】下列叙述中正确的是( )
A. 漂白粉中的有效成分为次氯酸钙,在空气中可以长时间放置而不变质
B.二氧化硅是将太阳能转变为电能的常用材料
C.美国纽约冬季城市供暖使用的主要能源是天然气,天然气属于不可再生能源
D.虎门销烟中用到了大量的生石灰,将生石灰投入销烟池的海水中,海水开始翻腾,这是一个物理变化
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.NH3、CO、CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.分子晶体熔点越高,其稳定性越增强
D.CS2、H2O、C2H2都是直线形分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(X代表卤素原子,R代表烃基) 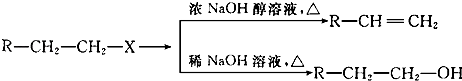
利用上述信息,按以下步骤从 ![]() 合成
合成 ![]() .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)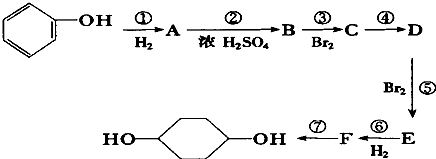
请回答下列问题:
(1)分别写出B、D的结构简式:B_、D .
(2)反应①~⑦中属于消去反应的是 . (填数字代号)
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为: .
(4)试写出C→D反应的化学方程式(有机物写结构简式,并注明反应条件): .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84g/mL)配制浓度为0.5molL﹣1的稀硫酸500mL.
(1)选用的主要仪器有:量筒,烧杯,玻璃棒,试剂瓶,还缺少仪器的名称是;
(2)请将下列各操作,按正确的操作顺序序号填在横线上;
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至环形刻度线
D.稀释浓H2SO4
E.将溶液冷却至室温后转入容量瓶
(3)简要回答下列问题:
①所需浓硫酸的体积为mL;
②如果实验室有15mL、20mL、50mL规格的量筒,应选用mL的量筒最好,量取时发现量筒不干净用水洗净后直接量取将使浓度(“偏高”、“偏低”、“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】截至到2013年12月末,中国光伏发电新增装机容量达到10.66GW,光伏发电累计装机容量达到17.16GW,图1为光伏并网发电装置.图2为电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).下列叙述中正确的是( ) 
A.图1中N型半导体为正极,P型半导体为负极
B.图2溶液中电子流向:从B极流向A极
C.X2为氧气
D.工作时,A极的电极反应式为CO(NH2)2+8OH﹣﹣6e﹣═CO32﹣+N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①H2②铝 ③CaO ④CO2⑤H2SO4⑥Ba(OH)2⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为 .
(2)⑩在水中的电离方程式为 .
(3)少量的④通入⑥的溶液中反应的离子方程式为 , 过量的④通入⑥的溶液中反应的离子方程式为 .
(4)⑥与过量的碳酸氢钠溶液反应离子方程式: .
(5)②与⑨发生反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,当有5.4g Al发生反应时,转移电子的数目为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应N2+3H22NH3 , △H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图1所示: 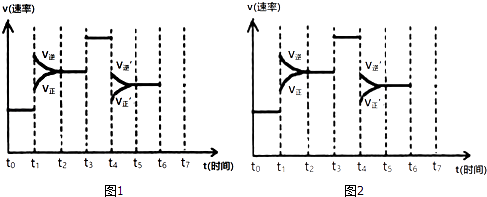
回答下列问题:
(1)处于平衡状态的时间段是(填选项).
A.t0~t1
B.t1~t2
C.t2~t3
D.t3~t4
E.t4~t5
F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是:t1时刻;t3时刻;t4时刻 . (填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中结论,下列时间段中,氨的百分含量最高的是(填选项).
A.t0~t1
B.t2~t3
C.t3~t4
D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,若将密闭容器体积缩小一半,则对反应产生的影响是(填选项).
A.正反应速率减小,逆反应速率增大
B.正反应速率增大,逆反应速率减小
C.正、逆反应速率都减小
D.正、逆反应速率都增大
(5)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图2中画出反应速率的变化曲线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com