
【题目】常温下含碳各微粒H2CO3、HCO3-和CO32-存在于CO2和NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )

A. 为获得尽可能纯的NaHCO3,宜控制溶液的pH为7~9之间
B. pH=10.25时,c(Na+)=c(CO32-)+c(HCO3-)
C. 根据图中数据,可以计算得到H2CO3第一步电离的平衡常数K1(H2CO3)=10-6.37
D. 若是0.1mol NaOH反应后所得的1L溶液,pH=10时,溶液中存在以下关系: c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
【答案】B
【解析】
A.根据图示可知,pH在7~9之间,溶液中主要存在HCO3-,该pH范围内和获得较纯的NaHCO3,选项A正确;B.pH=10.25时,溶质为碳酸钠和碳酸氢钠,碳酸钠溶液中满足物料守恒:c(Na+)═2c(CO32-)+2c(HCO3-)+2c(H2CO3),碳酸氢钠溶液中存在物料守恒:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),则混合液中c(Na+)>c(CO32-)+c(HCO3-),选项B错误;C.根据图象曲线可知,pH=6.37时,H2CO3和HCO3-的浓度相等,碳酸的第一步电离的平衡常数K1(H2CO3)=![]() =10-6.37,选项C正确;D.pH=10时的溶液为碱性,则c(OH-)>c(H+),溶质为碳酸钠和碳酸氢钠,c(Na+)离子浓度最大,结合图象曲线变化可知:c(HCO3-)>c(CO32-),此时离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),选项D正确;答案选B。
=10-6.37,选项C正确;D.pH=10时的溶液为碱性,则c(OH-)>c(H+),溶质为碳酸钠和碳酸氢钠,c(Na+)离子浓度最大,结合图象曲线变化可知:c(HCO3-)>c(CO32-),此时离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),选项D正确;答案选B。


科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 100mL12mol/L的浓硝酸与过量Cu反应转移电子数目为0.6NA
B. 将1molCl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA
C. 同温同压下,两个等体积的干燥圆底烧瓶中分别充满①HCl ②NO2 ,进行喷泉实验。经充分反应后烧瓶内溶质的物质的量浓度之比为3:2
D. 实验室里要用480 mL 0.1mol/L的硫酸铜溶液,需称取12.5克胆矾配制成溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图每一方框表示有关反应的某一反应物或生成物,有关操作已略去。又知A为高熔点物质,B为无色气体,D为一种天然出产的矿石的主要成分,可作为颜料。试回答:
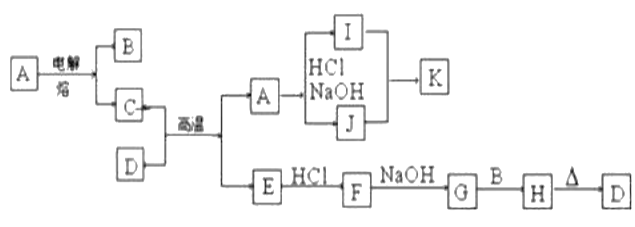
(1)写出下列物质的化学式:I____________,F____________。
(2)G转化为H的现象是____________,对应化学方程式为____________。
(3)写出I和J反应生成K的离子方程式____________。
(4)写出C+D→A+E的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物 X 可能是由 Na2SiO3、 Fe 、 Na2CO3、 BaCl2中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计实验方案如下图所示(所加试剂均过量)。下列说法不正确的是:

A. 该固体混合物一定含有 Fe、 Na2CO3、 BaCl2
B. 气体A一定是混合气体
C. 白色沉淀B在空气中逐渐变灰绿色,最后变红褐色
D. 沉淀A一定是 H2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ亚铁氰化钾K4[Fe(CN)6],俗名黄血盐,可溶于水,不溶于乙醇。它是一种食品添加剂,我们所食用的部分食盐中就添加了亚铁氰化钾作为抗结剂。如果食用过量,易引起胃肠适。同学们可以观察一下家中食盐的配料表,尽量选用不含抗结剂的食盐。亚铁氰化钾可用如下方法进行制备。
已知HCN是一种极弱的酸,现有一种用含NaCN的废水合成黄血盐的主要工艺流程如下:
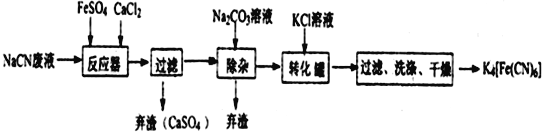
(1)常温下,NaCN水溶液的pH_______7(填“>”、“<”、“ = ”)。
(2)反应器中发生的主要反应的化学方程式为_____________________________。
(3)流程中加入Na2CO3溶液后过滤除去弃渣,过滤需要的玻璃仪器有烧杯、漏斗、______________。
(4)转化器中生成K4[Fe(CN)6]的反应类型是_______________,相同温度下,溶解度:K4[Fe(CN)6]___________Na4[Fe(CN)6](填“>”“ = ”“<”)。
(5)实验室常用K4[Fe(CN)6]检验Fe3+,生成难溶盐KFe[Fe(CN)6],试写出上述反应的离子方程式为_____________________________。
Ⅱ亚铁氰化钾也可以用硫酸亚铁铵为原料制备。可以用氧化还原滴定法测定晶体中Fe2+的含量。称取一份质量为20.0g 的硫酸亚铁铵晶体样品,制成溶液。用0.5 mol/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO4- 被还原成Mn2+时,耗KMnO4 溶液体积20.00mL。
滴定时,将KMnO4 溶液装在____(酸式或碱式) 滴定管中,判断反应到达滴定终点的现象为__________ ;晶体中FeSO4的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次递增的甲、乙、丙、丁、戊是周期表中前30号元素,其中甲、乙、丙三元素的基态原子2p能级都有单电子,单电子个数分别是2、3、2;丁与戊原子序数相差18,戊元素是周期表中ds区的第一种元素。回答下列问题:
(1)甲能形成多种常见单质,在熔点很高的两种常见单质中,原子的杂化方式分别为______、__________。
(2)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测丁元素的电离能突增应出现在第________电离能。
(3)戊的基态原子有________种形状不同的原子轨道;
(4)甲、乙分别都能与丙形成原子个数比为 1:3的微粒,则该两种微粒的空间构型分别为:_________________ ;__________________。
(5)丙和丁形成的一种离子化合物的晶胞结构如右图,该晶体中阳离子的配位数为_________ 。距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_______________。已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,该化合物的相对分子质量为 M,则该晶胞中黑球的半径r =_____cm。(用含ρ、NA的计算式表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 氢氟酸贮存在细口玻璃瓶里
B. 盛溴的试剂瓶里加一些水来防止溴挥发
C. 可用滴加酚酞看其是否变红的方法来检测久置的烧碱是否变质
D. 氯水保存在无色玻璃瓶中;液氯存贮存在钢瓶里
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有少量过氧化钠固体的试管中滴加水,直到气体不再放出,加水稀释,取少量所得溶液,加入少量二氧化锰,又有气体放出,待气体不再放出后,再滴加酚酞,溶液变红。下列猜测不合理的是
A.过氧化钠和水反应生成氢氧化钠和氧气
B.过氧化钠和水反应的产物是过氧化氢和氧气
C.过氧化氢在二氧化锰催化作用下分解生成氧气和水
D.过氧化钠跟水反应生成氢氧化钠和过氧化氢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com