
����Ŀ���������軯��K4[Fe(CN)6]��������Ѫ�Σ�������ˮ���������Ҵ�������һ��ʳƷ���Ӽ���������ʳ�õIJ���ʳ���о������������軯����Ϊ����������ʳ�ù�����������θ���ʡ�ͬѧ�ǿ��Թ۲�һ�¼���ʳ�ε����ϱ�������ѡ�ò����������ʳ�Ρ������軯�ؿ������·��������Ʊ���
��֪HCN��һ�ּ������ᣬ����һ���ú�NaCN�ķ�ˮ�ϳɻ�Ѫ�ε���Ҫ�����������£�
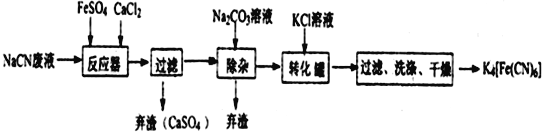
��1�������£�NaCNˮ��Һ��pH_______7������������������� = ������
��2����Ӧ���з�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ_____________________________��
��3�������м���Na2CO3��Һ����˳�ȥ������������Ҫ�IJ����������ձ���©����______________��
��4��ת����������K4[Fe(CN)6]�ķ�Ӧ������_______________����ͬ�¶��£��ܽ�ȣ�K4[Fe(CN)6]___________Na4[Fe(CN)6]��������� = ������������
��5��ʵ���ҳ���K4[Fe(CN)6]����Fe3+������������KFe[Fe(CN)6]����д��������Ӧ�����ӷ���ʽΪ_____________________________��
�������軯��Ҳ���������������Ϊԭ���Ʊ���������������ԭ�ζ����ⶨ������Fe2+�ĺ�������ȡһ������Ϊ20.0g ����������茶�����Ʒ���Ƴ���Һ����0.5 mol/L KMnO4��Һ�ζ�������Һ��Fe2+ȫ����������MnO4- ����ԭ��Mn2+ʱ����KMnO4 ��Һ���20.00mL��
�ζ�ʱ����KMnO4 ��Һװ��____(��ʽ���ʽ) �ζ����У��жϷ�Ӧ����ζ��յ������Ϊ__________ ��������FeSO4����������Ϊ____________��
���𰸡�>6NaCN+FeSO4+CaCl2=Na4[Fe��CN��6]+CaSO4��+2NaCl���������ֽⷴӦ<K++[Fe(CN)6]4-+Fe3+=KFe[Fe(CN)6]��ʽ�������һ����Һʱ���ճ����Ϻ�ɫ������30s����38%
��������
����1��NaCN��ǿ�������Σ�����Һ����Һˮ�⣬ʹ��Һ�Լ��ԣ�NaCNˮ������ӷ���ʽΪCN-+H2O![]() HCN+OH-����2���������̿�֪����Ӧ����NaCN ��FeSO4��CaCl2��Ӧ����CaSO4���Լ�������һ����Ӧ��Na4[Fe��CN��6]����Ϸ���ʽ��֪���в���NaCl���ʷ�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ6NaCN+FeSO4+CaCl2=Na4[Fe��CN��6]+CaSO4��+2NaCl����3��������Ҫ�IJ����������ձ���©������������(4)ת�����з����ķ�Ӧ�ǣ�Na4[Fe(CN)6]��4KCl===K4[Fe(CN)6]����4NaCl���˷�Ӧ���ڸ��ֽⷴӦ���ó�K4[Fe(CN)6]���ܽ��С��Na4[Fe(CN)6]����5��ʵ���ҳ���K4[Fe(CN)6]����Fe3+������������KFe[Fe(CN)6]�����ݷ�ӦNa4[Fe(CN)6]��4KCl===K4[Fe(CN)6]����4NaCl�ɵ÷�Ӧ�����ӷ���ʽΪK++[Fe(CN)6]4-+Fe3+=KFe[Fe(CN)6]��
HCN+OH-����2���������̿�֪����Ӧ����NaCN ��FeSO4��CaCl2��Ӧ����CaSO4���Լ�������һ����Ӧ��Na4[Fe��CN��6]����Ϸ���ʽ��֪���в���NaCl���ʷ�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ6NaCN+FeSO4+CaCl2=Na4[Fe��CN��6]+CaSO4��+2NaCl����3��������Ҫ�IJ����������ձ���©������������(4)ת�����з����ķ�Ӧ�ǣ�Na4[Fe(CN)6]��4KCl===K4[Fe(CN)6]����4NaCl���˷�Ӧ���ڸ��ֽⷴӦ���ó�K4[Fe(CN)6]���ܽ��С��Na4[Fe(CN)6]����5��ʵ���ҳ���K4[Fe(CN)6]����Fe3+������������KFe[Fe(CN)6]�����ݷ�ӦNa4[Fe(CN)6]��4KCl===K4[Fe(CN)6]����4NaCl�ɵ÷�Ӧ�����ӷ���ʽΪK++[Fe(CN)6]4-+Fe3+=KFe[Fe(CN)6]��
��KMnO4 ����ǿ�������ܸ�ʴ������װ����ʽ�ζ����У��жϷ�Ӧ����ζ��յ������Ϊ�������һ����Һʱ���ճ����Ϻ�ɫ������30s���䣻�辧����FeSO4�����ʵ���Ϊx����
5Fe2++ MnO4-+8H+�T5Fe3++Mn2++4H2O
5mol 1mol
x 0.5mol/L��20.0��10-3L
x=![]() ��������FeSO4����������Ϊ
��������FeSO4����������Ϊ![]() ��
��


 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ����ȵ�����������Һϴȥ�Թ��ڱ�մ�е����ʣ�������Ӧ6NaOH��3S![]() 2Na2S��Na2SO3��3H2O�����ڸ÷�Ӧ��˵������ȷ����(����)
2Na2S��Na2SO3��3H2O�����ڸ÷�Ӧ��˵������ȷ����(����)
A. ��������������ǻ�ԭ�� B. �����ǻ�ԭ����
C. ��ȱ����������ֱ��ֻ�ԭ�� D. ����3 mol ��ת�Ƶ���6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������У���ȷ����
A.ϡ��ŨH2SO4ʱ��������ˮ�������ڱڻ�������ŨH2SO�У�����ʱ����
B.�ⶨ��ҺpHʱ���ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ��۲���ֽ����ɫ�仯���������ɫ����Ƚ�
C.����NaOH����ʱ����NaOH������ڵ�����ֽ��������
D.������NaCl��Һ�õ�NaCl�����ʵ���У�������������е�ˮ��ȫ�����ɺ���ܳ�ȥ�ƾ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��������������������أ������й�˵����ȷ������ ��
A. ���ά����Ϣ����Ӧ��Խ��Խ�㷺������Ҫ�ɷ��ǹ赥��
B. Ϊ�ӿ�Ư�۵�Ư�����ʣ�ʹ��ʱ�ɵμӼ��δ���
C. ����������ˮ��ɱ������
D. ���ォ����Ϊ��ֹ�±��ȸ�֬ʳƷ�������ʣ����ڰ�װ���з�����ʯ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������º�̼����H2CO3��HCO3����CO32��������CO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�����������ҺpH�Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��

A. Ϊ��þ����ܴ���NaHCO3���˿�����Һ��pHΪ7��9֮��
B. pH=10.25ʱ��c(Na+)=c(CO32��)+c(HCO3��)
C. ����ͼ�����ݣ����Լ���õ�H2CO3��һ�������ƽ�ⳣ��K1(H2CO3)=10��6.37
D. ����0.1mol NaOH��Ӧ�����õ�1L��Һ��pH=10ʱ����Һ�д������¹�ϵ�� c(Na+)��c(HCO3��)��c(CO32��)��c(OH��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ת����ϵ�ж�����˵����ȷ����(��Ӧ��������ȥ)��
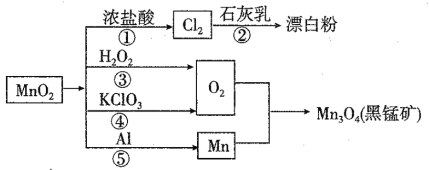
A. ��Ӧ�٢ڢۢܢݾ�����������ԭ��Ӧ�����ӷ�Ӧ
B. ��Ӧ��˵��������������������ǿ����
C. ���ɵ�����O2����Ӧ�ۺ͢�ת�Ƶĵ�����֮��Ϊ1��2
D. ��Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����X��Al2O3��Fe2O3��Cu��SiO2�е�һ�ֻ���������ɡ���������ʵ�顣�����й�˵����ȷ���ǣ�

A. ������������II���Եó�m(Fe2O3)��m(Cu)��1��1
B. ����I�м��ٵ�3 g����һ���ǻ����
C. ����II���������ٵ�����һ����Cu
D. ���ݲ���I��II�����жϻ����X�ijɷ�ΪAl2O3��Fe2O3��Cu��SiO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����ȡClO2�Ļ�ѧ��Ӧ:2NaClO3+SO2+H2SO4![]() 2ClO2+2NaHSO4,����˵������ȷ����
2ClO2+2NaHSO4,����˵������ȷ����
A. NaClO3�ڷ�Ӧ��ʧȥ����
B. SO2�ڷ�Ӧ�б�����
C. H2SO4�ڷ�Ӧ����������
D. 1 mol�������ڷ�Ӧ�еõ�2 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W����ͼ��ʾ��ת����ϵ����X��Y������ �� ��
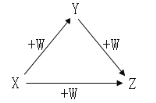
��Na��Na2O2 ��AlCl3��Al(OH)3 ��Cl2��FeCl3 ��C��CO
A. �٢� B. �ڢ� C. �ۢ� D. �ڢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com