
【题目】在标准状况下,35.5g氯气的体积是___L,将其与氢气完全化合生成氯化氢的物质的量是___mol,将生成的气体制成1L溶液,溶质的物质的量浓度是___mol/L,将此溶液取出20mL加蒸馏水稀释成200mL溶液,此稀稀后的溶液中溶质的物质的量浓度是___mol/L。
科目:高中化学 来源: 题型:
【题目】图a是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,图b是反应中的CO和NO的浓度随时间变化的示意图。根据图意回答下列问题:
a 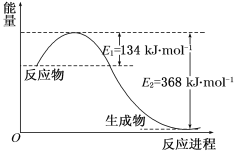 b
b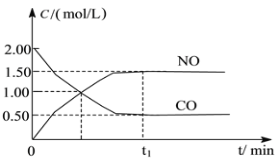
(1)写出NO2和CO反应的热化学方程式_______________。
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)=__________。
(3)此温度下该反应的平衡常数K=_________;温度降低,K________(填“变大”、“变小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同分异构现象在有机化学中普遍存在,中学阶段常见的同分异构体有三类。① 官能团异构(类别异构):是指由于官能团的不同而引起的同分异构现象。② 官能团位置异构:是指由于官能团取代的位置不同而引起的同分异构现象。③碳链异构:是指由于碳原子的排列顺序不同而引起的同分异构现象。已知分子式为C5H12O的有机物有很多同分异构体,下面给出其中的四种:
A.CH3—CH2—CH2—CH2—CH2OH B.CH3—O—CH2—CH2—CH2—CH3
![]()
![]()
根据上述信息完成下列各题:
(1) 根据所含官能团判断,A属于________类有机化合物,B物质的官能团名称为____________。B、C、D中,与A互为官能团异构的是________(填代号,下同),互为碳链异构的是________,互为官能团位置异构的是________
(2) 写出与A互为官能团位置异构(但与B、C或D不重复)的有机物的结构简式:_____________
(3) 与A互为碳链异构的同分异构体共有5种,除B、C或D中的一种外,其中两种的结构简式为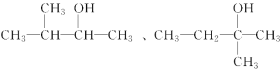 ,写出另外两种同分异构体的结构简式:____________________、_______________________。
,写出另外两种同分异构体的结构简式:____________________、_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1)Fe2+的M层电子排布式____________。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______I3(Mn)(填“>”、“<")。
(2)第四周期中,与Al原子未成对电子数相同的金属元素有_______种。气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为_________。根据等电子原理,AlO2-的空间构型为____________。科学实验证明:通常状态下并不存在NaAlO2 , Al(OH)3溶于强碱溶液形成的阴离子,实际是因为Al(OH)3分子中铝原子最外层电子数未达到饱和 ,能与OH-离子形成配位键,Al(OH)3与碱反应时只能中和1molOH-,表现为一元酸,写出Al(OH)3表现酸性的电离的方程式______________;
(3)Fe(CO)5的熔点为-20℃,沸点为103℃,易溶于乙醚,在Fe(CO)5中铁的化合价为_______,在Fe(CO)5中σ键和π键的数目之比为______。
(4)配位化合物K3[Fe(CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n=_____。产生的蓝色沉淀的化学式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.标准状况下,11.2LH2O含有的分子数为0.5NA
C.在常温常压下,71gCl2所含分子数为NA
D.标准状况下,32gO2中含有的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数值。下列有关叙述正确的是
为阿伏加德罗常数值。下列有关叙述正确的是
A.标准状况下,5.6LCO2中含有的共用电子对数目为2NA
B.标准状况下,22.4L苯中含有分子的数目为NA
C.1mol![]() 水解生成的
水解生成的![]() 胶体粒子数为NA
胶体粒子数为NA
D.在反应![]() 中,每生成3mol
中,每生成3mol![]() 转移的电子数为
转移的电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH 固体配制1.0mol/L的NaOH溶液240mL。
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、___。
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为___g,要完成本实验该同学应称出___gNaOH。
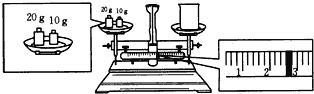
(3)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是___。
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究化学能与热能的转化,某实验小组设计了如下图所示的三套实验装置:
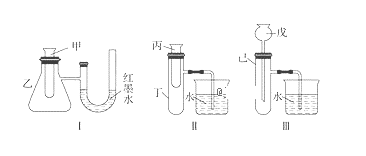
(1)上述3个装置中,不能验证“铜与浓硝酸的反应是吸热反应还是放热反应”的装置是_____(填装置序号)。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管中加入适量Ba(OH)2溶液与稀硫酸,U形管中可观察到的现象是___________。说明该反应属于______(填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在丙试管中进行)。
若观察到烧杯中产生气泡,则说明M溶于水___(填“一定是放热反应”、“一定是吸热反应”或“可能是放热反应”),理由是_____。
(4)至少有两种实验方法能验证超氧化钾与水的反应(4KO2+2H2O![]() 4KOH+3O2↑)是放热反应还是吸热反应。
4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择装置______(填装置序号)进行实验;
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是_____(填“吸热”或“放热”)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的产物中,存在同分异构体的是( )
A. CH3CH2CH2Br在碱性溶液中水解
B. 甲苯在催化剂作用下与Cl2发生苯环上的取代反应
C. ![]() 与NaOH的醇溶液共热反应
与NaOH的醇溶液共热反应
D. ![]() 在催化剂存在下与H2完全加成
在催化剂存在下与H2完全加成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com