
【题目】请按要求回答下列问题:
(1)胃舒平是治疗胃酸(HCl)过多的常用药物,其中含有的有效成分是不溶物氢氧化铝。其治疗原理是(用离子方程式表示)_______。
(2)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,生成两种化合物,其中一种是还原性气体且有毒性,该反应的化学方程式是_______。
(3)反应2H2CrO4+3H2O2=2Cr(OH)3 +3O2↑+2H2O中H2O2的变化过程为H2O2→O2。
①该反应的还原剂是________(填化学式)。
②在该反应方程式中用双线桥法标明电子转移的方向和数目。________
2H2CrO4+3H2O2=2Cr(OH)3+3O2↑+2H2O
③若反应中转移了3mol电子,则产生的气体在标准状况下体积为_______L。
【答案】Al(OH)3+3H+=Al3++3H2O Al2O3+3Cl2+3C![]() 2AlCl3 +3CO H2O2
2AlCl3 +3CO H2O2 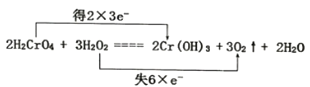 33.6
33.6
【解析】
(1)氢氧化铝与盐酸反应产生氯化铝和水;
(2)Al2O3与C、Cl2在高温条件下反应,生成AlCl3和CO;
(3)根据元素化合价升高,失去电子,被氧化,物质作还原剂;元素化合价降低,获得电子,被还原,物质作氧化剂,氧化剂获得电子总数与还原剂失去电子总数相等,等于反应过程中元素化合价升降总数,据此分析解答。
(1)氢氧化铝与盐酸反应产生氯化铝和水,用离子方程式表示为:Al(OH)3+3H+=Al3++3H2O;
(2) Al2O3与C、Cl2在高温条件下反应,生成AlCl3和CO,根据电子守恒、原子守恒,可得该反应的方程式为:Al2O3+3Cl2+3C![]() 2AlCl3 +3CO;
2AlCl3 +3CO;
(3)①在反应2H2CrO4+3H2O2=2Cr(OH)3 +3O2↑+2H2O中,Cr元素的化合价由反应前H2CrO4中的+6价变为反应后Cr(OH)3 中的+3价,化合价降低,获得电子2×3e-,被还原,H2CrO4作氧化剂;O元素的化合价由反应前H2O2中的-1价变为反应后O2中的0价,化合价升高,失去电子6×e-,H2O2作还原剂;
②根据①分析,反应过程中电子转移用线桥法标明电子转移的方向和数目为 ;
;
③在反应2H2CrO4+3H2O2=2Cr(OH)3+3O2↑+2H2O中,每转移6mol电子,反应会产生3molO2,则反应中转移了3mol电子,产生1.5molO2,产生的O2气体在标准状况下体积V(O2)=1.5mol×22.4L/mol=33.6L。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.1 mol CH≡CH可以与Br2发生加成反应,消耗2 mol Br2
B.苯的邻位二元取代物只有一种可以说明苯分子不具有碳碳单键和碳碳双键的交替结构
C.甲苯(![]() )可以发生取代反应,不能发生加成反应
)可以发生取代反应,不能发生加成反应
D.正己烷的沸点高于2-甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铝(AlP)是一种常用于粮食仓储的广谱性熏蒸杀虫剂,遇水立即产生高毒性气体 PH3(沸点-89.7℃,还原性强)。国家卫计委规定粮食中磷化物(以PH3计)的残留量不超过0.0500 mg/kg时为质量合格,反之不合格。某化学兴趣小组的同学用下述方法测定某粮食样品 中残留磷化物的质量以判断是否合格。
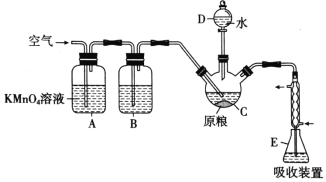
在C中加入100g原粮,E中加入20.00 mL 2.50×10-4 mol/ L KMnO4溶液(H2SO4酸化),往C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中过量的KMnO4溶液。回答下列问题:
(1)PH3的电子式为___________。仪器C的名称是___________。
(2)A中酸性高锰酸钾溶液的作用是___________通入空气的作用是______________________。
(3)PH3也可被NaClO氧化可用于制备NaH2PO2,制得的NaH2PO2和NiCl2溶液可用于化学镀镍, 同时生成磷酸和氯化物,请写出化学镀镍的化学方程式为______________________________。
(4)装置E中PH3被氧化成磷酸,充分反应后的吸收液,加水稀释至250mL,取25.00mL于锥形瓶中,用4.0×10-5mol/L的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液 20.00mL,Na2SO3与KMnO4溶液反应的离子方程式为:SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平),则滴定终点的现象为______________________________________________。
该原粮样品中磷化物(以PH3计)的残留量为__________________mg/kg。(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能表示H2(g)+ I2(g)![]() 2HI(g)已经达到平衡状态的标志有几个( )
2HI(g)已经达到平衡状态的标志有几个( )
①c(H2)=c(I2)=c(HI)时②c(H2):c(I2):c(HI)=1:1:2时③c(H2)、c(I2)、c(HI)不再随时间而改变④单位时间内生成nmolH2的同时生成2nmolHI⑤单位时间内生成n mol H2的同时生成n mol I2⑥反应速v(H2)=v(I2)=1/2v(HI)⑦一个H-H键断裂的同时有两个H-I键断裂⑧温度和体积一定时,容器内压强不再变化⑨温度和体积一定时,混合气体的颜色不再变化⑩温度和压强一定时,混合气体的密度不再变化条件一定,混合气体的平均相对分子质量不再变化
A. 3B. 4C. 5D. 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
(1) N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)→2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是__________。
A.N2O分解反应中:分解速率与是否含碘蒸气有关 B.第三步对总反应速率起决定作用
C.第二步活化能比第三步小 D.IO为反应的催化剂
(2)汽车尾气中含有较多的氮氧化物和不完全燃烧的CO,汽车三元催化器可以实现降低氮氧化物的排放量。汽车尾气中的NO(g)和CO(g)在催化剂的作用下转化成两种无污染的气体。如,
反应I:2CO +2NO → N2+2CO2 △H1; 反应II:4CO +2NO2 → N2+4CO2 △H2<0。
针对反应I:①已知:反应N2(g)+O2(g)=2NO(g) △H3=+180.0kJ·mol1,若CO的燃烧热为-283.5kJ·moll 则反应I的△H1=_________kJ·mol1。
②若在恒容的密闭容器中,充入2molCO和1molNO,发生反应I,下列选项中不能说明该反应已经达到平衡状态的是_______。
A.CO和NO的物质的量之比不变 B.混合气体的密度保持不变
C.混合气体的压强保持不变 D.2v(N2)正=v(CO)逆
(3)根据原电池原理和电解原理进行如图回答。请回答: 用如图所示装置进行实验(K闭合).
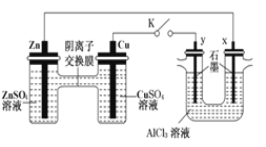
①Zn极为________极;实验过程中,SO42-________(填“从左向右”、“从右向左”或“不”)移动。
②y极的电极反应现象为________;
③写出生活中对钢闸门的一种电化学保护方法________________________。
④有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HClNH4Cl为电解质溶液制取新型燃料电池,请写出该电池的正极反应式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把aL含硫酸铵和硝酸铵的混合液分成两等份,一份需用b mol烧碱刚好把铵根离子全部赶出,另一份与氯化钡溶液反应时,消耗c mol氯化钡,由此可知原溶液中NO3—的物质的量浓度是(单位:mol·L—1) ( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为:KClO3+HCl(浓)== KCl+ClO2↑+Cl2↑+。
(1)请 写出完整的化学方程式并配平_______。
(2)浓盐酸在反应中显示出来的性质是_______(填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)用双线桥法标明电子转移的方向和数目____。
(4)产生0.1molCl2,则转移的电子的物质的量为___mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL,下列叙述不正确的是( )

A.某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。则烧杯的实际质量为27.4 g
B.要完成本实验该同学应称出10.0g NaOH
C.氢氧化钠固体溶解后必须恢复至室温再进行转移
D.容量瓶使用前需洗涤、并保持干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验所用试剂、现象和结论均正确的是
选项 | 实验装置 | 现象 | 结论 |
A |
| 装置Ⅲ中有浅黄色沉淀 | 苯和浓溴水发生取代反应 |
B |
| 高锰酸钾溶液褪色,溴的四氯化碳溶液褪色 | 石蜡油的分解产物中含有不饱和烃 |
C |
| 盛有饱和碳酸钠溶液的试管中,上方出现油状液体 | 制备乙酸乙酯 |
D |
| 甲醚有气泡 | 鉴别乙醇与甲醚(CH3OCH3) |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com