
科目: 来源: 题型:解答题
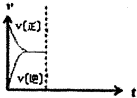 已知三个反应如下:
已知三个反应如下:| T/℃ | 700℃ | 800℃ |
| K1 | 2.38 | 2.56 |
| K2 | 0.80 |
| 反应时间/min | 0 | 2 | 4 | 6 |
| N(CO)/mol | 1.20 | 0.90 | 0.80 | |
| N(H2O)/mol | 0.60 | 0.20 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验序号 | 浓度(mol/L) | 时间(min) | |||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | |||
| 1 | 温 度 | 800℃ | 1.0 | 0.80 | O.64 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 | |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 | |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 | |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将容器体积变为原来一半 | B. | 压强变为原来一半 | ||
| C. | 加入2n molCO,2n molH2O | D. | 加入2n molCO2和2n molH2 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验题
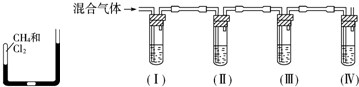
查看答案和解析>>
科目: 来源: 题型:填空题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目: 来源: 题型:解答题
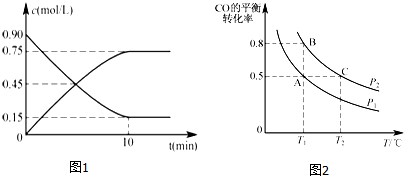 甲醇是一种重要的可再生能源.
甲醇是一种重要的可再生能源.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 两种难溶电解质,Ksp小的溶解度一定小 | |
| B. | 0.1 mol AgCl和0.1 mol AgI混合后加入1 L水中,所得溶液中c(Cl-)=c(I-) | |
| C. | 在硫酸钡的沉淀溶解平衡体系中加入蒸馏水,硫酸钡的Ksp增大 | |
| D. | 用锌片作阳极,铁片作阴极,电解ZnCl2溶液,铁片表面出现一层锌 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用HCl溶液代替蒸馏水洗涤AgCl,可以减少沉淀损失 | |
| B. | 将BaSO4固体加入到饱和Na2CO3溶液中,充分反应后过滤、洗涤;往滤渣中滴加稀盐酸,有气体产生,则证明此条件下Ksp(BaSO4)>Ksp(BaCO3) | |
| C. | 向水中加入NaHCO3或NaHSO4固体后,水的电离程度均增大 | |
| D. | 对于乙酸乙酯的水解反应,加入稀硫酸可提高反应速率和乙酸乙酯的转化率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com