3.从含铜废料(如:覆铜板、印刷线路板及铅冰铜等)中提取铜,既可提高资源的利用率又可减少重金属污染.
(1)废覆铜板(Cu和Sn组成)可用CuSO
4和H
2SO
4混合溶液作电解质溶液,直接电解回收精铜,阳极上发生的电极反应为Cu-2e
-=Cu
2+和Sn-2e
-=Sn
2+.
(2)废印刷线路板中的铜常用含盐酸的FeCl
3溶液或H
2O
2-HCl-NaCl混合溶液浸取回收.
①用FeCl
3溶液浸取铜时发生反应的离子方程式为2Fe
3++Cu=2Fe
2++Cu
2+;若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀,产生红褐色沉淀的原因是c(H
+)和c(Fe
3+)小,有利于Fe
3+水解生成Fe(OH)
3沉淀.
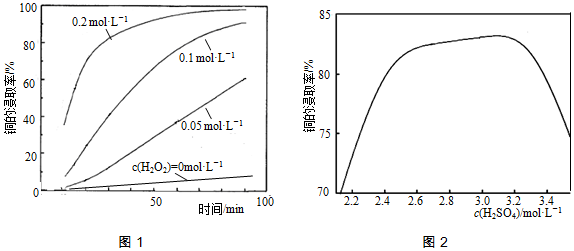
②将粉碎后的废印刷线路板放入三口烧瓶中,分别加入由0.3mol•L
-1盐酸、0.5mol•L
-1NaCl及不同浓度的H
2O
2组成的混合溶液,在温度、搅拌速率及固液比等均相同时,铜的浸取率随H
2O
2的浓度和时间的变化如图1所示.当c(H
2O
2)=0mol•L
-1时,也有少量的铜被浸出,其原因是液面上方空气中O
2随搅拌不断进入溶液,溶解的O
2将铜氧化而被浸取.
③用H
2O
2-HCl-NaCl混合溶液浸取时,其浸取过程包括:
(Ⅰ) Cu+H
2O
2+2H
+=Cu
2++2H
2O
(Ⅱ) Cu
2++Cu?2Cu
+(Ⅲ) Cu
++nCl
-?CuCl
n(n-1)-(Ⅳ) 2CuCl
n(n-1)-+2H
++H
2O
2=2Cu
2++2H
2O+2nCl
-其他条件相同时,增大下列离子浓度可以加速Cu从废电路板中浸出的是bc(填序号).
a.Na
+ b.Cu
2+ c.Cl
-d.OH
-
(3)铅冰铜(PbS、Cu
2S及FeS的混合物)可用HCl-H
2O
2混合溶液浸取.
①Cu
2S被HCl-H
2O
2混合溶液浸取得到硫酸铜和氯化铜溶液的化学方程式为Cu
2S+5H
2O
2+2HCl=CuCl
2+CuSO
4+6H
2O.
②若由H
2SO
4代替HCl-H
2O
2中的HCl,其他条件相同,铜的浸取率随硫酸浓度的变化如图2所示.当H
2SO
4浓度大于3.1mol•L
-1时,硫酸浓度越大,铜的浸取率反而越小,其原因可能是过量的硫酸会生成PbSO
4沉淀包裹在铅冰铜颗粒表面,使铜无法与浸出液接触.

