
科目: 来源: 题型:阅读理解
| 名称 | 性质 |
| 乙二醇 | 无色粘稠吸湿液体,易燃,沸点:196~198℃,与水混溶. |
| 丙酮 | 无色易燃液体,沸点:56.5℃,溶于水及大多数有机溶剂. |
| N,N二甲基甲酰胺(DMF) | 易燃,低毒,沸点:153℃,能与水和大多数有机溶剂混溶. |
| 对苯二甲酸(TPA) | 白色针状结晶或粉末,可燃,熔点:425℃(分解),约在300℃升华,不溶于水,微溶于热乙醇,溶于碱溶液.电离常数:Ka1=3.1×10-4,Ka2=1.5×10-5 |
查看答案和解析>>
科目: 来源: 题型:
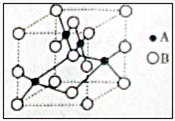 (2010?南京二模)纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.
(2010?南京二模)纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.查看答案和解析>>
科目: 来源: 题型:
滴定次数 |
0.05000mol?L-1Na2S2O3标准溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | |
| 1 | 0.00 | 20.04 |
| 2 | 0.12 | 20.08 |
| 3 | 0.05 | 20.05 |
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.核外电子排布相同的两种粒子其化学性质一定相同
B.所有原子都是由质子、中子和电子构成的
C.质子数和电子数均分别相同的阳离子和阴离子是不存在的
D.质子数相同的粒子,其核外电子排布也相同
查看答案和解析>>
科目: 来源: 题型:








| 次硫酸 |
| ℃170 |
| Br |


查看答案和解析>>
科目: 来源: 题型:阅读理解
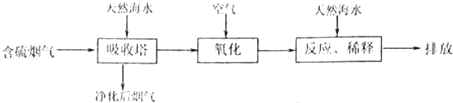
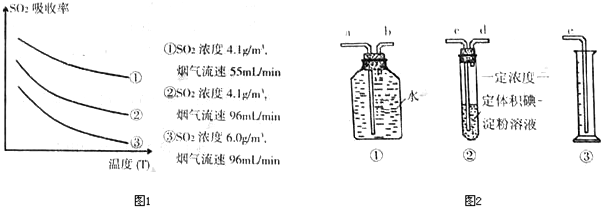
查看答案和解析>>
科目: 来源: 题型:
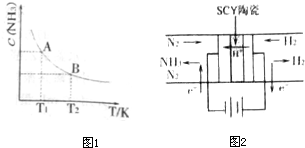
查看答案和解析>>
科目: 来源: 题型:
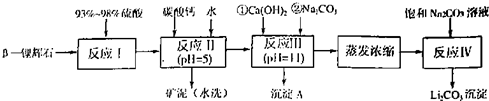
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
查看答案和解析>>
科目: 来源: 题型:
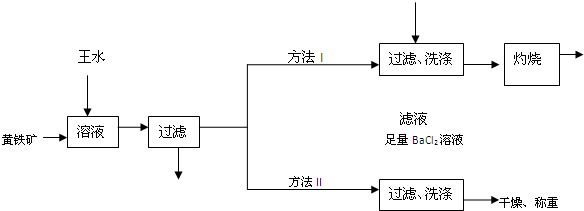
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com