
科目: 来源: 题型:
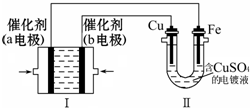 如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),电池总反应为:CH4+2O2+2KOH=K2CO3+3H2O,通过装置Ⅱ实现铁棒上镀铜.下列说法正确的是( )
如图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),电池总反应为:CH4+2O2+2KOH=K2CO3+3H2O,通过装置Ⅱ实现铁棒上镀铜.下列说法正确的是( )查看答案和解析>>
科目: 来源: 题型:
 已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色).如图连接好装置,往铁电极区滴入2滴黄色的K3[Fe(CN)6](铁氰化钾)溶液.下列说法正确的是( )
已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色).如图连接好装置,往铁电极区滴入2滴黄色的K3[Fe(CN)6](铁氰化钾)溶液.下列说法正确的是( )查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 装置 | 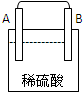 |
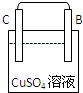 |
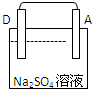 |
| 现象 | B棒有气泡 | C棒有Cu析出 | A棒附近PH升高 |
| ① | ② | ③ | |
| 四种金属活动性由强到弱的顺序: D>A>B>C D>A>B>C | |||
查看答案和解析>>
科目: 来源: 题型:
 将镁带投入盛放在敞口容器的盐酸里,产生H2的速率与 时间的关系可由图表示.
将镁带投入盛放在敞口容器的盐酸里,产生H2的速率与 时间的关系可由图表示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com