
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在0.01mol·L-1Ba(OH)2溶液中:Al3+、NH4+、NO![]() 、HCO
、HCO![]()
B.0.1mol/L的FeCl2溶液中:H+、Al3+、SO42-、ClO-
C.滴加KSCN溶液显红色的溶液:NH4+、K+、Cl-、I-
D.由水电离产生的c(H+)=1×10-13mol·L-1的溶液中:Na+、Ba2+、NO![]() 、Cl-
、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸240ml。
(1)在盛放浓硫酸的试剂瓶的标签上应印有下列警示标志中的____________。

(2)选用的主要仪器有:__________
①烧杯,②玻璃棒,③量筒,④胶头滴管,⑤____________。
(3)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至凹液面恰好与刻度线相切
D.稀释浓H2SO4
E.将冷却后的稀释液转入容量瓶
F.将蒸馏水注入容量瓶,直到液面距刻度线1-2cm处
G.用少量蒸馏水洗涤烧杯和玻璃棒2-3次,并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀,其操作正确的顺序依次为____________________________。
(4)简要回答下列问题:
①所需浓硫酸的体积为____________mL,如果实验室有10mL、20mL、50mL的量筒应选用____________mL的量筒最好
②下列操作使所配溶液浓度偏高的是__________
A.用水洗涤量取浓硫酸的量筒,并将洗涤液转入容量瓶中
B.用量筒来量取浓硫酸,读数时,俯视量筒
C.搅拌过程中有液体溅出
D.在转入容量瓶前烧杯中液体未冷却至室温
E.定容时,俯视刻度线
F.容量瓶用蒸馏水洗净后未经干燥马上用来配制溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在下列物质中①![]() Li ②
Li ②![]() Na③
Na③![]() Mg④
Mg④![]() Li⑤
Li⑤![]() C⑥C60⑦异丁烷⑧正丁烷⑨石墨
C⑥C60⑦异丁烷⑧正丁烷⑨石墨
互为同位素的是 (填编号,下同);互为同素异形体的是 ;
互为同分异构体的是 。
(2)在下列事实中,是什么因素影响了化学反应的速率?
夏天的食品易发霉,冬天就不易发生该现象。影响因素是 ;
MnO2加入双氧水中反应更剧烈。影响因素是 ;
同浓度、同体积的盐酸中放入同样大小的锌粒和镁条,镁条产生气体更快。影响因素是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】CO和联氨(N2H4)的性质及应用的研究是能源开发、环境保护的重要课题。
(1)①用CO、O2和KOH溶液可以制成碱性燃料电池,则该电池反应的离子方程式为 。
②用CO、O2和固体电解质还可以制成如下图1所示的燃料电池,则电极d的电极反应式为 。
(2)联氨的性质类似于氨气,将联氨通入CuO浊液中,有关物质的转化如图2所示。
①在图示2的转化中,化合价不变的元素是 (填元素名称)。
②在转化过程中通入氧气发生反应后,溶液的pH将 (填“增大”、“减小”或“不变”)。转化中当有1 mol N2H4参与反应时,需要消耗O2的物质的量为 。
③加入NaClO时发生的反应为:Cu(NH3)![]() +2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
+2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
该反应需在80℃以上进行,其目的除了加快反应速率外,还有 、 。
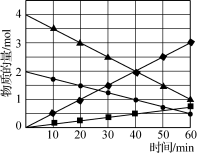
图3
(3)CO与SO2在铝矾土作催化剂、773 K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫,反应体系中各组分的物质的量与反应时间的关系如图3所示,写出该反应的化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下面是我们熟悉的物质:
①O2②SO2③CaCl2④HNO3⑤NaOH ⑥NH4Cl
这些物质中,属于共价化合物的是 ___________;属于离子化合物的是___________;只含离子键的是___________。
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
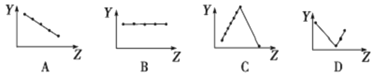
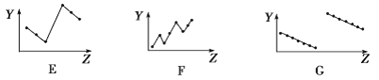
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数________________。
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径________________。
③第二、三周期主族元素随原子序数递增原子半径的变化____________。
(3)已知某单核粒子的结构示意图为:![]()
①当x-y=10时,该粒子为____________(填“原子”、“阳离子”或“阴离子”)。
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是_____________。
(4)已知A、B、C、D是中学化学中常见的四种10电子微粒,
它们之间存在如图中转化关系。
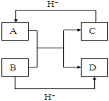
请写出:A的化学式 (写一种);D的化学式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,将1mol的CuSO45H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2:CuSO45H2O受热分解的化学方程式为CuSO45H2O(s) ![]() CuSO4(s)+5H2O(l),热效应为△H3,则下列判断正确的是( )
CuSO4(s)+5H2O(l),热效应为△H3,则下列判断正确的是( )
A.△H2>△H3 B.△H1<△H3
C.△H1+△H3=△H2 D. △H1+△H2>△H3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图示与对应叙述相符的是
A.图甲表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
B.图乙表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化
C.图丙表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂
D.图丁表示一定浓度Na2CO3溶液中滴加盐酸,生成CO2与滴加盐酸物质的量的关系
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,一密闭容器被无摩擦、可滑动的两隔板a和b分成甲、乙两室。标准状况下,在乙室中充入1.2molHCl,甲室中充入NH3、H2的混合气体,静止时活塞位置如下图。已知甲室中气体的质量比乙室中气体的质量少33.8g。

请回答下列问题:
(1)甲室中气体的物质的量为___________mol。
(2)甲室中气体的质量为__________g。
(3)甲室中NH3、H2的物质的量之比为_____________,质量比为___________。
(4)经过查资料知道HCl+NH3=NH4Cl(NH4Cl常温下是固体,假设固体的体积可忽略),如果将板a去掉,当HCl与NH3完全反应后,活塞b将静置于刻度“___________”处(填数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】通常用燃烧的方法测定有机物的的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。下图所示的是用燃烧法确定有机物分子式的常用装置。
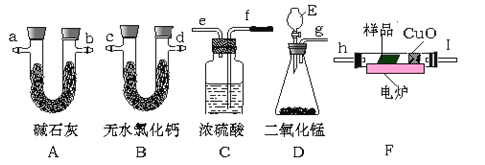
现准确称取1.8g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76g,B管增重0.36g。请回答:
(1)用该方法可测定含有哪些元素和什么状态的有机物_________________;
(2)A、B管内均盛有固态试剂,B管的作用是__________________;
(3)产生的气体由左向右流向,所选用的各导管口连接的顺序是__________________。
(4)E中应盛装什么试剂:______________。
(5)如果把CuO网去掉,A管重量将_______;(填“增大”、“减小”、或“不变”)
(6)该有机物的最简式为__________________;
(7)要确定该有机物的分子式,还必须知道的数据是___________;
A.消耗液体E的质量
B.样品的摩尔质量
C.CuO固体减少的质量
D.C装置增加的质量
E.燃烧消耗O2的物质的量
(8)在整个实验开始之前,需先让D产生的气体通过整套装置一段时间,其目的是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示。下列有关的说法错误的是( )
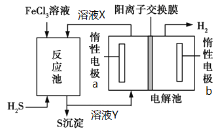
A. 惰性电极a发生氧化反应
B. Fe(OH)3胶体中滴加溶液X,先有沉淀后沉淀溶解
C. 溶液Y加热蒸发灼烧最终得到Fe2O3
D. 电解池总反应的离子方程式为2Fe2++2H+![]() 2Fe3++H2↑
2Fe3++H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com