
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A.常温常压下,48gO3 和O2混合气体含有的氧原子数为3NA
B.24g金属镁变为镁离子时失去的电子数为NA
C.4℃时9mL水和标准状况下11.2L氮气含有相同的原子数
D.同温同压下,NA个NO与NA个N2和O2的混合气体的体积不相等
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组同学通过下列流程制取不溶于水和稀硫酸的黄钾铵铁矾[KNH4Fex(SO4)y(OH)z],并通过实验测定样品中黄钾铵铁矾的有关组成。

实验测定:
①称取一定质量的样品加入稀盐酸中充分溶解,将所得溶液转移至容量瓶并配制成l00mL溶液A;
②量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32g;
③量取25.00mL溶液A,加入足量KI,用2.000mol·L﹣1Na2S2O3溶液进行滴定(已知反应为I2+2Na2S2O3═2NaI+Na2S4O6,消耗30.00mL Na2S2O3溶液至终点。
(1)在[KNH4Fex(SO4)y(OH)z]中x、y、z的代数关系式为 。
(2)若加入H2SO4将pH调节为2,则溶液c(Fe3+)应为 mol·L﹣1。(已知Ksp[Fe(OH)3]=4.0×10﹣38)
(3)实验测定②中检验沉淀是否完全的方法是 。
(4)根据以上实验数据计算样品中的n(Fe3+)∶n(SO42﹣)。(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下反应:2A(g)+B(g) ![]() 3C(g) ΔH<0,在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
3C(g) ΔH<0,在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
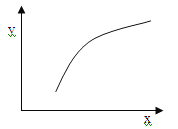
选项 | x | y |
A | A的浓度 | 平衡常数K |
B | 温度 | 混合气体的密度 |
C | B的物质的量 | A的转化率 |
D | 催化剂的质量 | C的体积分数 |
查看答案和解析>>
科目: 来源: 题型:
【题目】在相同温度下,体积均为1 L的四个密闭容器中,保持温度和容积不变,以四种不同的投料方式进行反应。平衡时有关数据如下(已知2SO2(g)+O2(g) ![]() 2SO3(g)ΔH=-196.6 kJ·mol-1)。
2SO3(g)ΔH=-196.6 kJ·mol-1)。
容器 | 甲 | 乙 | 丙 | 丁 |
起始投料量 | 2molSO2 1mol O2 | 1 mol SO2 0.5mol O2 | 2mol SO3 | 2mol SO2 2mol O2 |
反应放出或吸收的热量(kJ) | a | b | c | d |
平衡时c(SO3) (mol·L-1) | e | f | g | h |
下列关系正确的是( )
A.a=c;e=g B.a>2b;e>2f C.a>d;e>h D.c+98.3e>196.6
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关氨或铵盐的说法不正确的是
A.NH3属于弱电解质
B.可用湿润的红色石蕊试纸检验氨气
C.用盐酸滴定氨水,当溶液呈中性时,c(NH4+) = c(Cl-)
D.常温时,0.1mol·L-1NH4Cl溶液加水稀释,![]() 的值不变
的值不变
查看答案和解析>>
科目: 来源: 题型:
【题目】(下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
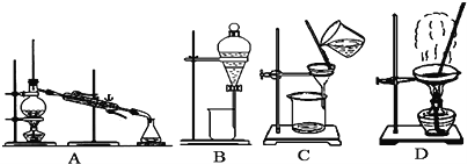
(1)写出图中标序号的对应仪器名称:②_________________,③_______________。仪器②中水流方向为___________(填“上进下出”或 “下进上出”)
(2)选择合适的实验方法分离下列混合物,用代表整套装置的字母填空;
①从氯化钾溶液中得到氯化钾固体,选择装置____________;
②分离饱和食盐水与沙子的混合物,选择装置____________;
③除去自来水中的Cl-等杂质以制取蒸馏水,选择装置____________;
④分离乙醇和水的混合物,选择装置________;
⑤分离汽油和水的混合物,选择装置____________;
(3)分离碘和水的混合物,可选择下列哪种试剂?_______(填序号),所用分离方法为________。
A.四氯化碳 B.乙醇 C.蒸馏水
查看答案和解析>>
科目: 来源: 题型:
【题目】
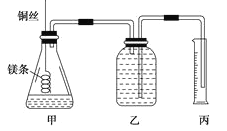
② 配制100mL.1.0mol·L-1的盐酸溶液;
②用__________(填仪器名称并注明规格)量取10.0mL 1.0mol·L-1的盐酸溶液加入锥形瓶甲中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为__________g;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为VmL。
请将上述步骤补充完整并回答下列问题。
(1)步骤①中,配制100mL 1.0mol·L-1的盐酸溶液时,下列哪些操作会使配制浓度偏小________(填写字母)。
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
(2)请填写操作步骤中的空格:步骤②_________,步骤③_________g。
(3)实验步骤⑤中应选用____________(填字母)的量筒;
A.100mL B.200mL C.500mL
读数时除恢复到室温,调节乙丙内液面相平外,还要注意 。
(4)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=____________L/mol。
(5)若未除去镁条表面的氧化镁,则测得该条件下气体的摩尔体积 (填偏大、偏小或无影响)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com