
科目: 来源: 题型:
【题目】工业上湿法制高铁酸钾的基本流程如下:
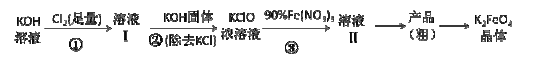
已知:高铁酸盐热稳定性差
回答下列问题:
(1)第③步发生反应的离子方程式 。
(2)第③步反应的体系,温度不宜过高,并最好控制温度在 30℃以下,其原因是 。
(3)通过结晶方法从溶液II得到的粗产品中主要含有杂质 (填化学式),可通过重结晶法提纯K2FeO4,具体操作步骤有:将粗产品先用饱和KOH溶液溶解,然后浓缩、冷却结晶、过滤、洗涤、干燥。其干燥可采用的方法是 (写出一种干燥方法)。
(4)利用电化学原理,用铁钉和氢氧化钾溶液为原料可以获得K2FeO4。在制备过程中铁钉作______极,请写出获得FeO42-的电极反应式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 碘晶体受热转变为碘蒸气,吸收的热量用于克服碘原子间的作用力
B. 硫酸钾和硫酸溶于水都电离出硫酸根离子,所以它们在熔融状态下都能导电
C. 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成
D. H2和Cl2在光照条件反应生成HCl,一定有共价键的断裂和形成
查看答案和解析>>
科目: 来源: 题型:
【题目】为了除去MgCl2酸性溶性中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸。这种试剂是
A. NH3·H2O B. NaOH C. Na2CO3D.MgO
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于SO2的说法中,不正确的是( )
A. SO2是酸性氧化物
B. SO2是形成酸雨的主要污染物之一
C. SO2与水反应生成H2SO4
D. 高温下SO2可被催化氧化生成SO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列意外事故的处理方法中,错误的是( )
A.皮肤烫伤后刺痛发红,应立即用凉水冲洗、浸泡
B.温度计打破,其中的水银流出,立即把看得见的水银收集并放入瓶中密闭,在洒落水银的地方撒上硫黄粉
C.在胶塞上安装玻璃管时,不小心手被玻璃管割伤,先除去伤口处的玻璃,再用75%的酒精擦洗水消毒,之后找医生敷药包扎
D.不小心将酒精灯碰倒在桌面上,燃烧起来,立即用手拍打把火扑灭
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D四种元素。A元素的离子具有黄色的焰色反应.B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100 mL2 mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。C单质新制水溶液为黄绿色且有漂白性,D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件,回答:
(1)元素C (填元素符号),写出C-离子的离子结构示意图 。
(2)写出元素的名称: B 、D ;
(3)A与D形成淡黄色的化合物的化学式为 ,
(4)C元素的单质有毒,可用A的最高价氢氧化物的溶液吸收,其离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O,发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
A. 在该温度下平衡常数K=1
B. 平衡常数与反应温度无关
C. CO的转化率为50%
D. 其他条件不变改变压强平衡不移动
查看答案和解析>>
科目: 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图

请根据以上信息回答下列问题:
(1)上图④的反应条件是点燃,请写出N_________(填化学式)。
(2)写出反应②电解饱和食盐水的化学方程式:______________________________。
(3)粗盐中含有Ca2+、Mg2+、SO等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为____________。
A.②③④① B.③②④①
C.④③②① D.③④②①
(4)提取粗盐后剩余的海水(母液)中,可用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是____________。
A.分解反应 B.化合反应 C.复分解反应 D.置换反应
(5)提取粗盐后剩余的海水(母液)中,可用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是____________。
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)过氧化钠保存不当容易变质,生成Na2CO3。判断过氧化钠在空气中是否变质的简单方法是观察颜色是否 。
(2)某过氧化钠样品已经部分变质,可以取少量样品,溶解,加入 溶液,充分振荡,看是否有白色沉淀,通过判断溶液中含有碳酸根来证明Na2O2已经变质
(3)检验样品中还有过氧化钠的方法是:取少量样品放入试管中,再加入适量的水,用 ,通过验证反应产生了氧气来证明样品中仍有Na2O2
(4)某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。
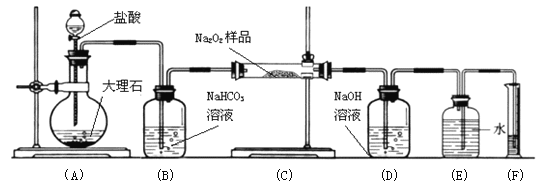
上图中的E和F构成量气装置,用来测定O2的体积。
写出装置A中发生反应的离子方程式:
装置B的作用是除去混在二氧化碳中的氯化氢气体,
NaOH的作用是
他们在读出量筒内水的体积数后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com