
科目: 来源: 题型:
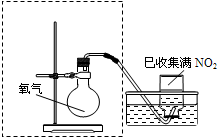 某小组设计实验,探究NO2被水吸收,力求达到:①NO2尽可能全部吸收 ②集气瓶中残留的气体尽可能少.
某小组设计实验,探究NO2被水吸收,力求达到:①NO2尽可能全部吸收 ②集气瓶中残留的气体尽可能少.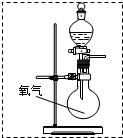

| 实验步骤 | 实验现象 | 化学方程式 | |
| ① | 将收集满NO2的集气瓶倒立 在水槽中 |
||
| ② | 气体由无色变成红棕色, 后又变成无色,液面继 续上升 | ||
| ③ | 其它现象与上相同.最后 瓶内只含极少量气体,液 体几乎充满 |
查看答案和解析>>
科目: 来源: 题型:


查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 观察要点或实验步骤 | 现象、结论或注意事项 | |
| 方法一 | 观察二者外观上的细小差别 | 呈 白色粉末 白色粉末 状的是碳酸钠,呈白色细小晶体 白色细小晶体 的是碳酸氢钠 |
| 方法二 | 分别滴入几滴水 | 结成块状并且试管底部温度较高的是 碳酸钠 碳酸钠 ;未结块并且试管底部温度较低的是 碳酸氢钠 碳酸氢钠 . |
| 方法三 | 再分别加入10mL水,滴入 1~2滴酚酞试液 |
该操作中加入水后应 用力振荡或用玻璃棒搅拌 用力振荡或用玻璃棒搅拌 ;滴入酚酞后应着重观察 所得溶液颜色的深浅 所得溶液颜色的深浅 . |
查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com