
科目: 来源: 题型:
【题目】(双选题)下列有关硫酸的化学事实与硫酸表现出的性质(括号中)的描述中,正确的是( )
A.久置在敞口容器中的浓硫酸,溶液质量增大(脱水性)
B.在加热条件下铁与浓硫酸反应(氧化性、酸性)
C.蔗糖与浓硫酸反应的“黑面包”实验(吸水性)
D.浓硫酸与氯化钠固体反应制HCl(难挥发性)
查看答案和解析>>
科目: 来源: 题型:
【题目】丁烷广泛应用于家用液化石油气及打火机中作燃料,下列关于丁烷叙述不正确的是( )
A. 常温下,C4H10是液体
B. C4H10和CH4互为同系物
C. 丁烷有正丁烷和异丁烷两种同分异构体
D. 丁烷在一定条件下与氯气发生取代反应
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W有如下图所示的转化关系,且ΔH=ΔH1+ΔH2,则X、Y可能是
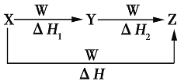
①C、CO ②S、SO2 ③AlCl3、Al(OH)3 ④Na2CO3、NaHCO3 ⑤Fe、FeCl2
A.①②③④⑤ B.②④⑤ C.①③④ D.①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】I.中和热测定是中学化学重要的定量实验
(1)实验中需要的玻璃仪器有__________________________;
(2)现通过相同体积(100mL),相同物质的量浓度(0.2mol·L-1)的硫酸和氢氧化钠溶液反应,测定中和热,实验测得反应时,溶液温度平均升高t℃,计算中和热的表达式ΔH=___________(假设溶液的密度,比热容与水的相同)。
II.过氧化钠是一种重要的氧化剂
(1)过氧化钠的电子式是______,其中含有的化学键类型是______;
(2)在氯化亚铁的溶液中加入与其等物质的量的Na2O2,恰好使氯化亚铁转化为氢氧化铁写出该反应的离子方程式:___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】假设反应N2+3H22NH3(正反应为放热反应) 的正反应速率是v1 , 逆反应速率是v2 , 当升高温度时,v1和v2的变化情况为( )
A.同时增大
B.v1减小,v2增大
C.同时减小
D.v1增大,v2减小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A.NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质
B. 蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质
C.铜、石墨均导电,所以它们是电解质
D.液态HCl、固态NaCl均不导电,所以HCl、NaCl均不是电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定体积的容器中加入1.5mol氙气(Xe)和7.5mol氟气(F2),于400℃和2633kPa压强下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气,则所得无色晶体产物中,氙与氟的原子个数之比是
A.1∶2 B.1∶3 C.1∶4 D.1∶6
查看答案和解析>>
科目: 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。

回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由 。
(5)用相同浓度和体积的稀醋酸代替稀盐酸进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度℃ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)反应②是________________(填“吸热”或“放热”)反应。
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如左下图所示。则平衡状态由A变到B时,平衡常数K(A)_____________K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______(用K1、K2表示)。
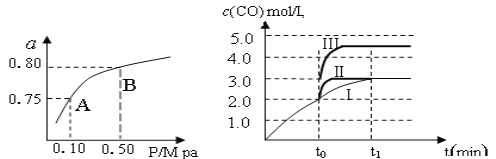
(3)在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如右上图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。
当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_____________________。
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_____________________。
(4)一种甲醇燃料电池,使用的电解质溶液是2mol·L-1的KOH溶液。
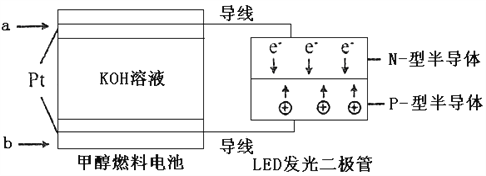
请写出加入(通入)b物质一极的电极反应式_________________;
每消耗6.4g甲醇转移的电子数为_______________。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合后,溶液中:2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数Ka为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com